Clear Sky Science · ar
يعطّل GLP-1 قنوات KATP في الخلايا الشِعرية التاجية كوسيط لإشارة الدماغ-الأمعاء-القلب التي تتوسط الحماية القلبية
لماذا حماية الأوعية القلبية الصغيرة مهمة
عندما يُعاد فتح شريان قلبي مسدود بعد نوبة قلبية، يفترض كثيرون أن تدفّق الدم قد استُعيد بالكامل. ومع ذلك، في ما يصل إلى نصف المرضى تظل أصغر الأوعية الدموية في القلب مغلقة، فتستمر أجزاء من عضلة القلب محرومة من الدم. تُعرف هذه المشكلة الخفية باسم «انعدام الإعادة للتدفق» (no‑reflow)، وهي تزيد بشكل كبير من خطر فشل القلب والوفاة. تكشف الدراسة الملخّصة هنا عن مسار إشاري بين الدماغ والأمعاء والقلب يمكنه فتح هذه الأوعية الصغيرة من الداخل ويقترح طرقًا جديدة لحماية القلب باستخدام أدوية معروفة بالفعل لعلاج السكري.
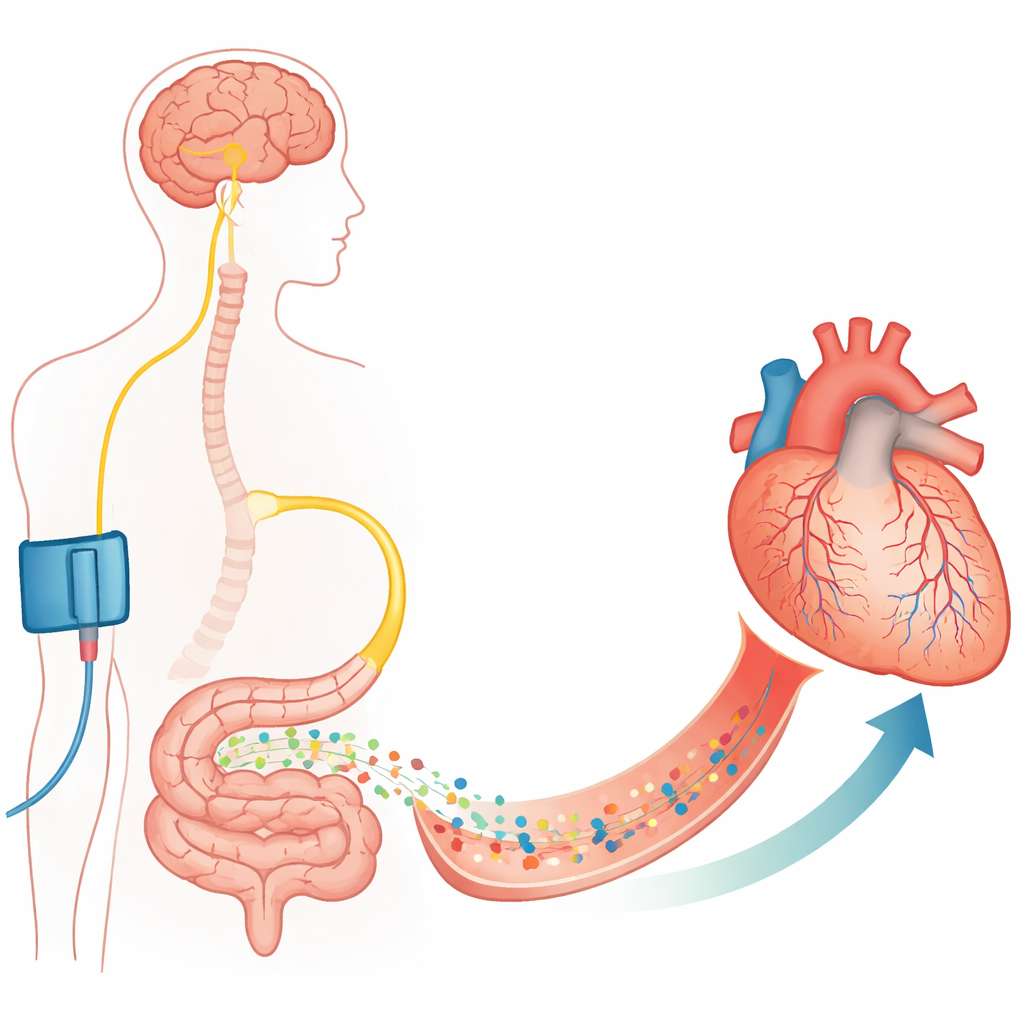
من الشرايين الكبيرة إلى خلايا البوابة الصغيرة
فتح شريان تاجي مسدود بواسطة دعامات (stent) ينقذ الحياة لكنه ليس كافيًا دائمًا. يركّز المؤلفون على الشعيرات الدموية، الأوعية الرقيقة للغاية التي توصل الأكسجين فعليًا إلى نسيج القلب. تحيط بهذه الشعيرات خلايا داعمة تُسمى الخلايا الشِعرية (pericytes)، التي تستطيع انقباض أو استرخاء جدار الوعاء. أظهرت أعمال سابقة أنه خلال وبعد فترة انقطاع الدم، تنقبض هذه الخلايا الشِعرية وأحيانًا تموت وهي في حالة انقباض، مما يضيّق الشعيرات الدموية بشكل دائم ويسبب انعدام الإعادة للتدفق. تؤكد هذه الدراسة في قلوب الفئران والجرذان أنه بعد انسداد محكوم وإعادة فتح شريان تاجي، تظل العديد من الشعيرات الدموية مقيدة عند مواقع الخلايا الشِعرية وجزء كبير لم يعد يحمل دمًا، على الرغم من أن الشريان الرئيسي يظل سالكًا.
هرمون من الأمعاء يتواصل مع شعيرات القلب
سأل الباحثون بعد ذلك ما إن كان لدى الجسم طريقة مدمجة لإرخاء هذه الخلايا الشِعرية. فحصوا ظاهرة تُسمى التكييف الإسخيمي البعيد (remote ischaemic preconditioning)، حيث إن قطع تدفق الدم مؤقتًا عن طرف (مثل وضع كفة على الساق) يحمي القلب لاحقًا من انسداد. أشارت أعمال سابقة إلى العصب المبهم (vagus) وهرمون الأمعاء GLP‑1 كرسل رئيسية. باستخدام مسبارات فلورية وأجسام مضادة، أظهر الفريق أن مستقبلات GLP‑1 موجودة على الخلايا الشِعرية التاجية في الفئران وفي خلايا شِعرية قلبية بشرية مزروعة. في جرذان حية، أدى جعل الأطراف الخلفية إسخيمية لفترة قصيرة قبل انسداد تاجي إلى تقليل حاد في انسدادات الشعيرات واستعادة حجم الدم المروى في منطقة القلب المهددة — لكن فقط إذا كانت مستقبلات GLP‑1 نشطة. إعاقة هذه المستقبلات أزالت الفائدة وأعادت ظهور انعدام الإعادة للتدفق.
كيف يجعل GLP-1 الشعيرات تتسع مرة أخرى
لتفكيك الآلية، استخدم المؤلفون قطعة معزولة من قلب فأر مُضغوطة حيث تمكنوا من مراقبة شعيرة مفردة وخلايا شِعرية تحت المجهر. عندما أزالوا الأكسجين والجلوكوز من السائل المحيط بالنسيج، انقبضت الخلايا الشِعرية وانكمشت أقطار الشعيرات الدموية. إضافة دواء مشابه لـ GLP‑1 (Exendin‑4) أثناء استمرار الظروف منخفضة الأكسجين تسبّب في استرخاء الخلايا الشِعرية وإعادة توسع الشعيرات إلى عرضها الأصلي تقريبًا. اختفى هذا التأثير إذا حَجَبوا نوعًا محددًا من قنوات الأيون المعروفة بقنوات البوتاسيوم الحساسة للأدينوسين ثلاثي الفوسفات (KATP) أو أزالوا وراثيًا مُكوِّنًا رئيسيًا من KATP في الخلايا الشِعرية فقط. وبالمثل، مَنَفِذ مباشر لقنوات KATP استطاع عكس الانقباض المستحث بالعقاقير في الفئران العادية لكنه لم يعمل في الحيوانات التي حُذِفت فيها قنوات KATP من الخلايا الشِعرية. كما فقدت الفئران الخالية من قنوات KATP في الخلايا الشِعرية الفائدة الواقية للتكييف الإسخيمي البعيد في تجارب الجسم الكامل، ما يربط هذه القنوات بقوة بالطريق الوقائي.
ضبط المسار بدقة عبر طاقة الخلية والإشارات
يتعمق التقرير في كيفية التحكم بهذه القنوات. أظهر الفريق أن إنزيمًا يحس بحالة طاقة الخلية، وهو بروتين كيناز المنشط بـ AMP (AMPK)، حاسم. منع AMPK حال دون قدرة GLP‑1 على إعادة فتح الشعيرات المقيدة وحوّل قنوات KATP بعيدًا عن سطح الخلية، ما يوحي بأن AMPK يساعد في نقل هذه القنوات إلى موقعها على غشاء الخلية الشِعرية حيث يمكنها العمل. ووجدوا أيضًا أن حجب إنتاج أكسيد النيتريك أو مستقبلات الموسكارينيك (الأسيتيل كولين) لم يزيد الانقباض بحد ذاته، لكنه حجب بالتحديد التوسع الذي يستدعيه GLP‑1. يتوافق هذا مع نموذج يتمثل في أن أكسيد النيتريك والأسيتيل كولين يعملان في المراحل الأعلى بتحفيز AMPK، والذي بدوره يعزز نقل قنوات KATP ويسمح لـ GLP‑1 بإحداث استقطاب مفرط واسترخاء الخلايا الشِعرية.
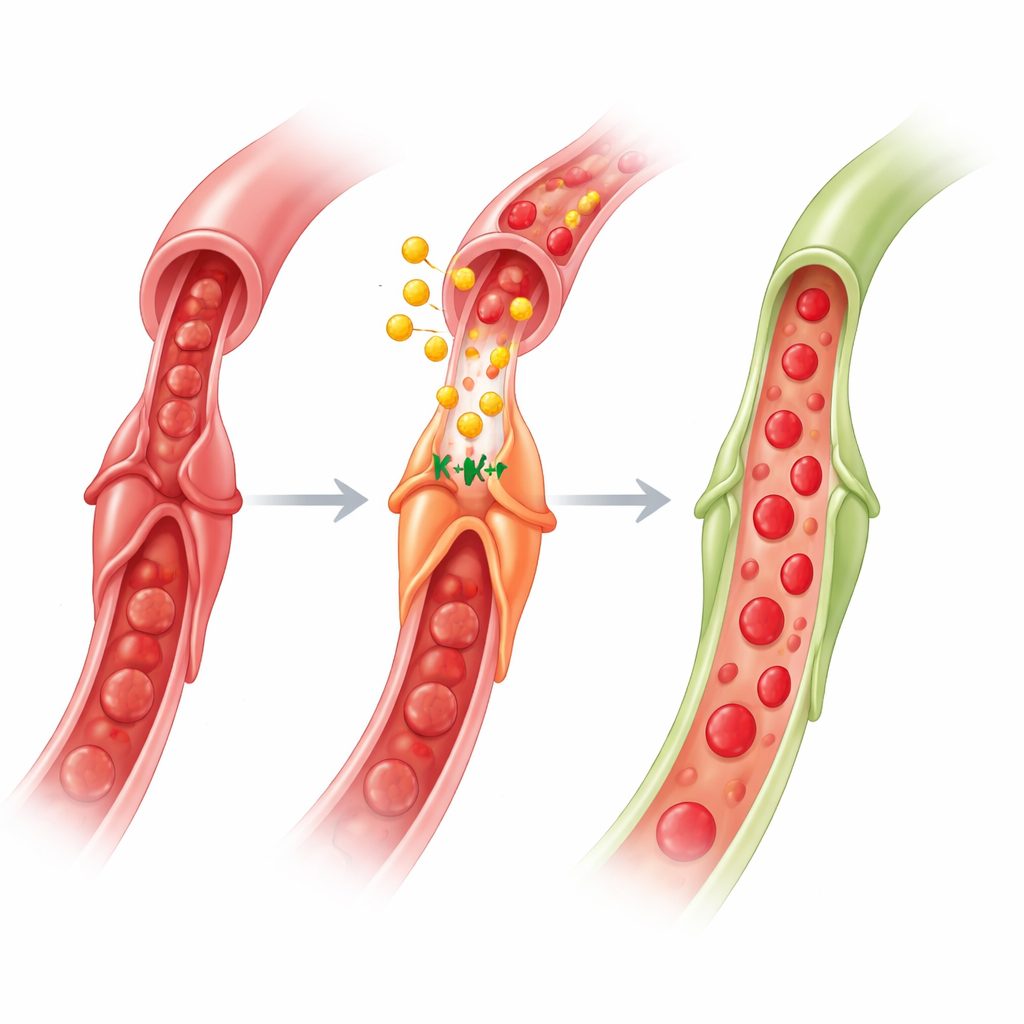
ما الذي يعنيه هذا لعلاجات القلب المستقبلية
تُظهر النتائج معًا دائرة دماغ‑أمعاء‑قلب: إشارة إسخيمية قصيرة في طرف تنشط الأعصاب المتجهة إلى الأمعاء، وخلايا الأمعاء تطلق GLP‑1 إلى مجرى الدم، وGLP‑1 ينتقل إلى القلب ليعمل على الخلايا الشِعرية. من خلال تفعيل قنوات KATP — بمساعدة AMPK، وأكسيد النيتريك والأسيتيل كولين — يجعل GLP‑1 الخلايا الشِعرية تتخلى عن احتجازها للشعيرات، مستعيدًا التدفق في الدورة الدقيقة بعد إعادة فتح الشريان. للقراء غير المتخصصين، الرسالة الأساسية هي أن حماية القلب لا تقتصر على فتح الشرايين الكبيرة فقط؛ بل تتعلق أيضًا بإقناع خلايا البوابة الصغيرة بالانفتاح. وبما أن أدوية معتمدة على GLP‑1 مستخدمة بالفعل على نطاق واسع لعلاج السكري والسمنة وأظهرت فوائد قلبية، فإن تحسينها لاستهداف وظيفة الخلايا الشِعرية أثناء وبعد النوبات القلبية قد يوفر طريقة جديدة لتقليل انعدام الإعادة للتدفق وتحسين التعافي.
الاستشهاد: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
الكلمات المفتاحية: نوبة قلبية, الدورة الدقيقة, GLP-1, الخلايا الشِعرية (Pericytes), حماية القلب