Clear Sky Science · pt
GLP-1 ativa canais KATP em pericitos coronarianos como efetor da sinalização cérebro‑intestino‑coração que media cardioproteção
Por que proteger os pequenos vasos cardíacos é importante
Quando uma artéria cardíaca obstruída é reaberta após um infarto, muitos presumem que o fluxo sanguíneo é totalmente restaurado. No entanto, em até metade dos pacientes, os menores vasos sanguíneos do coração permanecem fechados, de modo que partes do músculo cardíaco continuam sem suprimento sanguíneo. Esse problema oculto, chamado “no‑reflow” (ausência de reperfusão), aumenta muito o risco de insuficiência cardíaca e de morte. O estudo resumido aqui revela uma via de sinalização cérebro–intestino–coração que pode abrir esses pequenos vasos de dentro para fora e sugere novas formas de proteger o coração usando fármacos já conhecidos do tratamento do diabetes.
Das grandes artérias às pequenas células guardiãs
Desobstruir uma artéria coronária com um stent salva vidas, mas nem sempre é suficiente. Os autores focam nos capilares, os vasos finíssimos que de fato entregam oxigênio ao músculo cardíaco. Envolvendo esses capilares estão células de sustentação chamadas pericitos, que podem contrair ou relaxar a parede do vaso. Trabalhos anteriores mostraram que durante e após um período sem sangue, esses pericitos se contraem e às vezes morrem em estado contraído, estreitando permanentemente os capilares e causando no‑reflow. Este estudo confirma, em corações de ratos e camundongos, que após uma obstrução controlada e a reabertura de uma artéria coronária, muitos capilares permanecem constritos nos locais dos pericitos e uma grande fração deixa de conduzir sangue, mesmo com a artéria principal pérvia.
Um hormônio do intestino que conversa com os capilares do coração
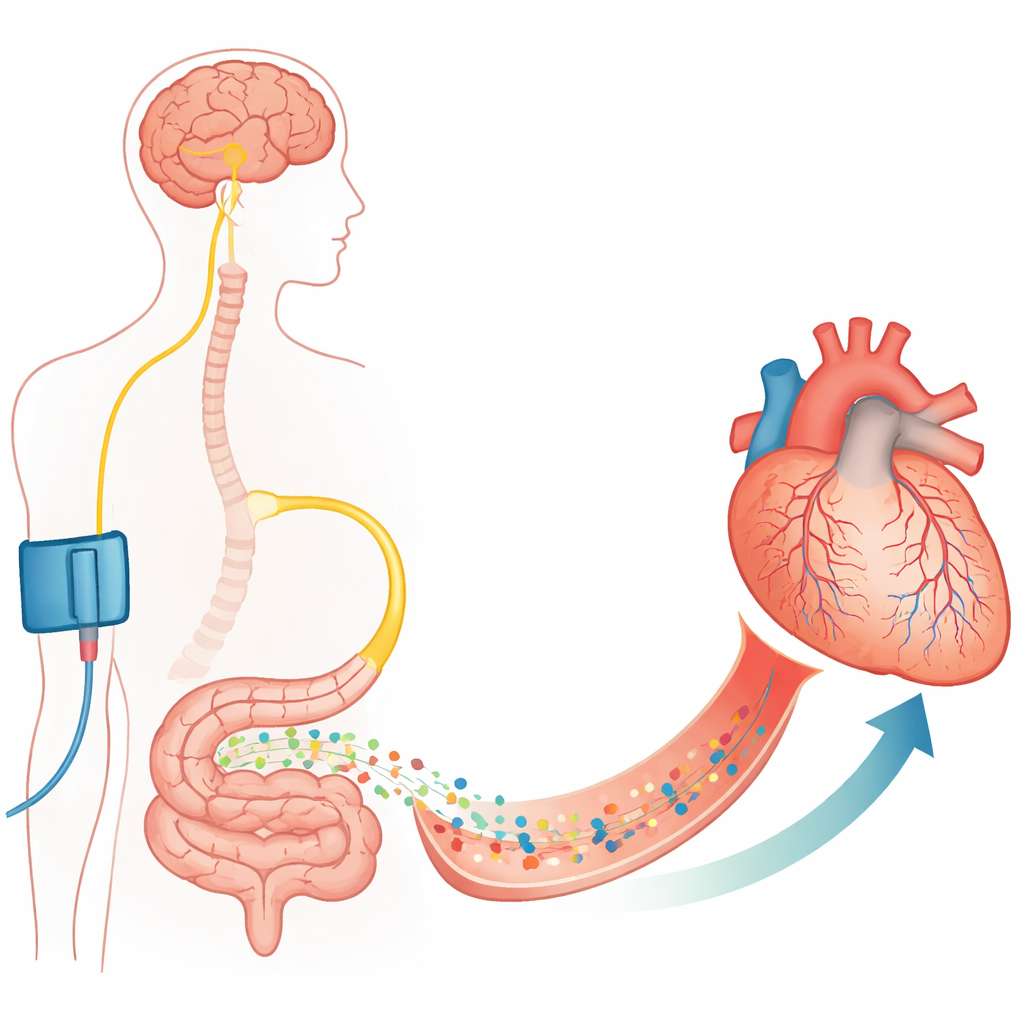
Os pesquisadores então perguntaram se o corpo tem um mecanismo próprio para relaxar esses pericitos. Eles examinaram um fenômeno chamado pré‑condicionamento isquêmico remoto, em que a breve interrupção do fluxo sanguíneo em um membro (por exemplo com uma braçadeira) de alguma forma protege o coração de uma obstrução posterior. Trabalhos anteriores indicaram o nervo vago e o hormônio intestinal GLP‑1 como mensageiros chave. Usando sondas fluorescentes e anticorpos, a equipe demonstrou que receptores de GLP‑1 estão presentes em pericitos coronarianos de camundongos e em pericitos cardíacos humanos cultivados. Em ratos vivos, provocar brevemente isquemia nos membros posteriores antes de uma obstrução coronária reduziu fortemente os bloqueios capilares e restaurou o volume de sangue perfundido na região cardíaca em risco — mas somente se os receptores de GLP‑1 estavam ativos. Bloquear esses receptores eliminou o benefício e trouxe de volta o no‑reflow.
Como o GLP‑1 faz os capilares se alargarem novamente
Para dissecar o mecanismo, os autores usaram um pedaço isolado e pressurizado de coração de camundongo onde puderam observar capilares e pericitos individuais ao microscópio. Quando removeram oxigênio e glicose do fluido que banhava o tecido, os pericitos se contraíram e os diâmetros capilares diminuíram. Adicionar um fármaco semelhante ao GLP‑1 (Exendina‑4) enquanto as condições de baixo oxigênio persistiam fez com que os pericitos relaxassem e os capilares se reexpandissem quase até a largura original. Esse efeito desapareceu se bloquearam um tipo específico de canal iônico conhecido como canal potássio sensível ao ATP (KATP) ou removeram geneticamente um componente crucial do KATP apenas nos pericitos. De modo semelhante, um abridor direto de canais KATP pôde reverter a constrição induzida por drogas em camundongos normais, mas não em animais com KATP ausente nos pericitos. Camundongos sem canais KATP nos pericitos também perderam o benefício protetor do pré‑condicionamento remoto em experimentos com animais inteiros, ligando firmemente esses canais à via protetora.
Ajustando a via com energia celular e sinalização
A história aprofunda‑se em como esses canais são controlados. A equipe mostrou que uma enzima que detecta o estado energético celular, a quinase ativada por AMP (AMPK), é crucial. Bloquear a AMPK impediu o GLP‑1 de reabrir os capilares constritos e deslocou os canais KATP para longe da superfície celular, sugerindo que a AMPK ajuda a posicionar esses canais na membrana dos pericitos onde podem funcionar. Também descobriram que bloquear a produção de óxido nítrico ou receptores muscarínicos (acetilcolina) não agravou a constrição por si só, mas bloqueou especificamente a dilatação desencadeada pelo GLP‑1. Isso se encaixa num modelo em que óxido nítrico e acetilcolina atuam a montante ao estimular a AMPK, que por sua vez promove o tráfego dos canais KATP e permite que o GLP‑1 hiperpolarize e relaxe os pericitos.
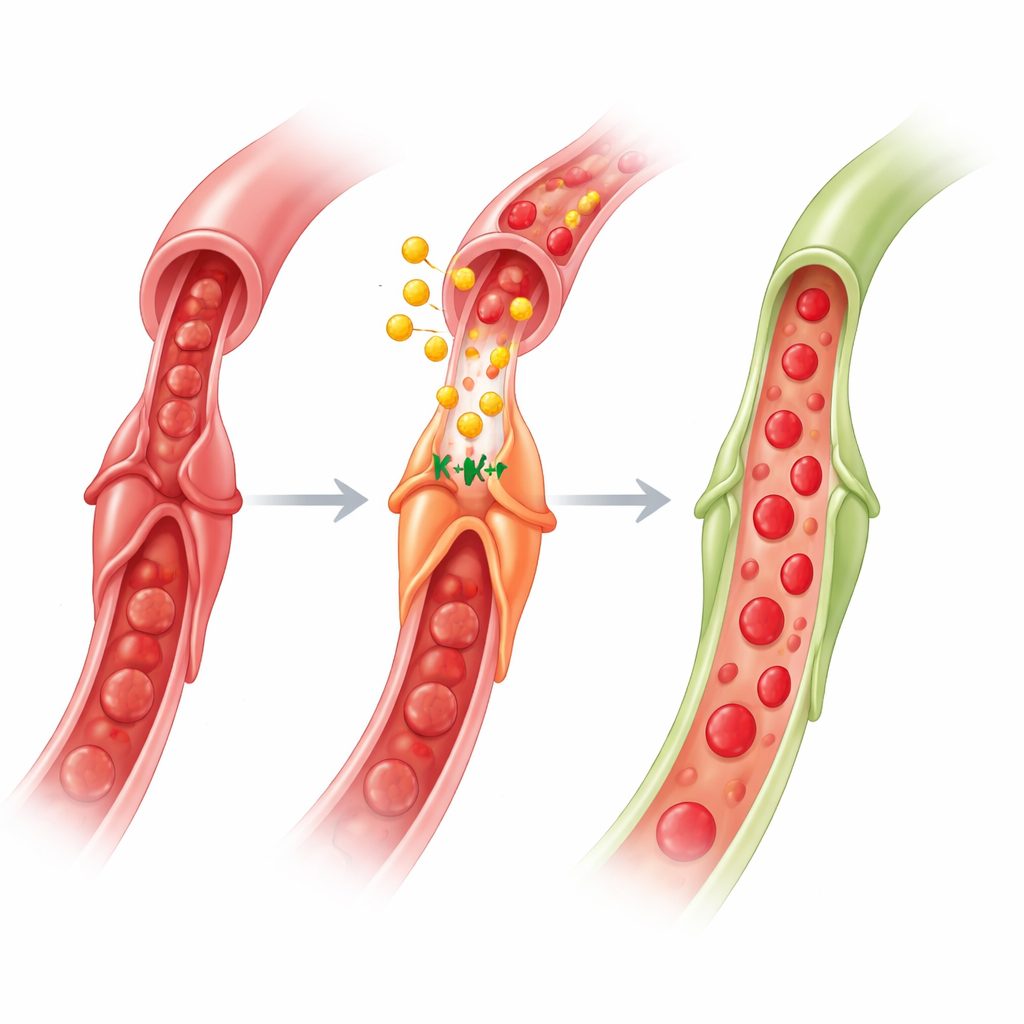
O que isso significa para tratamentos cardíacos futuros
Em conjunto, o trabalho revela um circuito cérebro–intestino–coração: um sinal isquêmico breve em um membro ativa nervos para o intestino, células intestinais liberam GLP‑1 na corrente sanguínea, e o GLP‑1 viaja ao coração para agir nos pericitos. Ao engajar canais KATP — com auxílio da AMPK, do óxido nítrico e da acetilcolina — o GLP‑1 faz com que os pericitos soltem os capilares, restaurando o fluxo na microcirculação após a reabertura de uma artéria. Para não especialistas, a mensagem principal é que proteger o coração não se resume apenas a desobstruir artérias grandes; trata‑se também de persuadir pequenas células guardiãs a se abrirem. Como os fármacos à base de GLP‑1 já são amplamente usados para diabetes e obesidade e mostraram benefícios cardiovasculares, refiná‑los para direcionar a função dos pericitos durante e após infartos pode oferecer uma nova maneira de reduzir o no‑reflow e melhorar a recuperação.
Citação: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Palavras-chave: infarto, microcirculação, GLP-1, pericitos, cardioproteção