Clear Sky Science · fr
Le GLP-1 active les canaux KATP des péricytes coronaires en tant qu’effecteur du signal cerveau‑intestin‑cœur médiant la cardioprotection
Pourquoi protéger les minuscules vaisseaux du cœur est important
Lorsque l’on rouvre une artère coronaire bouchée après un infarctus, beaucoup supposent que le flux sanguin est entièrement rétabli. Pourtant, chez jusqu’à la moitié des patients, les plus petits vaisseaux du cœur restent fermés, si bien que des zones du muscle cardiaque demeurent privées de sang. Ce problème caché, appelé « no‑reflow », augmente fortement le risque d’insuffisance cardiaque et de décès. L’étude résumée ici dévoile une voie de signalisation cerveau–intestin–cœur capable d’ouvrir ces minuscules vaisseaux de l’intérieur et suggère de nouvelles façons de protéger le cœur en utilisant des médicaments déjà connus dans le traitement du diabète.
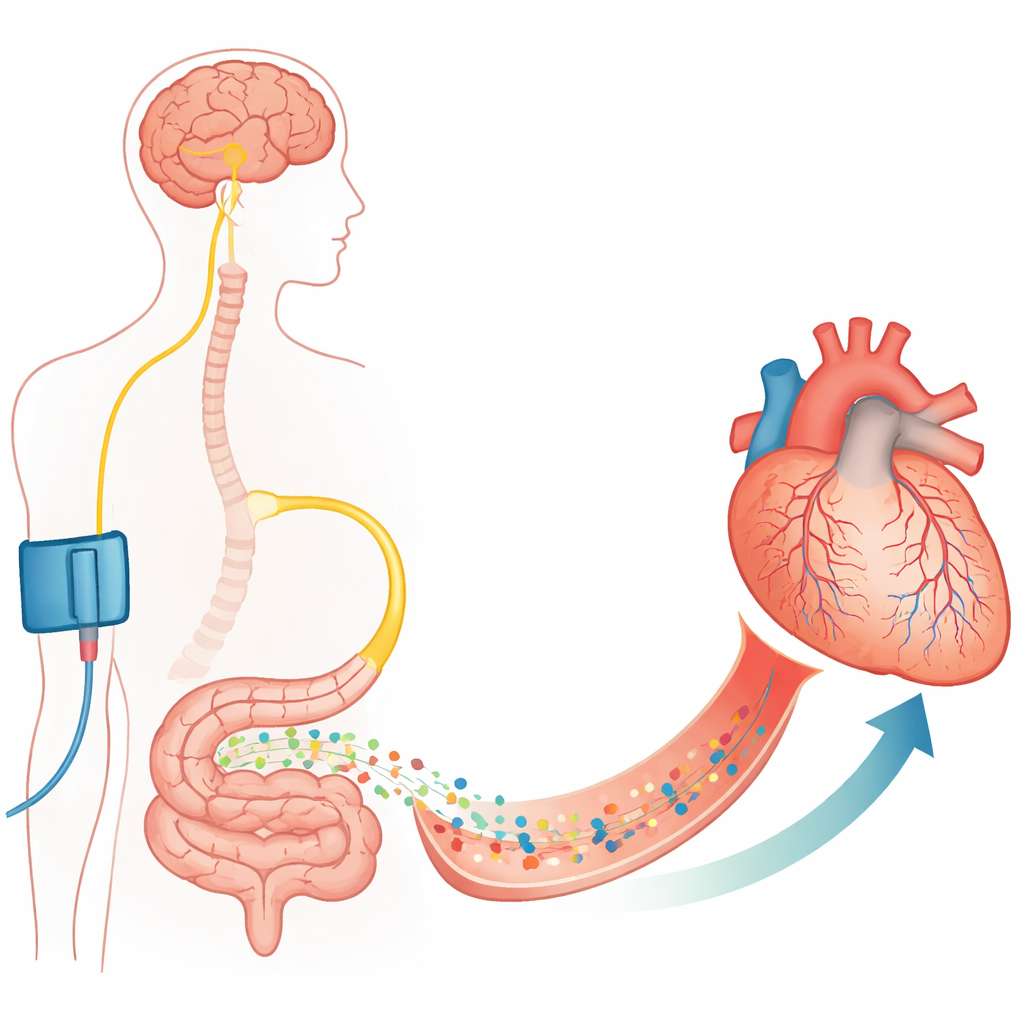
Des grosses artères aux petites cellules gardiennes
Ouvrir une artère coronaire obstruée avec une endoprothèse sauve des vies mais n’est pas toujours suffisant. Les auteurs se concentrent sur les capillaires, ces vaisseaux d’une finesse extrême qui apportent réellement l’oxygène au muscle cardiaque. Enroulées autour de ces capillaires, des cellules de soutien appelées péricytes peuvent comprimer ou relâcher la paroi vasculaire. Des travaux antérieurs ont montré que pendant et après une période sans apport sanguin, ces péricytes se contractent et parfois meurent dans un état contracté, rétrécissant de façon permanente les capillaires et provoquant le no‑reflow. Cette étude confirme, dans des cœurs de rat et de souris, que suite à une occlusion contrôlée puis la réouverture d’une artère coronaire, de nombreux capillaires restent contractés au niveau des péricytes et qu’une grande fraction ne transporte plus de sang, même si l’artère principale est perméable.
Une hormone intestinale qui communique avec les capillaires cardiaques
Les chercheurs ont ensuite cherché à savoir si l’organisme dispose d’un mécanisme interne pour relaxer ces péricytes. Ils ont examiné un phénomène appelé préconditionnement ischémique à distance, où l’ischémie brève d’un membre (par exemple par un brassard) protège d’une manière ou d’une autre le cœur contre une obstruction ultérieure. Des travaux antérieurs pointaient le nerf vague et l’hormone intestinale GLP‑1 comme messagers clés. À l’aide de sondes fluorescentes et d’anticorps, l’équipe a montré que les récepteurs du GLP‑1 sont présents sur les péricytes coronaires chez la souris et sur des péricytes humains cardiaques en culture. Chez le rat in vivo, provoquer brièvement une ischémie des membres inférieurs avant une occlusion coronaire a fortement réduit les obstructions capillaires et restauré le volume sanguin perfusé dans la région cardiaque menacée — mais seulement si les récepteurs du GLP‑1 étaient actifs. Le blocage de ces récepteurs a annulé le bénéfice et a rétabli le no‑reflow.
Comment le GLP-1 fait à nouveau s’élargir les capillaires
Pour disséquer le mécanisme, les auteurs ont utilisé un fragment de cœur de souris isolé et sous pression permettant d’observer au microscope des capillaires et des péricytes uniques. Lorsqu’ils ont retiré l’oxygène et le glucose du liquide baignant le tissu, les péricytes se sont contractés et les diamètres capillaires ont diminué. L’ajout d’un médicament mimant le GLP‑1 (Exendin‑4) alors que les conditions d’hypoxie persistaient a provoqué la relaxation des péricytes et la réexpansion des capillaires presque jusqu’à leur largeur initiale. Cet effet disparaissait si l’on bloquait un type spécifique de canal ionique connu sous le nom de canal potassique sensible à l’ATP (KATP) ou si l’on supprimait génétiquement un composant clé du KATP uniquement dans les péricytes. De même, un ouvreur direct des canaux KATP pouvait inverser la constriction induite par la drogue chez des souris normales mais pas chez les souris déficientes en KATP au niveau des péricytes. Les souris sans canaux KATP des péricytes ont également perdu le bénéfice cardioprotecteur du préconditionnement à distance dans des expériences sur animaux entiers, liant fermement ces canaux à la voie protectrice.
Ajuster finement la voie via l’énergie cellulaire et la signalisation
L’histoire entre dans le détail du contrôle de ces canaux. L’équipe a montré qu’une enzyme détectant le statut énergétique cellulaire, la protéine kinase activée par l’AMP (AMPK), est cruciale. Le blocage de l’AMPK empêchait le GLP‑1 de rouvrir les capillaires contractés et déplaçait les canaux KATP hors de la surface cellulaire, suggérant que l’AMPK favorise le trajet de ces canaux jusqu’à la membrane des péricytes où ils peuvent fonctionner. Ils ont aussi constaté que le blocage de la production d’oxyde nitrique ou des récepteurs muscariniques (acétylcholine) n’aggravait pas la constriction en soi, mais bloquait spécifiquement la dilatation déclenchée par le GLP‑1. Cela correspond à un modèle où l’oxyde nitrique et l’acétylcholine agissent en amont en stimulant l’AMPK, qui à son tour favorise le trafic des canaux KATP et permet au GLP‑1 d’hyperpolariser et de relaxer les péricytes.
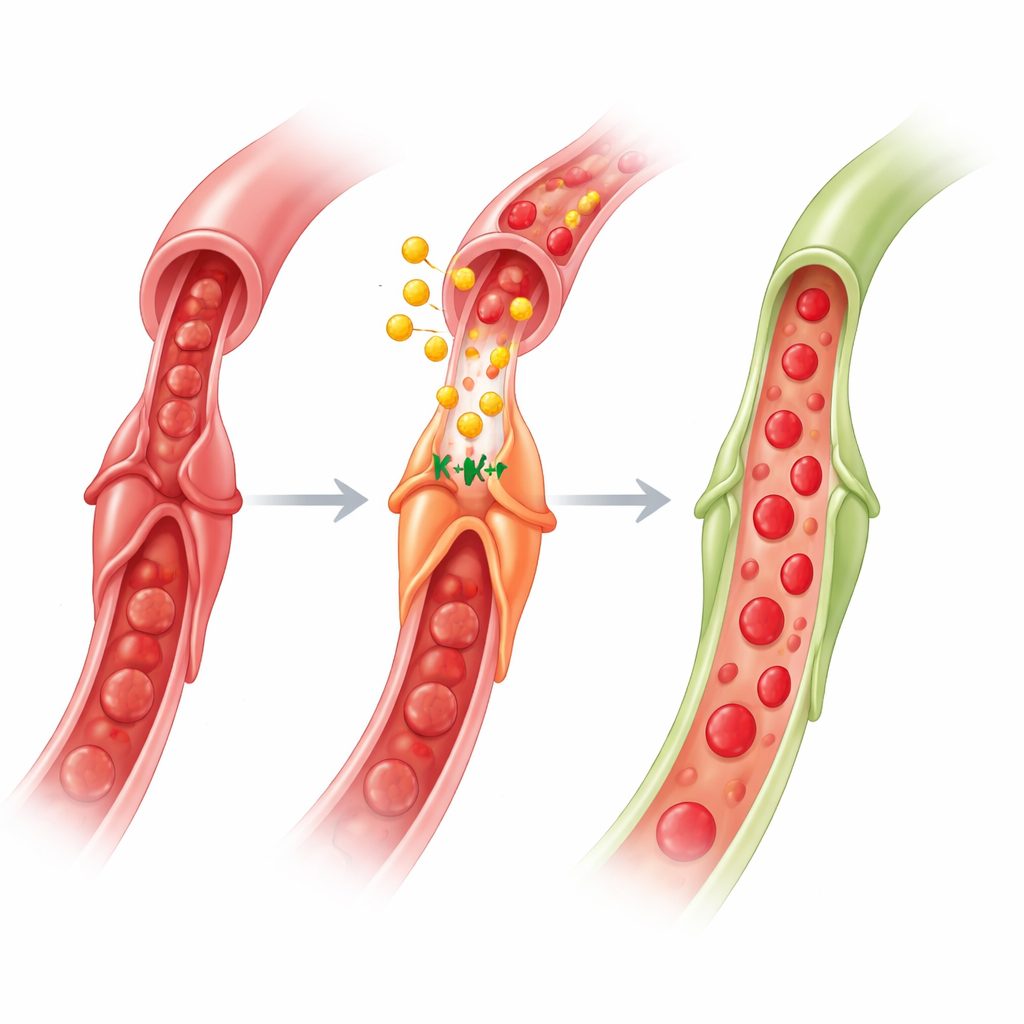
Ce que cela signifie pour les traitements cardiaques futurs
Dans l’ensemble, ce travail révèle un circuit cerveau–intestin–cœur : un signal ischémique bref dans un membre active des nerfs vers l’intestin, les cellules intestinales libèrent du GLP‑1 dans la circulation sanguine, et le GLP‑1 se rend au cœur pour agir sur les péricytes. En mobilisant les canaux KATP — avec l’aide de l’AMPK, de l’oxyde nitrique et de l’acétylcholine — le GLP‑1 amène les péricytes à lâcher prise sur les capillaires, restaurant le flux dans la microcirculation après la réouverture d’une artère. Pour le grand public, le message clé est que protéger le cœur ne consiste pas seulement à déboucher les grosses artères ; il s’agit aussi de convaincre de minuscules cellules gardiennes d’ouvrir. Comme les médicaments à base de GLP‑1 sont déjà largement utilisés pour le diabète et l’obésité et ont montré des bénéfices cardiovasculaires, les affiner pour cibler la fonction des péricytes pendant et après les infarctus pourrait offrir une nouvelle voie pour réduire le no‑reflow et améliorer la récupération.
Citation: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Mots-clés: infarctus, microcirculation, GLP-1, péricytes, cardioprotection