Clear Sky Science · de
GLP-1 aktiviert KATP-Kanäle in koronaren Perizyten als Effektor der Gehirn‑Darm‑Herz‑Signalgebung, die Kardioprotektion vermittelt
Warum der Schutz winziger Herzgefäße wichtig ist
Wenn eine verstopfte Herzarterie nach einem Herzinfarkt wiedereröffnet wird, gehen viele Menschen davon aus, dass der Blutfluss vollständig wiederhergestellt ist. Dennoch bleiben bei bis zu der Hälfte der Patientinnen und Patienten die kleinsten Gefäße im Herzen geschlossen, sodass Teile des Herzmuskels weiterhin unterversorgt sind. Dieses verborgene Problem, „No‑Reflow“ genannt, erhöht das Risiko für Herzinsuffizienz und Tod deutlich. Die hier zusammengefasste Studie entdeckt eine Gehirn–Darm–Herz‑Signalbahn, die diese winzigen Gefäße von innen her öffnen kann, und weist auf neue Möglichkeiten hin, das Herz mit bereits aus der Diabetesbehandlung bekannten Medikamenten zu schützen.
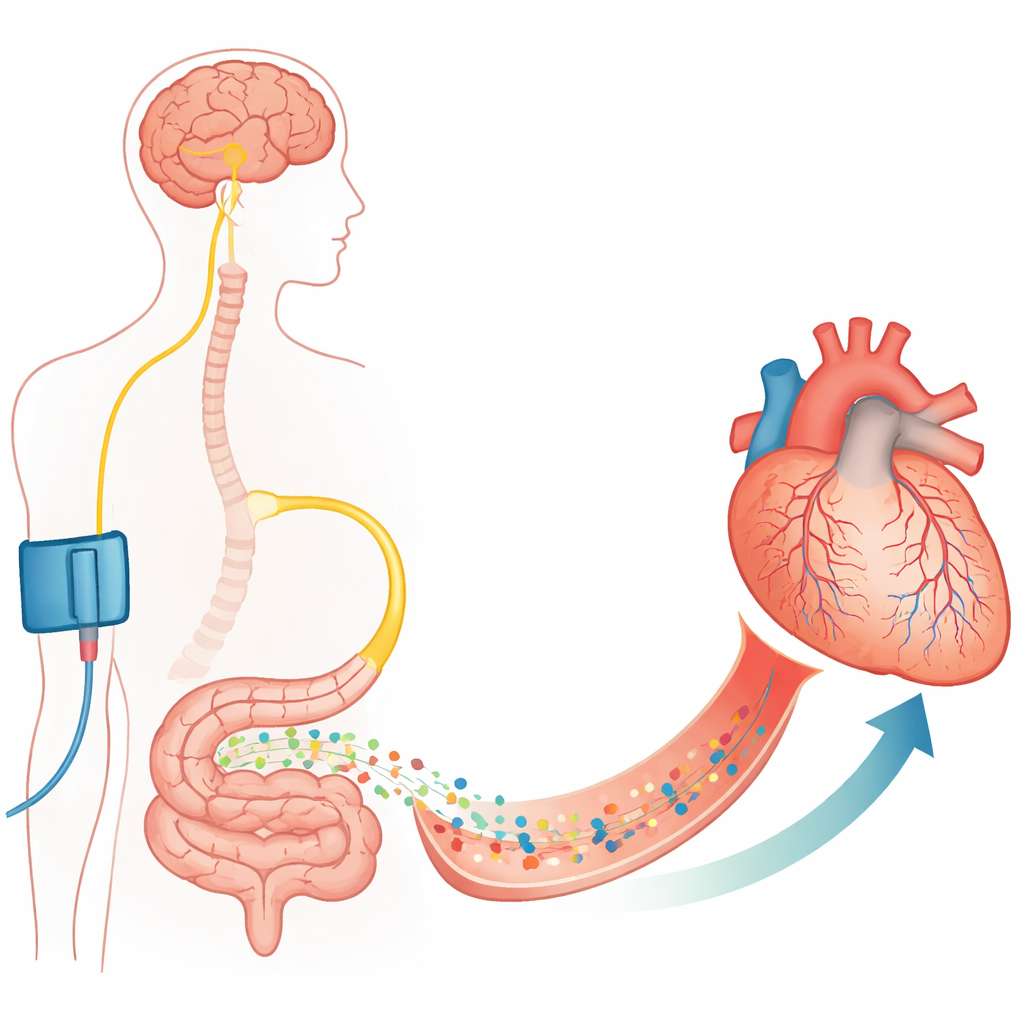
Von großen Arterien zu winzigen Torwächterzellen
Das Offenlegen einer verstopften Koronararterie mit einem Stent kann lebensrettend sein, reicht aber nicht immer aus. Die Autorinnen und Autoren konzentrieren sich auf Kapillaren, die haarfeinen Gefäße, die tatsächlich Sauerstoff an den Herzmuskel liefern. Um diese Kapillaren herum liegen Stützzellen, sogenannte Perizyten, die die Gefäßwand zusammenziehen oder entspannen können. Frühere Arbeiten zeigten, dass Perizyten während und nach einer Durchblutungsunterbrechung verengen und manchmal in einem kontrahierten Zustand sterben, wodurch Kapillaren dauerhaft verengt werden und No‑Reflow entsteht. Diese Studie bestätigt in Ratten‑ und Mausherzen, dass nach einer kontrollierten Blockade und Wiedereröffnung einer Koronararterie viele Kapillaren an Perizytenstellen weiterhin verkleinert sind und ein großer Anteil kein Blut mehr führt, obwohl die Hauptarterie durchgängig ist.
Ein Hormon aus dem Darm, das mit Herzkapillaren kommuniziert
Die Forschenden fragten dann, ob der Körper einen eingebauten Mechanismus hat, um diese Perizyten zu entspannen. Sie untersuchten ein Phänomen namens remote ischemic preconditioning, bei dem das kurzzeitige Abschneiden der Blutversorgung eines Gliedmaßes (zum Beispiel mit einer Manschette) das Herz vor einem späteren Verschluss schützt. Frühere Arbeiten deuteten auf den Vagusnerv und das Darmhormon GLP‑1 als entscheidende Botenstoffe hin. Mit fluoreszierenden Sonden und Antikörpern zeigte das Team, dass GLP‑1‑Rezeptoren an koronaren Perizyten in Mäusen und in kultivierten menschlichen Herzperizyten vorhanden sind. In lebenden Ratten reduzierte eine kurzzeitige Ischämie der Hinterbeine vor einer Koronarblockade deutlich Kapillarblockaden und stellte das durchströmte Blutvolumen in der gefährdeten Herzregion wieder her – jedoch nur, wenn GLP‑1‑Rezeptoren aktiv waren. Das Blockieren dieser Rezeptoren beseitigte den Nutzen und ließ No‑Reflow wieder auftreten.
Wie GLP-1 Kapillaren wieder erweitert
Um den Mechanismus zu untersuchen, nutzten die Autorinnen und Autoren ein isoliertes, unter Druck stehendes Stück Mausherz, in dem sie einzelne Kapillaren und Perizyten unter dem Mikroskop beobachten konnten. Wenn sie Sauerstoff und Glukose aus der umgebenden Flüssigkeit entfernten, zogen sich Perizyten zusammen und die Kapillardurchmesser verringerten sich. Die Zugabe eines GLP‑1‑ähnlichen Medikaments (Exendin‑4) während fortgesetzter Hypoxie führte dazu, dass sich die Perizyten entspannten und die Kapillaren fast wieder auf ihre ursprüngliche Breite ausdehnten. Dieser Effekt verschwand, wenn sie einen spezifischen Typ von Ionenkanal, bekannt als ATP‑sensitiver Kaliumkanal (KATP), blockierten oder eine Schlüsselsubkomponente des KATP‑Kanals gezielt nur in Perizyten genetisch entfernten. Ebenso konnte ein direkter KATP‑Öffner die durch Ischämie induzierte Verengung in normalen Mäusen umkehren, nicht aber in Perizyten‑KATP‑Knockouts. Mäuse ohne Perizyten‑KATP‑Kanäle verloren in Ganzkörperexperimenten auch den schützenden Effekt der entfernten Präconditioning, womit diese Kanäle eindeutig mit dem Schutzweg verknüpft sind.
Feinabstimmung des Weges durch zelluläre Energie‑ und Signalmechanismen
Die Arbeit geht näher darauf ein, wie diese Kanäle gesteuert werden. Das Team zeigte, dass ein Enzym, das den zellulären Energiestatus misst, die AMP‑aktivierte Proteinkinase (AMPK), entscheidend ist. Das Blockieren von AMPK verhinderte, dass GLP‑1 verengte Kapillaren wieder öffnete, und verschob KATP‑Kanäle von der Zelloberfläche weg, was darauf hindeutet, dass AMPK dazu beiträgt, diese Kanäle an die Perizytenmembran zu transportieren, wo sie funktionieren können. Sie fanden außerdem, dass das Blockieren der Stickstoffmonoxid‑Produktion oder muskarinischer (Acetylcholin‑)Rezeptoren die Verengung für sich genommen nicht verschlimmerte, aber spezifisch die von GLP‑1 ausgelöste Erweiterung blockierte. Das passt zu einem Modell, in dem Stickstoffmonoxid und Acetylcholin stromaufwärts AMPK stimulieren, das wiederum den KATP‑Kanaltransport fördert und GLP‑1 ermöglicht, Perizyten zu hyperpolarisieren und zu entspannen.
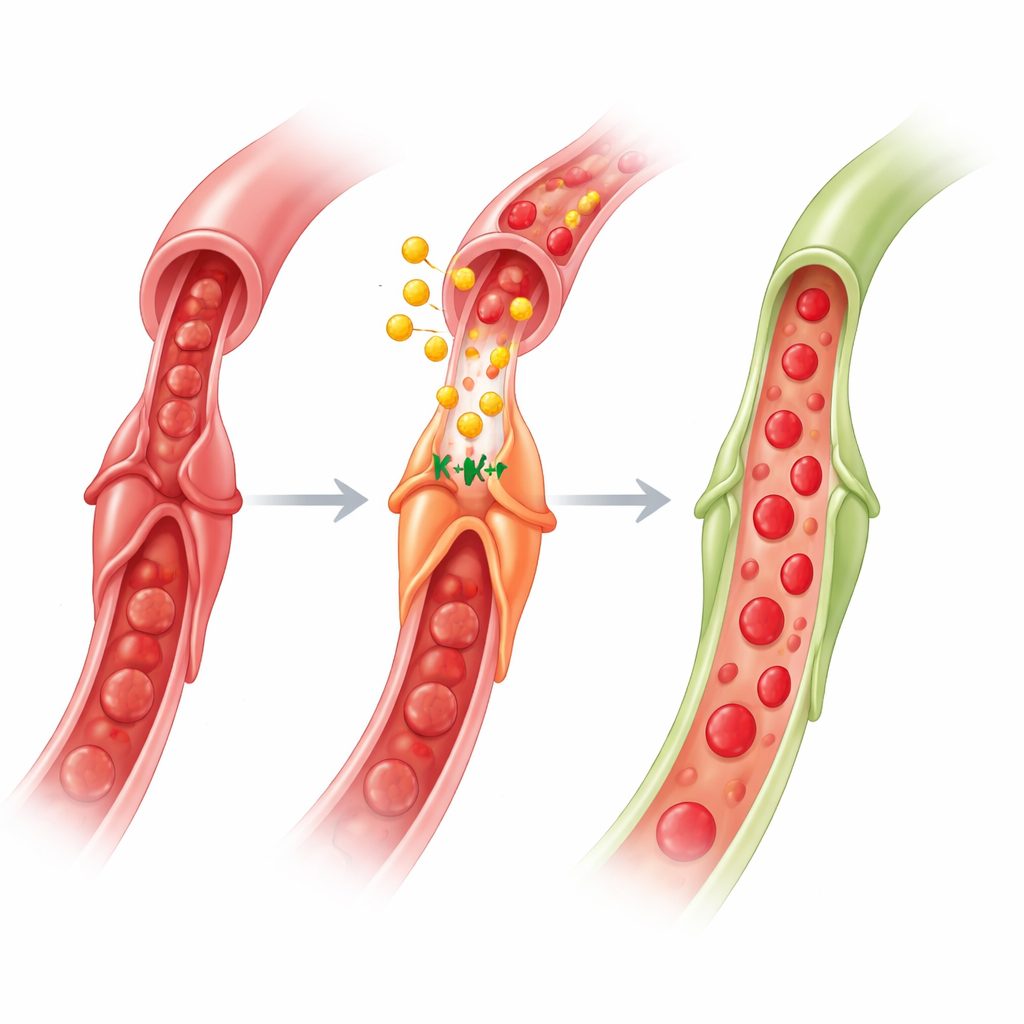
Was das für künftige Herzbehandlungen bedeutet
Insgesamt enthüllt die Arbeit einen Gehirn–Darm–Herz‑Kreislauf: Ein kurzes ischämisches Signal in einem Gliedmaß aktiviert Nerven zum Darm, Darmzellen setzen GLP‑1 ins Blut frei, und GLP‑1 gelangt zum Herzen, um auf Perizyten zu wirken. Indem GLP‑1 KATP‑Kanäle aktiviert – mit Unterstützung von AMPK, Stickstoffmonoxid und Acetylcholin – lässt es Perizyten die Kapillaren los und stellt den Fluss in der Mikrozirkulation nach der Wiedereröffnung einer Arterie wieder her. Für Nicht‑Spezialisten ist die Kernbotschaft, dass Herzschutz nicht nur darin besteht, große Arterien freizumachen; es geht auch darum, winzige Torwächterzellen zum Öffnen zu bewegen. Da GLP‑1‑basierte Medikamente bereits weit verbreitet zur Behandlung von Diabetes und Adipositas eingesetzt werden und kardiovaskuläre Vorteile gezeigt haben, könnte deren Feinabstimmung zur gezielten Beeinflussung der Perizytenfunktion während und nach Herzinfarkten einen neuen Ansatz bieten, No‑Reflow zu verringern und die Erholung zu verbessern.
Zitation: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Schlüsselwörter: Herzinfarkt, Mikrozirkulation, GLP-1, Perizyten, Kardioprotektion