Clear Sky Science · ru
GLP-1 активирует KATP-каналы в коронарных перицитах как эффектор сигнальной цепи мозг‑кишечник‑сердце, обеспечивающей кардиопротекцию
Почему важно защищать крошечные сосуды сердца
Когда заблокированную коронарную артерию восстанавливают после инфаркта, многие полагают, что кровоток полностью восстановлен. Однако у почти половины пациентов самые мелкие сосуды сердца остаются сжатыми, и участки сердечной мышцы продолжают испытывать недостаток крови. Эта скрытая проблема, называемая «no‑reflow» (отсутствие реперфузии), значительно повышает риск сердечной недостаточности и смерти. Вкратце изложенное здесь исследование выявляет сигнальную цепочку мозг–кишечник–сердце, которая способна изнутри раскрывать эти крошечные сосуды, и указывает на новые подходы к защите сердца с помощью уже известных препаратов, применяемых при диабете.
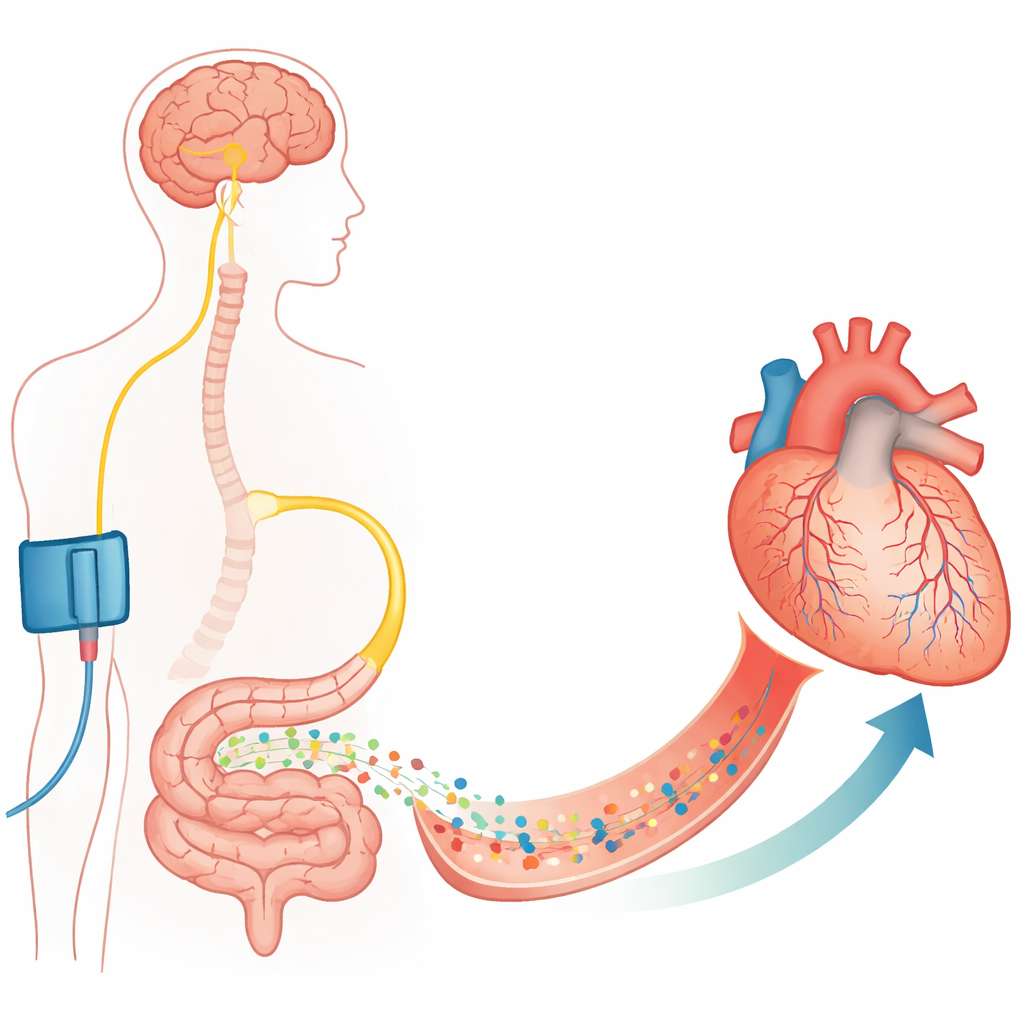
От крупных артерий к крошечным клеткам‑регуляторам
Расширение забитой коронарной артерии с помощью стента спасает жизнь, но не всегда бывает достаточным. Авторы сосредоточились на капиллярах — тончайших сосудах, которые действительно доставляют кислород к сердечной мышце. Вокруг капилляров расположены опорные клетки — перициты, которые могут сжимать или расслаблять стенку сосуда. Ранее показали, что во время и после периода ишемии перициты сокращаются и иногда умирают в сократившемся состоянии, что необратимо сужает капилляры и вызывает no‑reflow. В этом исследовании подтверждено на сердце крыс и мышей, что после контролируемой блокировки и восстановления проходимости коронарной артерии многие капилляры остаются суженными в местах перицитов, и значительная часть их перестаёт пропускать кровь, хотя главная артерия проходима.
Гормон из кишки, который «разговаривает» с капиллярами сердца
Затем исследователи задались вопросом, есть ли у организма встроенный способ расслаблять эти перициты. Они изучали феномен, называемый отдалённой ишемической предподготовкой, когда кратковременное прекращение кровотока в конечности (например, манжетой) как‑то защищает сердце от последующей блокады. Предыдущие работы указывали на блуждающий нерв и кишечный гормон GLP‑1 как ключевых посредников. С помощью флуоресцентных датчиков и антител команда показала, что рецепторы GLP‑1 присутствуют на коронарных перицитах у мышей и на культивируемых человеческих перицитах сердца. В живых крысах кратковременная ишемия задних конечностей перед блокадой коронарной артерии резко уменьшала блокировки капилляров и восстанавливала перфузируемый объём крови в уязвимом участке сердца — но только при активных рецепторах GLP‑1. Блокирование этих рецепторов устраняло эффект и возвращало no‑reflow.
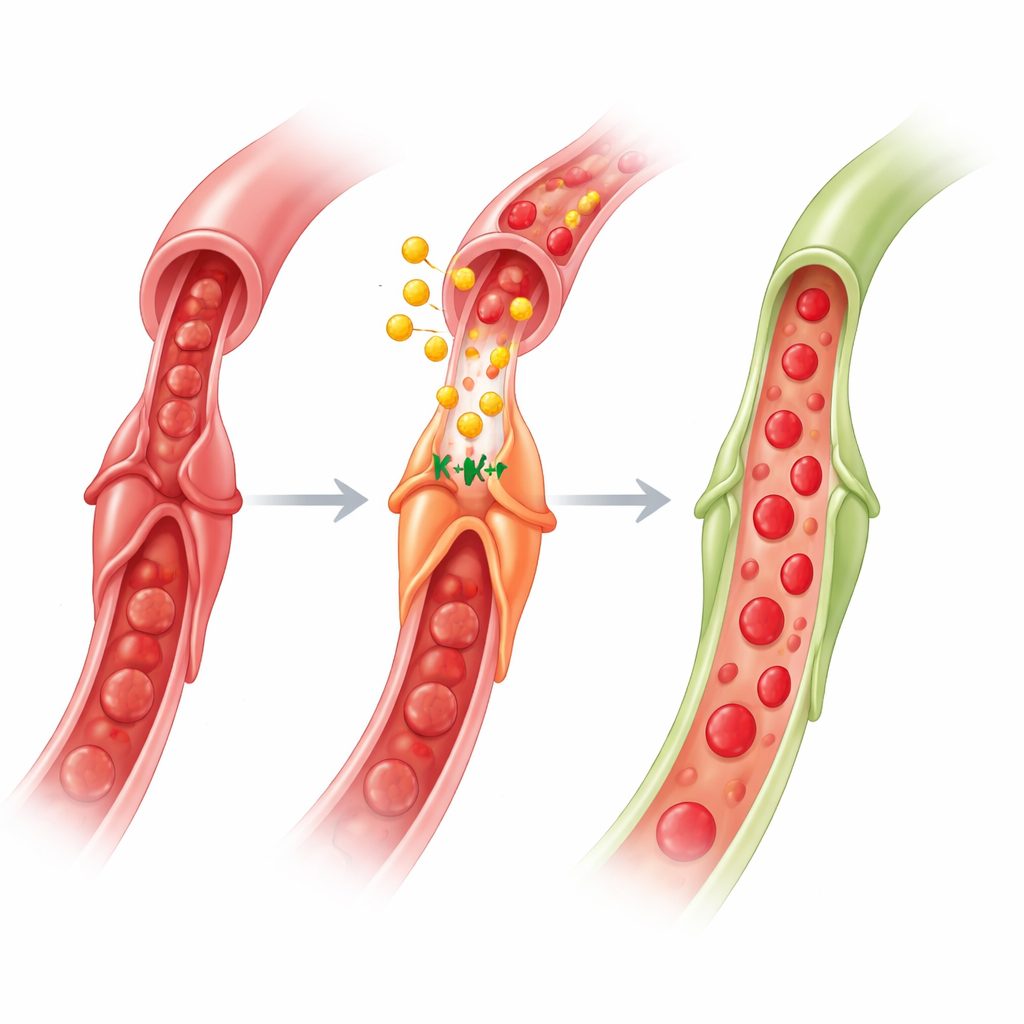
Как GLP‑1 снова расширяет капилляры
Чтобы разобраться в механизме, авторы использовали изолированный, камерно прессионированный кусочек мышиного сердца, где они могли наблюдать отдельные капилляры и перициты под микроскопом. При удалении кислорода и глюкозы из раствора, омывающего ткань, перициты сокращались, и диаметр капилляров уменьшался. Добавление препарата, подобного GLP‑1 (Exendin‑4), в условиях низкого кислорода вызвало расслабление перицитов и почти полное восстановление диаметра капилляров. Этот эффект исчезал, если блокировали специфический тип ионного канала — ATP‑чувствительный калиевый (KATP) канал, или генетически удаляли ключевой компонент KATP только в перицитах. Аналогично, прямой активатор KATP‑каналов мог обратить сужение, вызванное отсутствием кислорода, у нормальных мышей, но не у мышей с дефицитом KATP в перицитах. Мыши без KATP‑каналов в перицитах также теряли кардиозащитный эффект от отдалённой предподготовки в экспериментах на живых животных, что прочно связывает эти каналы с защитным путём.
Тонкая настройка пути через клеточную энергию и сигналы
Дальнейшее исследование показало, как контролируются эти каналы. Команда продемонстрировала, что ключевая роль принадлежит ферменту, чувствительному к энергетическому состоянию клетки — AMP‑активируемой протеинкиназе (AMPK). Блокада AMPK препятствовала открытию капилляров под действием GLP‑1 и смещала KATP‑каналы с поверхности клетки, что наводит на мысль, что AMPK способствует доставке этих каналов на мембрану перицитов, где они могут функционировать. Они также показали, что блокада синтеза оксида азота или мускариновых (ацетилхолиновых) рецепторов сама по себе не усиливала сужение, но специфически препятствовала дилатации, вызванной GLP‑1. Это согласуется с моделью, в которой оксид азота и ацетилхолин действуют выше по потоку, стимулируя AMPK, который в свою очередь продвигает транспорт KATP‑каналов и позволяет GLP‑1 гиперполяризовать и расслаблять перициты.
Что это значит для будущих методов лечения сердца
В совокупности работа выявляет цепь мозг–кишечник–сердце: кратковременный ишемический сигнал в конечности активирует нервы, идущие к кишке, клетки кишечника выбрасывают GLP‑1 в кровоток, и GLP‑1 попадает в сердце, действуя на перициты. Вовлекая KATP‑каналы — при содействии AMPK, оксида азота и ацетилхолина — GLP‑1 заставляет перициты ослабить захват капилляров, восстанавливая кровоток в микроциркуляции после открытия артерии. Для неспециалистов главный вывод таков: защита сердца — это не только восстановление проходимости крупных артерий, но и убеждение крошечных «стражей‑перицитов» открыть капилляры. Поскольку препараты на основе GLP‑1 уже широко используются при диабете и ожирении и демонстрируют сердечно‑сосудистые преимущества, их адаптация для модуляции функции перицитов во время и после инфаркта может стать новым способом уменьшить no‑reflow и улучшить восстановление.
Цитирование: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Ключевые слова: инфаркт миокарда, микроциркуляция, GLP-1, перициты, кардиопротекция