Clear Sky Science · es
La GLP-1 activa los canales KATP en pericitos coronarios como efector de la señalización cerebro-intestino-corazón que media la cardioprotección
Por qué importa proteger los diminutos vasos del corazón
Cuando una arteria coronaria obstruida se reabre tras un infarto, mucha gente asume que el flujo sanguíneo se restaura por completo. Sin embargo, en hasta la mitad de los pacientes, los vasos más pequeños del corazón permanecen cerrados, de modo que partes del músculo cardíaco siguen privadas de sangre. Este problema oculto, denominado “no‑reflow” (ausencia de reflujo), aumenta considerablemente el riesgo de insuficiencia cardíaca y muerte. El estudio resumido aquí revela una vía de señalización cerebro‑intestino‑corazón que puede abrir estos diminutos vasos desde dentro y sugiere nuevas formas de proteger el corazón con fármacos ya conocidos por su uso en la diabetes.
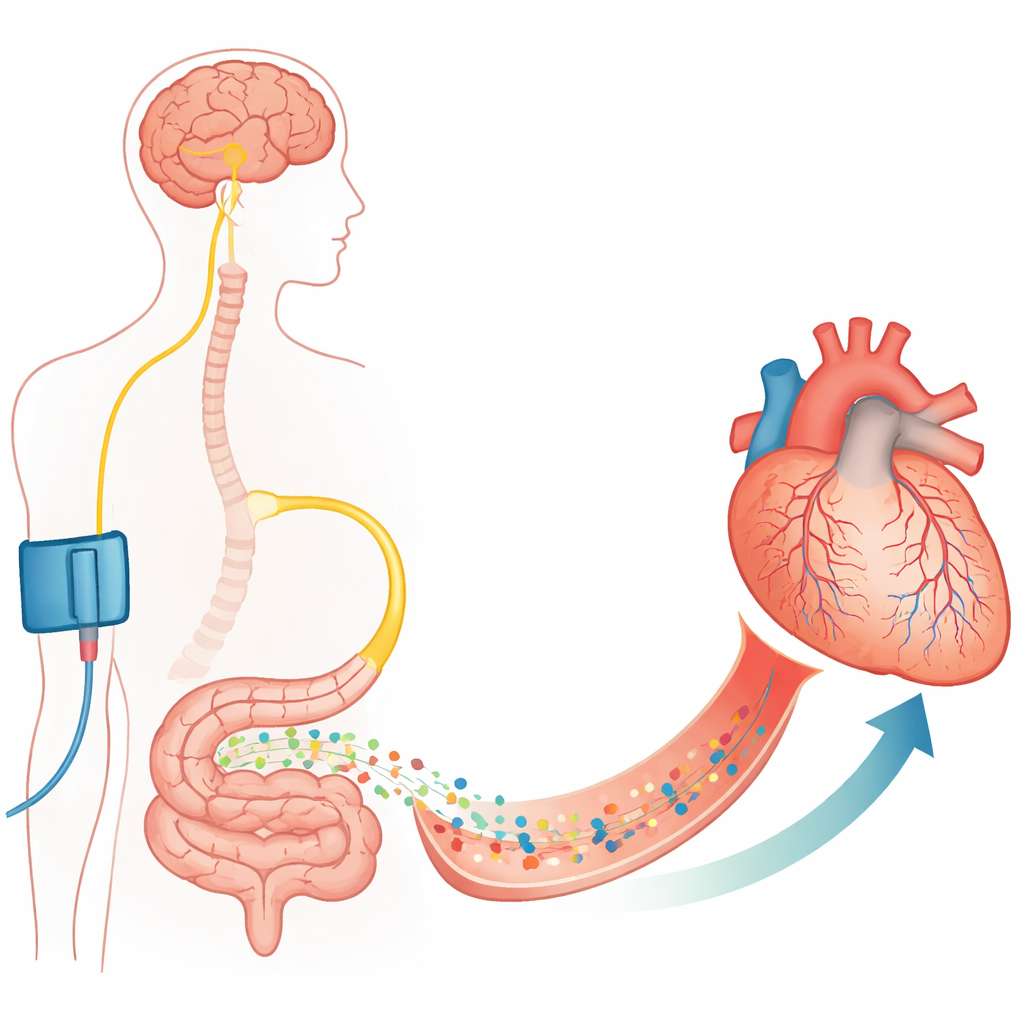
De las arterias grandes a las pequeñas células guardianas
Abrir una arteria coronaria obstruida con un stent salva vidas pero no siempre es suficiente. Los autores se centran en los capilares, los vasos extremadamente finos que realmente entregan oxígeno al músculo cardíaco. Alrededor de estos capilares hay células de soporte llamadas pericitos, que pueden contraer o relajar la pared vascular. Trabajos anteriores mostraron que durante y después de un periodo sin flujo, estos pericitos se contraen y a veces mueren en un estado contraído, estrechando permanentemente los capilares y causando no‑reflow. Este estudio confirma en corazones de rata y ratón que tras una obstrucción controlada y la reapertura de una arteria coronaria, muchos capilares permanecen constrictos en los sitios de los pericitos y una gran fracción deja de transportar sangre, aunque la arteria principal esté permeable.
Una hormona intestinal que habla con los capilares del corazón
Los investigadores se preguntaron entonces si el organismo dispone de un mecanismo propio para relajar estos pericitos. Examinaron un fenómeno llamado precondicionamiento isquémico remoto, en el que cortar brevemente el flujo sanguíneo a una extremidad (por ejemplo con un manguito) protege de algún modo al corazón frente a una obstrucción posterior. Trabajos previos apuntaban al nervio vago y a la hormona intestinal GLP‑1 como mensajeros clave. Usando sondas fluorescentes y anticuerpos, el equipo mostró que los receptores de GLP‑1 están presentes en pericitos coronarios de ratón y en pericitos cardíacos humanos cultivados. En ratas vivas, provocar brevemente isquemia en las extremidades antes de una obstrucción coronaria redujo de forma marcada los bloqueos capilares y restauró el volumen de sangre perfundida en la región cardíaca en riesgo, pero solo si los receptores de GLP‑1 estaban activos. Bloquear estos receptores eliminó el beneficio y el no‑reflow reapareció.
Cómo la GLP-1 hace que los capilares se vuelvan a ensanchar
Para desentrañar el mecanismo, los autores usaron un fragmento aislado y presurizado de corazón de ratón donde pudieron observar capilares y pericitos individuales bajo el microscopio. Cuando eliminaron oxígeno y glucosa del fluido que bañaba el tejido, los pericitos se contraían y los diámetros capilares se reducían. Añadir un fármaco similar a la GLP‑1 (Exendin‑4) mientras continuaban las condiciones de baja oxigenación provocó que los pericitos se relajaran y los capilares se reexpandieran casi hasta su anchura original. Este efecto desapareció si bloquearon un tipo específico de canal iónico conocido como canal potasio sensible al ATP (KATP) o si eliminaron genéticamente un componente clave de KATP únicamente en los pericitos. De modo similar, un activador directo de canales KATP pudo revertir la constricción inducida por el fármaco en ratones normales pero no en animales con eliminación de KATP en pericitos. Los ratones carentes de canales KATP en pericitos también perdieron el beneficio protector del precondicionamiento remoto en experimentos con animales completos, vinculando firmemente estos canales a la vía protectora.
Ajustar la vía mediante la energía celular y la señalización
La historia profundiza en cómo se controlan estos canales. El equipo mostró que una enzima que detecta el estado energético celular, la proteína quinasa activada por AMP (AMPK), es crucial. Bloquear AMPK impidió que la GLP‑1 reabriera los capilares constrictos y desplazó los canales KATP lejos de la superficie celular, lo que sugiere que AMPK ayuda a movilizar estos canales hacia la membrana del pericito donde pueden funcionar. También hallaron que bloquear la producción de óxido nítrico o los receptores muscarínicos (de acetilcolina) no empeoró la constricción por sí mismo, pero bloqueó específicamente la dilatación desencadenada por la GLP‑1. Esto encaja con un modelo en el que el óxido nítrico y la acetilcolina actúan aguas arriba estimulando AMPK, que a su vez promueve el tráfico de canales KATP y permite que la GLP‑1 hiperpolarice y relaje los pericitos.
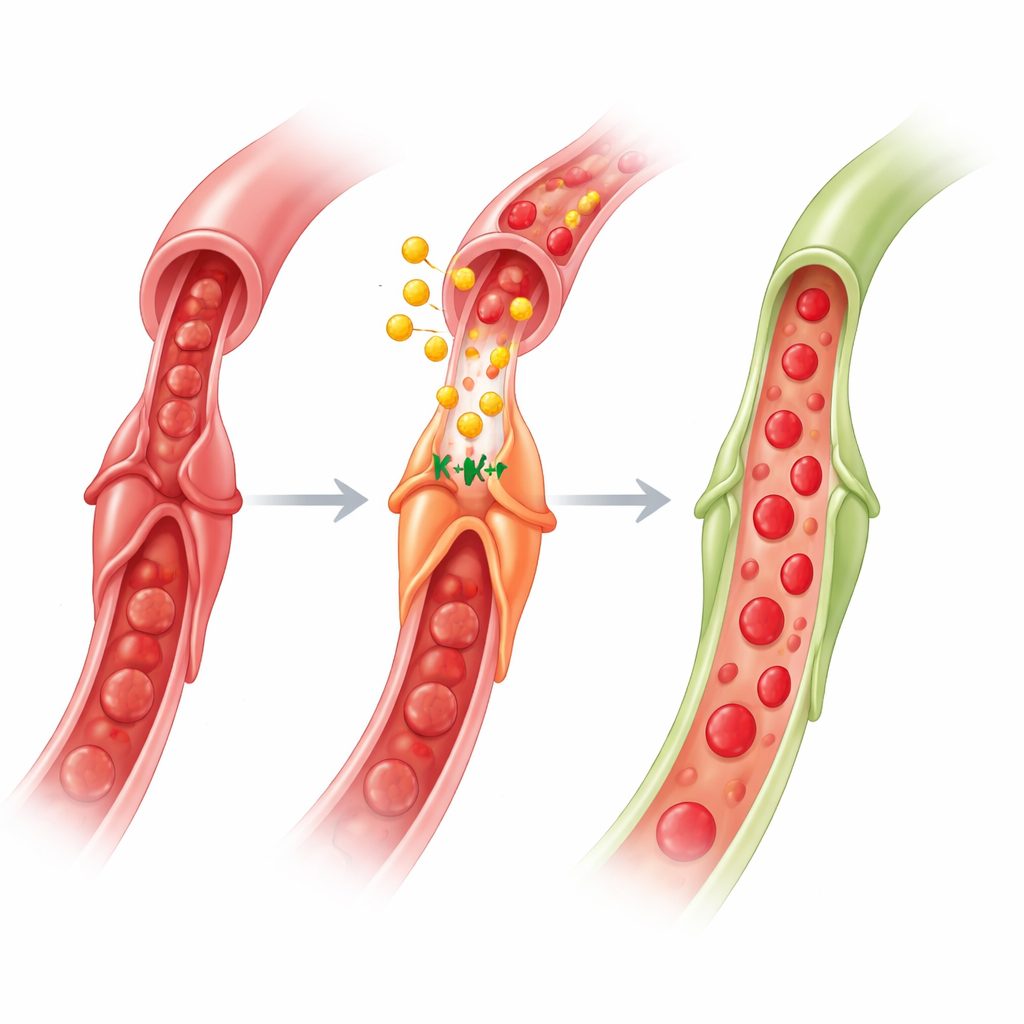
Qué significa esto para futuros tratamientos cardíacos
En conjunto, el trabajo revela un circuito cerebro‑intestino‑corazón: una señal isquémica breve en una extremidad activa nervios hacia el intestino, las células intestinales liberan GLP‑1 al torrente sanguíneo, y la GLP‑1 viaja al corazón para actuar sobre los pericitos. Al activar canales KATP, con la ayuda de AMPK, óxido nítrico y acetilcolina, la GLP‑1 hace que los pericitos aflojen su agarre en los capilares, restaurando el flujo en la microcirculación tras la reapertura de una arteria. Para el público no especializado, el mensaje clave es que proteger el corazón no se trata solo de desobstruir las arterias grandes; también consiste en convencer a las pequeñas células guardianas de que se abran. Dado que los fármacos basados en GLP‑1 ya se usan ampliamente para la diabetes y la obesidad y han mostrado beneficios cardiovasculares, afinarlos para orientar la función de los pericitos durante y después de los infartos podría ofrecer una nueva forma de reducir el no‑reflow y mejorar la recuperación.
Cita: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Palabras clave: infarto de miocardio, microcirculación, GLP-1, pericitos, cardioprotección