Clear Sky Science · sv
GLP-1 aktiverar KATP-kanaler i koronära pericyter som effektor i hjärna-tarm-hjärta‑signalering som medierar hjärtskydd
Varför skydd av hjärtats miniskenor spelar roll
När en tilltäppt kranskärl öppnas igen efter en hjärtinfarkt antar många att blodflödet återställts helt. Ändå förblir de minsta blodkärlen i hjärtat tilltäppta hos upp till hälften av patienterna, så delar av hjärtmuskeln fortsätter att vara blodtörstiga. Detta dolda problem, kallat ”no‑reflow”, ökar kraftigt risken för hjärtsvikt och död. Studien som sammanfattas här avslöjar en hjärna–tarm–hjärta‑signalväg som kan öppna dessa små kärl inifrån och föreslår nya sätt att skydda hjärtat med läkemedel som redan används vid diabetesbehandling.
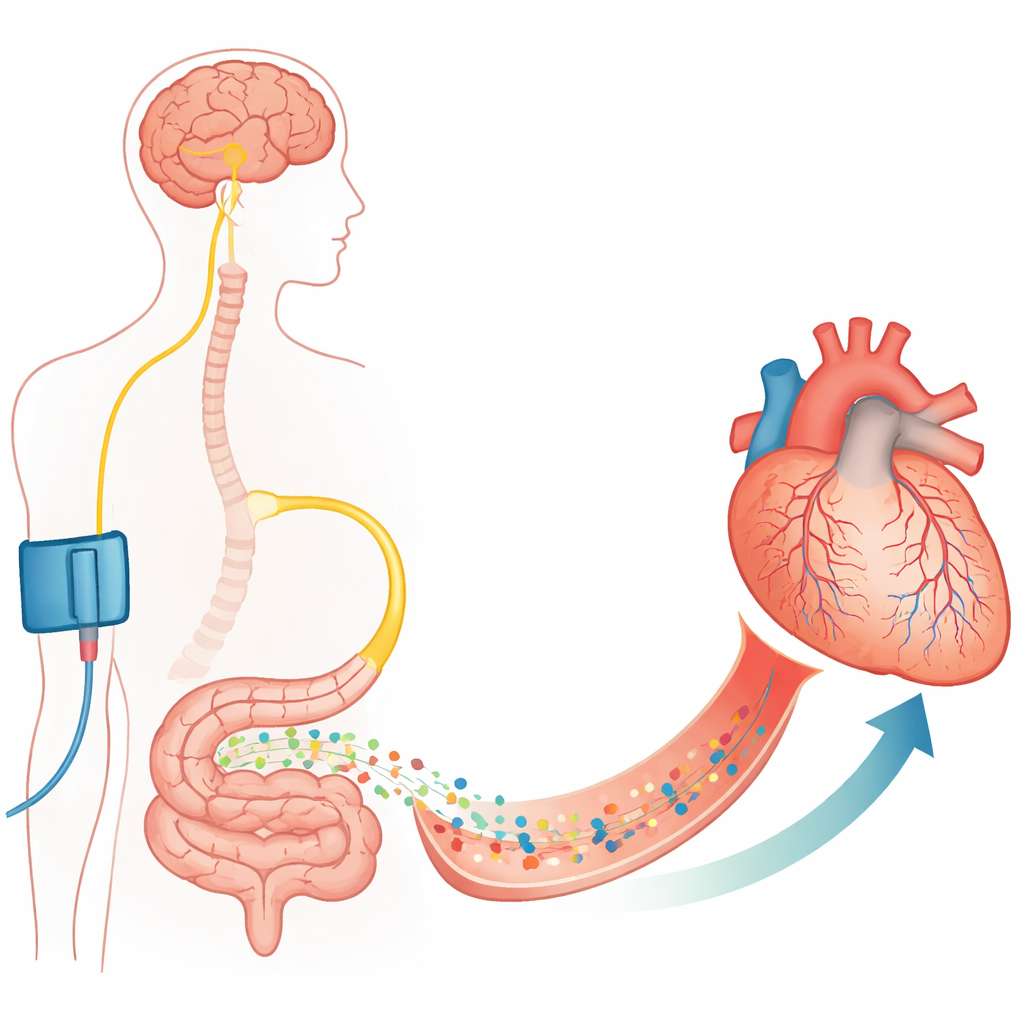
Från stora artärer till små grindvakter
Att öppna ett tilltäppt kranskärl med en stent kan rädda liv men är inte alltid tillräckligt. Författarna fokuserar på kapillärerna, de hårfinna kärlen som faktiskt levererar syre till hjärtmuskel. Omslutna runt dessa kapillärer finns stödjeceller som kallas pericyter, vilka kan dra ihop eller slappna av kärlväggen. Tidigare arbete visade att under och efter en period utan blod så drar pericyterna ihop sig och ibland dör i ett kontraherat tillstånd, vilket permanent förtränger kapillärerna och orsakar no‑reflow. Denna studie bekräftar i rått- och mushjärtan att efter en kontrollerad ocklusion och återöppning av en kransartär förblir många kapillärer förträngda vid pericytställen och en stor andel inte längre för blod, trots att huvudartären är öppen.
Ett hormon från tarmen som talar med hjärtats kapillärer
Forskarna frågade sedan om kroppen har ett inbyggt sätt att få dessa pericyter att slappna av. De undersökte ett fenomen kallat avlägsen ischemisk förkonditionering, där kortvarig avstängning av blodflödet till en extremitet (till exempel med en manschett) på något sätt skyddar hjärtat från en senare ocklusion. Tidigare arbete pekade på vagusnerven och tarmhormonet GLP‑1 som viktiga budbärare. Med fluorescerande prober och antikroppar visade teamet att GLP‑1‑receptorer finns på koronära pericyter hos möss och på odlade mänskliga hjärtpericyter. I levande råttor minskade kortvarig ischemi i bakbenen före en koronär ocklusion kraftigt kapillärblockeringar och återställde perfunderad blodvolym i det hotade hjärtområdet — men bara om GLP‑1‑receptorerna var aktiva. Blockering av dessa receptorer utplånade fördelen och återförde no‑reflow.
Hur GLP-1 får kapillärerna att vidga sig igen
För att dissekera mekanismen använde författarna en isolerad, belastad bit av mushjärta där de kunde i mikroskopi följa enstaka kapillärer och pericyter. När de tog bort syre och glukos från vätskan som badade vävnaden drog pericyterna ihop sig och kapillärernas diametrar krympte. Tillsats av ett GLP‑1‑liknande läkemedel (Exendin‑4) medan låg‑syre‑förhållandena fortsatte fick pericyterna att slappna av och kapillärerna att åter expandera nästan till ursprunglig bredd. Denna effekt försvann om de blockerade en viss typ av jonkanal känd som en ATP‑känslig kaliumkanal (KATP) eller genetiskt tog bort en nyckelkomponent i KATP endast i pericyter. På samma sätt kunde en direkt KATP‑kanalöppnare reversera läkemedelsinducerad förträngning hos normala möss men inte hos pericytspecifika KATP‑knockouter. Möss utan pericyt‑KATP‑kanaler förlorade också det hjärtskyddande resultatet av avlägsen förkonditionering i hela‑djurexperiment, vilket tydligt kopplar dessa kanaler till den skyddande vägen.
Finkalibrering av vägen med cellens energi och signalering
Berättelsen går djupare i hur dessa kanaler kontrolleras. Teamet visade att ett enzym som känner av cellens energitillstånd, AMP‑beroende proteinkinaskinas (AMPK), är avgörande. Blockering av AMPK förhindrade att GLP‑1 återöppnade förträngda kapillärer och försköt KATP‑kanaler bort från cellens yta, vilket antyder att AMPK hjälper till att flytta dessa kanaler till pericytens membran där de kan fungera. De fann också att blockering av kväveoxidsyntes eller muskarina (acetylkolin) receptorer inte förvärrade förträngningen i sig, men specifikt blockerade den vidgning som GLP‑1 utlöste. Detta stämmer med en modell där kväveoxid och acetylkolin verkar uppströms genom att stimulera AMPK, som i sin tur främjar KATP‑kanalernas trafik och möjliggör för GLP‑1 att hyperpolarisera och slappna av pericyterna.
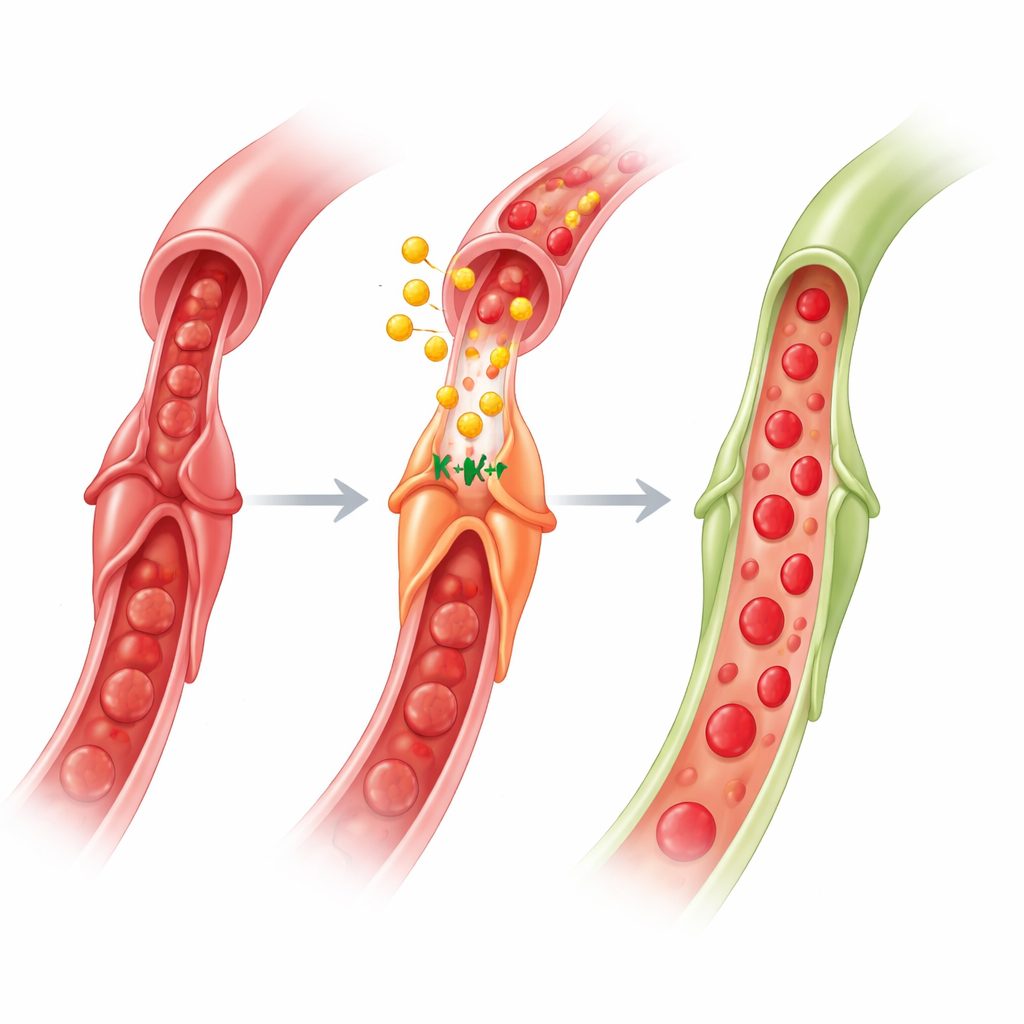
Vad detta betyder för framtida hjärtbehandlingar
Sammantaget visar arbetet en hjärna–tarm–hjärta‑krets: en kortvarig ischemisk signal i en extremitet aktiverar nerver till tarmen, tarmceller släpper ut GLP‑1 i blodet, och GLP‑1 färdas till hjärtat för att verka på pericyter. Genom att engagera KATP‑kanaler — med hjälp av AMPK, kväveoxid och acetylkolin — får GLP‑1 pericyterna att släppa sitt grepp om kapillärerna och återställa flödet i mikrocirkulationen efter att en artär återöppnats. För icke‑specialister är huvudbudskapet att skydd av hjärtat inte bara handlar om att öppna stora artärer; det handlar också om att övertala små grindvaktceller att öppna sig. Eftersom GLP‑1‑baserade läkemedel redan används brett för diabetes och fetma och visat kardiovaskulära fördelar, kan en vidareutveckling för att rikta pericytfunktionen under och efter hjärtinfarkter erbjuda ett nytt sätt att minska no‑reflow och förbättra återhämtning.
Citering: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Nyckelord: hjärtinfarkt, mikrocirkulation, GLP-1, pericyter, hjärtskydd