Clear Sky Science · zh
基于铁死亡纳米疗法改善结直肠癌免疫抑制微环境中的肿瘤相关成纤维细胞
这项研究对结肠癌患者为何重要
许多结直肠癌患者无法从现有突破性免疫疗法中获益,因为他们的肿瘤被一层坚固的支持细胞包围和保护。本研究探索了一种新途径,利用特制的磁性纳米颗粒选择性破坏这些支持细胞,打开肿瘤屏障以便机体自身免疫防御进入,同时也有助于杀伤癌细胞。
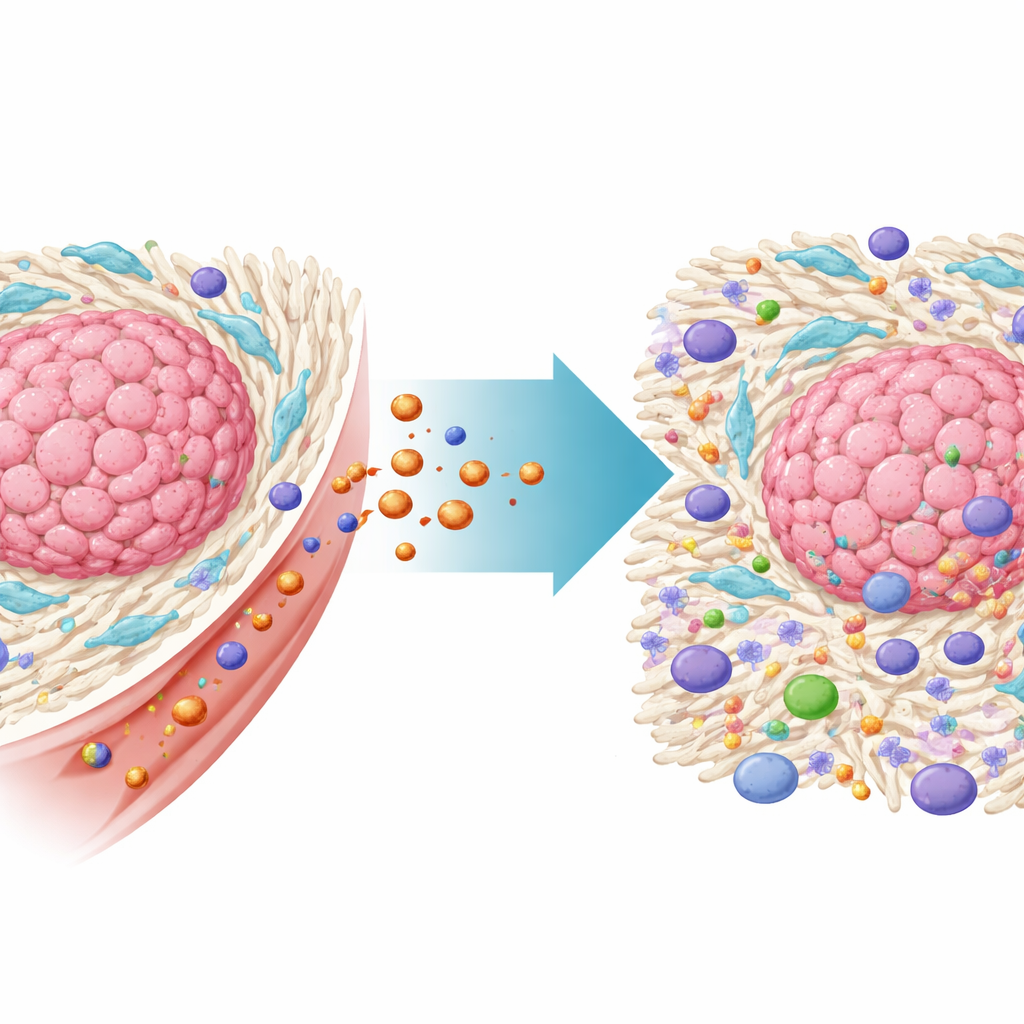
隐藏的帮手——为肿瘤提供保护
结直肠肿瘤生长在由非癌细胞组成的复杂“邻里”中,称为肿瘤微环境。其中最重要的成分之一是肿瘤相关成纤维细胞(CAFs),一种被肿瘤劫持的结缔组织细胞。CAFs在癌组织周围构建致密的细胞外基质支架,物理上阻挡免疫细胞和药物的进入。它们还释放抑制免疫反应的信号并帮助癌细胞抵抗治疗。本研究的大规模患者数据证实,富含CAFs的结直肠癌与更差的生存率和对免疫疗法的耐受性相关,凸显了直接针对这些细胞的必要性。
针对肿瘤“支持细胞”的智能纳米疗法
研究者开发了具有核壳结构的微小铜-铁磁性纳米颗粒,专门设计为更易被CAFs摄取。这些颗粒具有两项关键物理特性:能够将近红外激光转化为热能,并在细胞内催化生成有毒的含氧活性分子。由于CAFs天然比正常成纤维细胞或许多肿瘤细胞摄取更多纳米颗粒,它们成为主要靶标。研究团队还在部分颗粒表面连接了一种短的类DNA适配体AS1411,引导颗粒更有效地朝向在细胞膜上呈现核蛋白(nucleolin)的成纤维细胞和肿瘤细胞。
触发新型细胞死亡并重塑肿瘤信号
进入CAFs后,纳米颗粒释放铁和铜离子。铁促进活性氧(ROS)的产生,而铜降低一种名为GPX4的保护性酶的水平。两者联合将CAFs推向铁死亡——一种由细胞膜不可控氧化驱动的细胞死亡形式。在体外培养和动物模型中,CAFs比正常成纤维细胞对该过程更为脆弱。与此同时,受处理的CAFs改变了其分泌的化学信号混合:那些通常促进肿瘤生长和免疫抑制的信号减少,而有助于招募和激活免疫细胞的信号增加。因此,暴露于“重新编程”成纤维细胞分泌物的癌细胞在增殖、迁移和获得侵袭性性状方面能力下降。
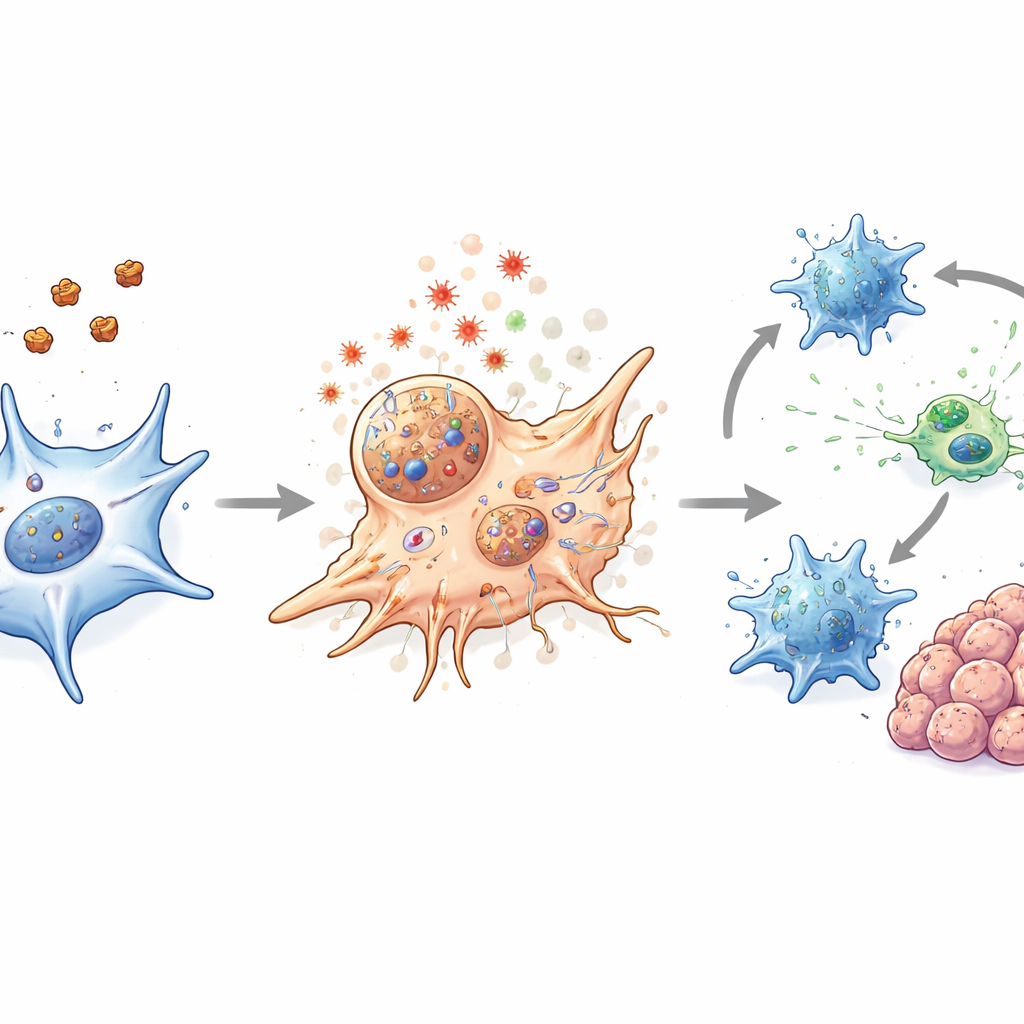
在肿瘤内唤醒免疫系统
在多种结直肠癌小鼠模型中,包括标准移植肿瘤、自发性肠道肿瘤的遗传模型,以及来源于患者的肿瘤和类器官,纳米颗粒治疗使肿瘤缩小且安全性良好。重要的是,该疗法不仅仅杀死CAFs,还松解了肿瘤周围的物理屏障并改变了局部化学环境,促进了免疫活性。树突状细胞作为免疫系统的哨兵和“教师”,在治疗后显示出更强的成熟迹象。杀伤性CD8 T细胞变得更活跃并产生更多与有效肿瘤攻击相关的分子,即便其总体数量并未显著改变。当纳米颗粒与温和的激光加热结合时,这些效应进一步增强,且对正常组织未见明显损害。
从实验室模型走向未来治疗
为测试该策略在真实世界情境下的适用性,团队将其应用于来自患者的肿瘤样本和培养的迷你肿瘤(类器官)。纳米颗粒疗法,尤其是携带AS1411靶向成分并结合激光激活的版本,强烈损伤了癌变组织及其周围成纤维细胞,同时在很大程度上保留了来自健康结肠组织的类器官。跨多个复杂模型,呈现出相同模式:针对CAFs的纳米疗法削弱了肿瘤的保护性外壳,重新激活了局部免疫反应,并直接损伤癌细胞。
这对未来癌症治疗可能意味着什么
研究表明,攻击肿瘤的“帮手”与直接攻击肿瘤细胞同样重要。通过使用基于铁死亡的磁性纳米颗粒选择性地使肿瘤相关成纤维细胞失能,研究者既拆除了物理屏障,又解除或减弱了对免疫系统的化学抑制。在仍处于临床前阶段的情况下,这项工作指向一种新型治疗类别:将靶向纳米技术、可控的细胞死亡和免疫激活结合的策略。此类方法有望使对免疫疗法耐受的结直肠癌变得更易响应,并改善当前难治肿瘤患者的预后。
引用: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
关键词: 结直肠癌, 肿瘤微环境, 纳米颗粒疗法, 肿瘤相关成纤维细胞, 铁死亡