Clear Sky Science · nl
Verbetering van door colorectale kanker geassocieerde fibroblasten in een immunosuppressieve micro-omgeving door ferroptose-gebaseerde nanotherapie
Waarom dit onderzoek belangrijk is voor patiënten met colonkanker
Veel mensen met colorectale kanker profiteren niet van de huidige baanbrekende immunotherapieën omdat hun tumoren omringd en beschermd worden door een stevige laag steuncellen. Deze studie onderzoekt een nieuwe manier om dat schild te doorbreken met speciaal ontworpen magnetische nanodeeltjes die selectief deze steuncellen beschadigen, waardoor de tumor toegankelijker wordt voor de eigen immuunverdediging van het lichaam en tegelijkertijd helpt kankercellen te doden.
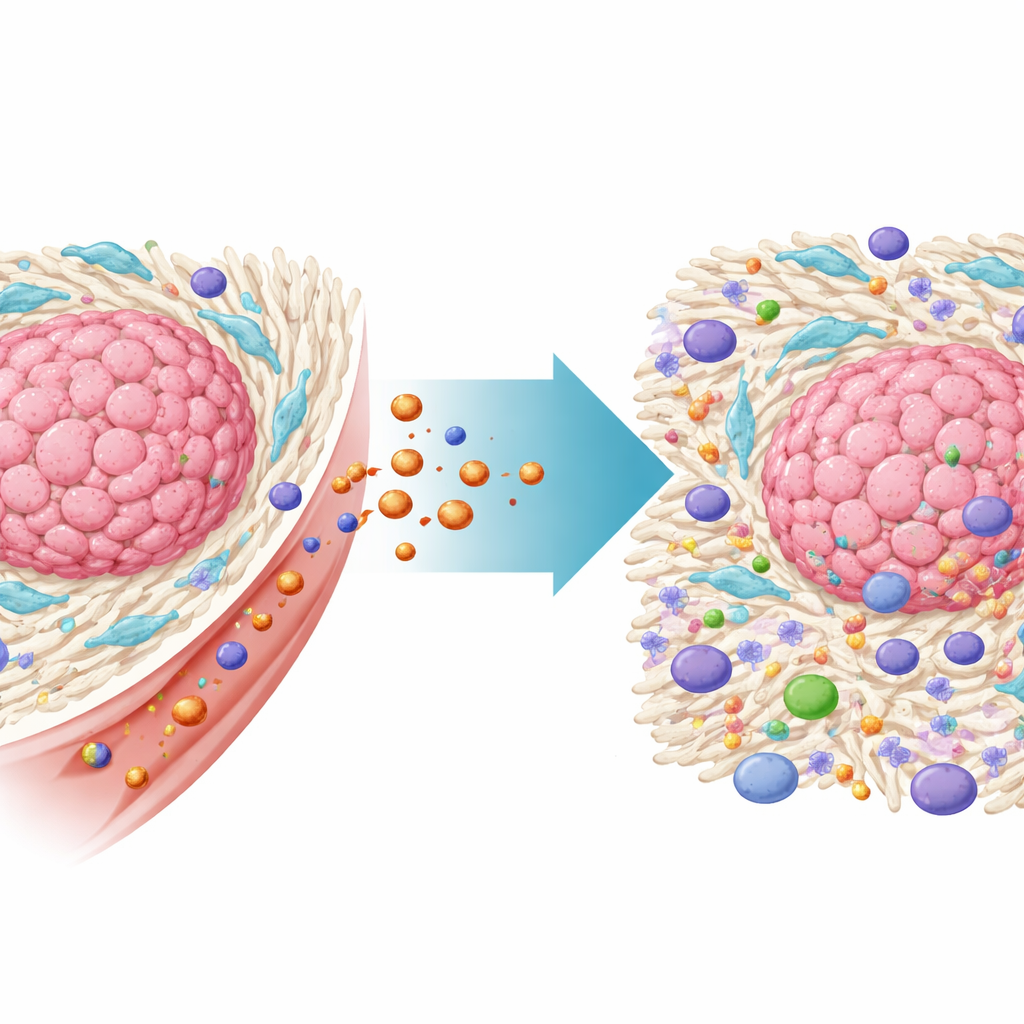
De verborgen helpers die tumoren afschermen
Colorectale tumoren groeien binnen een complex netwerk van niet-kankerachtige cellen, de zogenaamde tumormicro-omgeving. Een van de belangrijkste spelers hierin zijn kanker-geassocieerde fibroblasten, of CAFs, een type bindweefselcel dat door de tumor gekaapt wordt. CAFs bouwen een dicht geraamte van extracellulaire matrix rond de kanker, dat immuuncellen en geneesmiddelen fysiek blokkeert. Ze geven ook chemische signalen af die immuunresponsen verzwakken en kankercellen helpen therapieresistent te worden. Grootschalige patiëntgegevens in deze studie bevestigden dat colorectale kankers met veel CAFs geassocieerd waren met slechtere overleving en weerstand tegen immunotherapie, wat het belang onderstreept om deze cellen direct te targeten.
Een slimme nanotherapie gericht op de steuncellen van de tumor
De onderzoekers ontwikkelden zeer kleine koper–ijzer magnetische nanodeeltjes met een kern–mantelstructuur die speciaal aantrekkelijk zijn voor CAFs. Deze deeltjes hebben twee belangrijke fysieke eigenschappen: ze kunnen nabij-infrarood laserlicht omzetten in warmte en ze kunnen de vorming katalyseren van toxische zuurstofgebaseerde moleculen binnenin cellen. Omdat CAFs van nature meer nanodeeltjes opnemen dan normale fibroblasten of veel tumorcellen, worden zij het primaire doelwit. Het team hechtte bovendien een kort DNA-achtig aptameer, AS1411, aan het oppervlak van sommige deeltjes om ze efficiënter naar fibroblasten en tumorcellen te leiden die het eiwit nucleoline op hun buitenmembraan vertonen.
Het opwekken van een nieuwe vorm van celdood en het herbedraden van tumorsignalen
Eens binnenin CAFs, geven de nanodeeltjes ijzer- en kopermionen vrij. IJzer voedt de productie van reactieve zuurstofsoorten, terwijl koper de niveaus verlaagt van een beschermend enzym dat GPX4 heet. Samen duwen deze veranderingen CAFs in ferroptose, een vorm van celdood die wordt aangedreven door ongecontroleerde oxidatie van celmembranen. In kweek en in diermodellen bleken CAFs kwetsbaarder voor dit proces dan normale fibroblasten. Tegelijkertijd veranderden de behandelde CAFs de samenstelling van de chemische boodschappers die ze afscheiden: signalen die normaal tumorgroei en immuunsuppressie bevorderen werden verminderd, terwijl andere signalen die immuuncellen aantrekken en activeren toenamen. Als gevolg daarvan werden kankercellen die blootgesteld werden aan de "herschikte" fibroblastsecreties minder in staat om te groeien, te migreren en invasieve eigenschappen aan te nemen.
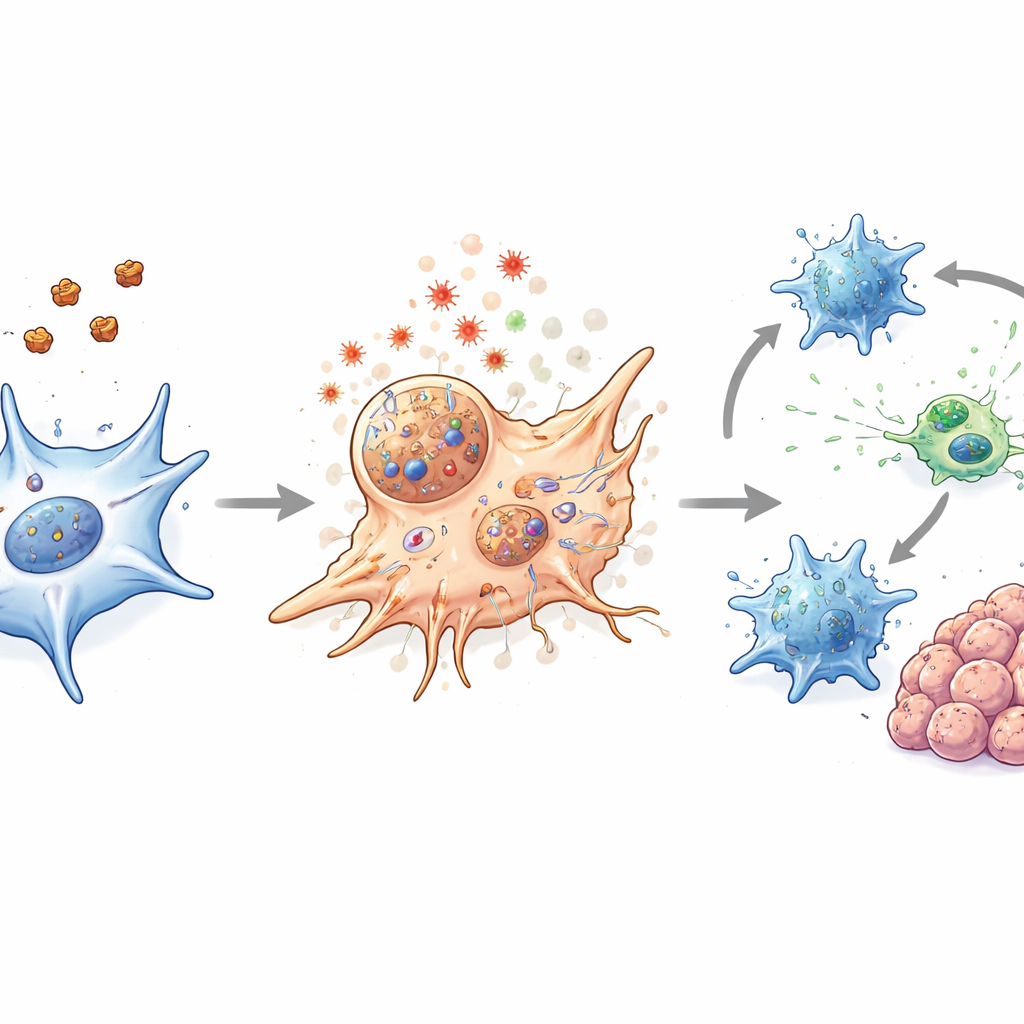
Het immuunsysteem binnen de tumor wakker schudden
In muismodellen van colorectale kanker, inclusief standaard geïmplanteerde tumoren, een genetisch model dat spontaan darmtumoren ontwikkelt, en patiënt-afgeleide tumoren en organoïden, verkleinde de nanodeeltjebehandeling tumoren en deed dit op een veilige manier. Belangrijk was dat de therapie meer deed dan enkel CAFs doden. Ze maakte ook de fysieke barrière rond tumoren losser en verschuifde de lokale chemie op een manier die immuunactiviteit stimuleerde. Dendritische cellen, die fungeren als wachtposten en leraren van het immuunsysteem, toonden sterkere aanwijzingen van rijping na behandeling. Cytotoxische CD8 T-cellen werden actiever en produceerden meer moleculen geassocieerd met effectieve tumoraanval, ook al veranderde hun totale aantal niet dramatisch. Wanneer nanodeeltjes werden gecombineerd met milde laserverhitting, werden deze effecten verder versterkt zonder merkbare schade aan normaal weefsel.
Van laboratoriummodellen naar toekomstige behandelingen
Om te testen hoe breed toepasbaar deze benadering zou kunnen zijn in realistische omstandigheden, paste het team hun strategie toe op tumorstalen en mini-tumoren (organoïden) gekweekt van patiënten. De nanodeeltjetherapie, vooral de versie met het AS1411-targetingcomponent en in combinatie met laseractivering, beschadigde kankergeweefsel en de omringende fibroblasten sterk, terwijl organoïden uit gezond colonweefsel grotendeels gespaard bleven. In meerdere geavanceerde modellen verscheen hetzelfde patroon: op CAF gerichte nanotherapie verzwakte de beschermende schaal van de tumor, wekte lokale immuunresponsen opnieuw en beschadigde direct kankercellen.
Wat dit kan betekenen voor toekomstige kankerzorg
De studie suggereert dat het aanvallen van de helpers van de tumor net zo belangrijk kan zijn als het aanvallen van de tumorcellen zelf. Door ferroptose-gebaseerde magnetische nanodeeltjes te gebruiken om kanker-geassocieerde fibroblasten selectief uit te schakelen, konden de onderzoekers zowel fysieke barrières ontmantelen als chemische remmen op het immuunsysteem opheffen bij colorectale kanker. Hoewel dit werk nog in de preklinische fase verkeert, wijst het op een nieuwe klasse van behandelingen die gerichte nanotechnologie, gecontroleerde celdood en immuunactivatie combineren. Dergelijke strategieën zouden op termijn resistente colorectale kankers gevoeliger voor immunotherapie kunnen maken en de uitkomsten kunnen verbeteren voor patiënten van wie de tumoren momenteel moeilijk te behandelen zijn.
Bronvermelding: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Trefwoorden: colorectale kanker, tumormicro-omgeving, nanodeeltjetherapie, kanker-geassocieerde fibroblasten, ferroptose