Clear Sky Science · pl
Poprawa funkcji fibroblastów związanych z rakiem jelita grubego w immunosupresyjnym mikrośrodowisku za pomocą nanoterapii opartej na ferroptozie
Dlaczego to badanie ma znaczenie dla pacjentów z rakiem jelita
Wielu pacjentów z rakiem jelita grubego nie odnosi korzyści z przełomowych terapii immunologicznych, ponieważ ich guzy są otoczone i chronione przez zwartą warstwę komórek podporowych. To badanie bada nowy sposób przełamania tej osłony przy użyciu specjalnie zaprojektowanych magnetycznych nanocząstek, które selektywnie uszkadzają te komórki podporowe, otwierając guz na własne mechanizmy odpornościowe organizmu, a jednocześnie pomagając w niszczeniu komórek nowotworowych.
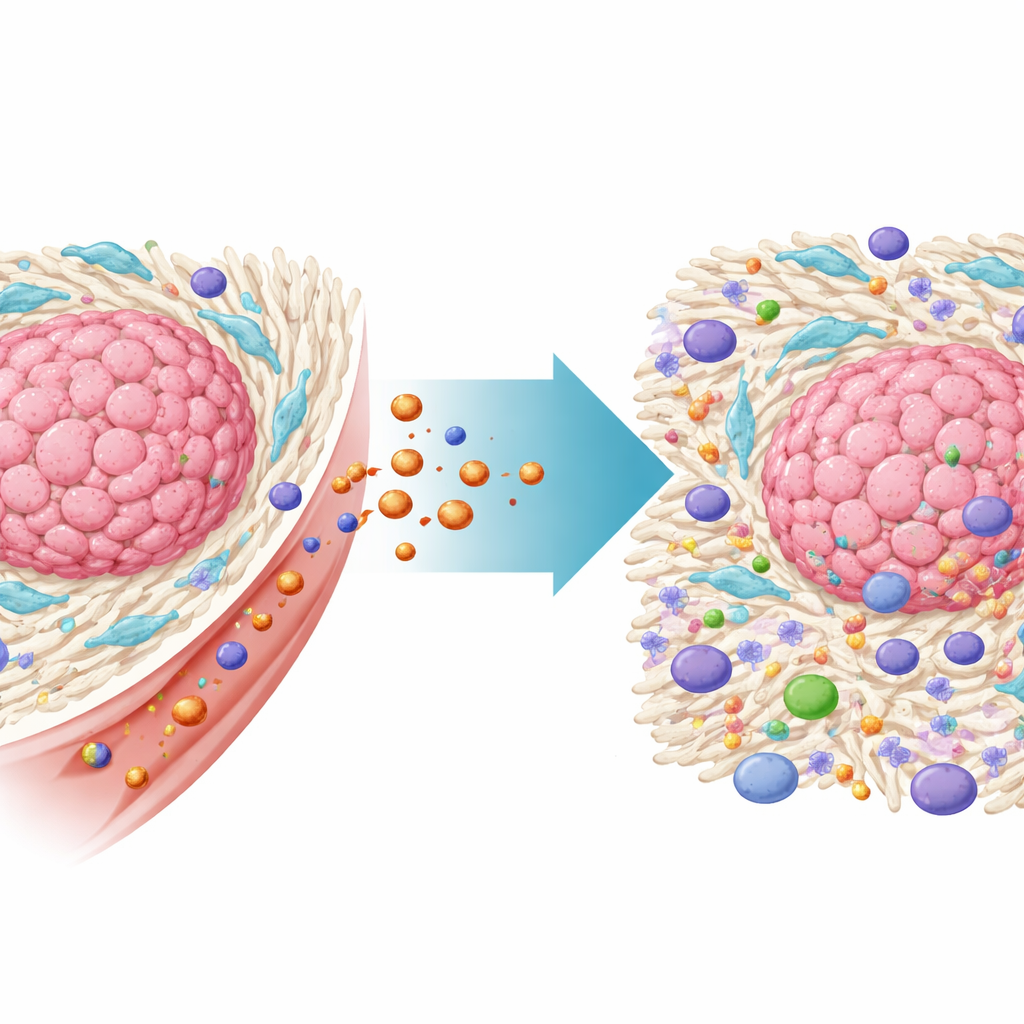
Ukryci pomocnicy chroniący guzy
Guzy jelita grubego rozwijają się w złożonym sąsiedztwie komórek nienowotworowych zwanym mikrośrodowiskiem guza. Do jednych z najważniejszych należą fibroblasty związane z nowotworem (CAFs) — typ komórek tkanki łącznej, który zostaje wykorzystany przez guz. CAFs tworzą gęstą strukturę macierzy zewnątrzkomórkowej wokół nowotworu, co fizycznie blokuje dostęp komórek odpornościowych i leków. Wydzielają też sygnały chemiczne osłabiające odpowiedź immunologiczną i pomagające komórkom nowotworowym opierać się terapiom. Dane pacjentów z tego badania potwierdziły, że raki jelita grubego bogate w CAFs wiążą się z gorszym przeżyciem i opornością na immunoterapię, co podkreśla potrzebę bezpośredniego celowania w te komórki.
Inteligentna nanoterapia ukierunkowana na komórki podporowe guza
Naukowcy opracowali maleńkie magnetyczne nanocząstki miedź–żelazo o strukturze typu rdzeń–powłoka, zaprojektowane tak, by szczególnie przyciągać CAFs. Cząstki te mają dwie kluczowe właściwości fizyczne: potrafią przekształcać światło bliskiej podczerwieni w ciepło oraz katalizować powstawanie toksycznych cząsteczek tlenowych wewnątrz komórek. Ponieważ CAFs naturalnie wchłaniają więcej nanocząstek niż zwykłe fibroblasty czy wiele komórek nowotworowych, stają się głównym celem. Zespół przyłączył też do powierzchni niektórych cząstek krótki aptamer podobny do DNA, zwany AS1411, kierując je skuteczniej do fibroblastów i komórek nowotworowych, które na swojej zewnętrznej błonie wykazują białko nukleolina.
Wywołanie nowej formy śmierci komórkowej i przestawienie sygnałów w guzie
Po dostaniu się do CAFs nanocząstki uwalniają jony żelaza i miedzi. Żelazo napędza produkcję reaktywnych form tlenu, natomiast miedź obniża poziomy ochronnego enzymu GPX4. Wspólnie te zmiany popychają CAFs w kierunku ferroptozy — formy śmierci komórkowej spowodowanej niekontrolowaną oksydacją błon komórkowych. W hodowlach i modelach zwierzęcych CAFs okazały się bardziej podatne na ten proces niż normalne fibroblasty. Równocześnie leczone CAFs zmieniły profil uwalnianych mediatorów: sygnały normalnie sprzyjające wzrostowi guza i tłumiące układ odpornościowy zostały zmniejszone, zaś wzrosły czynniki pomagające rekrutować i aktywować komórki odpornościowe. W rezultacie komórki nowotworowe wystawione na „reprgramowane” wydzieliny fibroblastów stały się mniej zdolne do wzrostu, migracji i nabywania cech inwazyjnych.
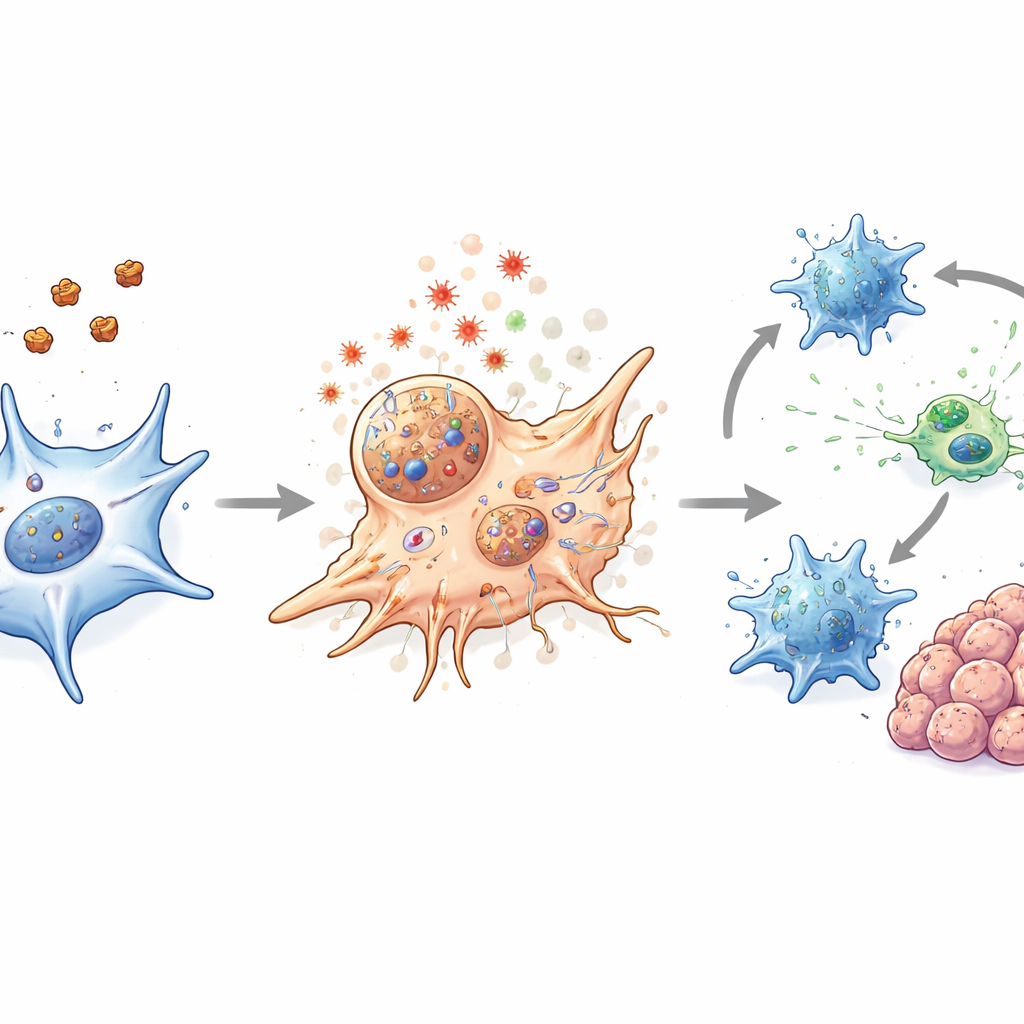
Rozbudzenie układu odpornościowego wewnątrz guza
W modelach mysich raka jelita grubego, obejmujących standardowe guzy wszczepione, model genetyczny rozwijający spontaniczne guzy jelitowe oraz guzy i organoidy pochodzące od pacjentów, leczenie nanocząstkami zmniejszało rozmiar guzów i było bezpieczne. Co ważne, terapia robiła więcej niż tylko zabijać CAFs. Luzowała też barierę fizyczną wokół guzów i zmieniała lokalną chemię w sposób sprzyjający aktywności immunologicznej. Komórki dendrytyczne — pełniące rolę strażników i nauczycieli układu odpornościowego — wykazywały silniejsze cechy dojrzewania po terapii. Komórki efektorowe CD8 stały się bardziej aktywne i produkowały więcej cząsteczek związanych z efektywnym atakiem na guz, nawet jeśli ich ogólna liczba nie zmieniła się dramatycznie. Gdy nanocząstki połączono z łagodnym ogrzewaniem laserowym, efekty te uległy dalszemu wzmocnieniu bez widocznych szkód dla tkanek normalnych.
Od modeli laboratoryjnych ku przyszłym terapiom
Aby sprawdzić, jak szeroko podejście to może działać w realnych warunkach, zespół zastosował swoją strategię do próbek tumorów i mini-guzów (organoidy) hodowanych od pacjentów. Terapia nanocząstkami, szczególnie wersja zawierająca element celujący AS1411 i stosowana wraz z aktywacją laserową, silnie uszkadzała tkanki nowotworowe i otaczające je fibroblasty, przy jednoczesnym względnym oszczędzeniu organoidów pochodzących z zdrowej tkanki jelita. W wielu zaawansowanych modelach powtarzał się ten sam wzorzec: nanoterapia ukierunkowana na CAFs osłabiała ochronną powłokę guza, przywracała lokalne odpowiedzi immunologiczne i bezpośrednio raniła komórki nowotworowe.
Co to może znaczyć dla przyszłej opieki onkologicznej
Badanie sugeruje, że atakowanie pomocników guza może być równie ważne jak atakowanie samych komórek nowotworowych. Poprzez zastosowanie magnetycznych nanocząstek wywołujących ferroptozę w celu selektywnego unieszkodliwienia fibroblastów związanych z nowotworem, badacze zdołali zarówno rozebrać fizyczne bariery, jak i zdjąć chemiczne hamulce układu odpornościowego w raku jelita grubego. Choć prace te pozostają na etapie przedklinicznym, wskazują na nową klasę terapii łączących ukierunkowaną nanotechnologię, kontrolowaną śmierć komórkową i aktywację odporności. Takie strategie mogłyby w przyszłości uczynić oporne raki jelita grubego bardziej podatnymi na immunoterapię i poprawić wyniki leczenia u pacjentów, których guzy są obecnie trudne do leczenia.
Cytowanie: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, terapia nanopartikularna, fibroblasty związane z nowotworem, ferroptoza