Clear Sky Science · de
Verbesserung von krebsassoziierten Fibroblasten bei kolorektalem Krebs im immunsuppressiven Mikroenvironment durch ferroptosebasierte Nanotherapie
Warum diese Forschung für Darmkrebspatienten wichtig ist
Viele Menschen mit kolorektalem Krebs profitieren nicht von den heutigen Durchbruch-Immuntherapien, weil ihre Tumoren von einer dichten Schicht stützender Zellen umgeben und geschützt sind. Diese Studie untersucht einen neuen Weg, diese Schutzschicht zu durchbrechen, indem speziell entwickelte magnetische Nanopartikel eingesetzt werden, die gezielt diese Stützzellen schädigen, den Tumor für die körpereigenen Immunabwehr öffnen und gleichzeitig dazu beitragen, Krebszellen zu zerstören.
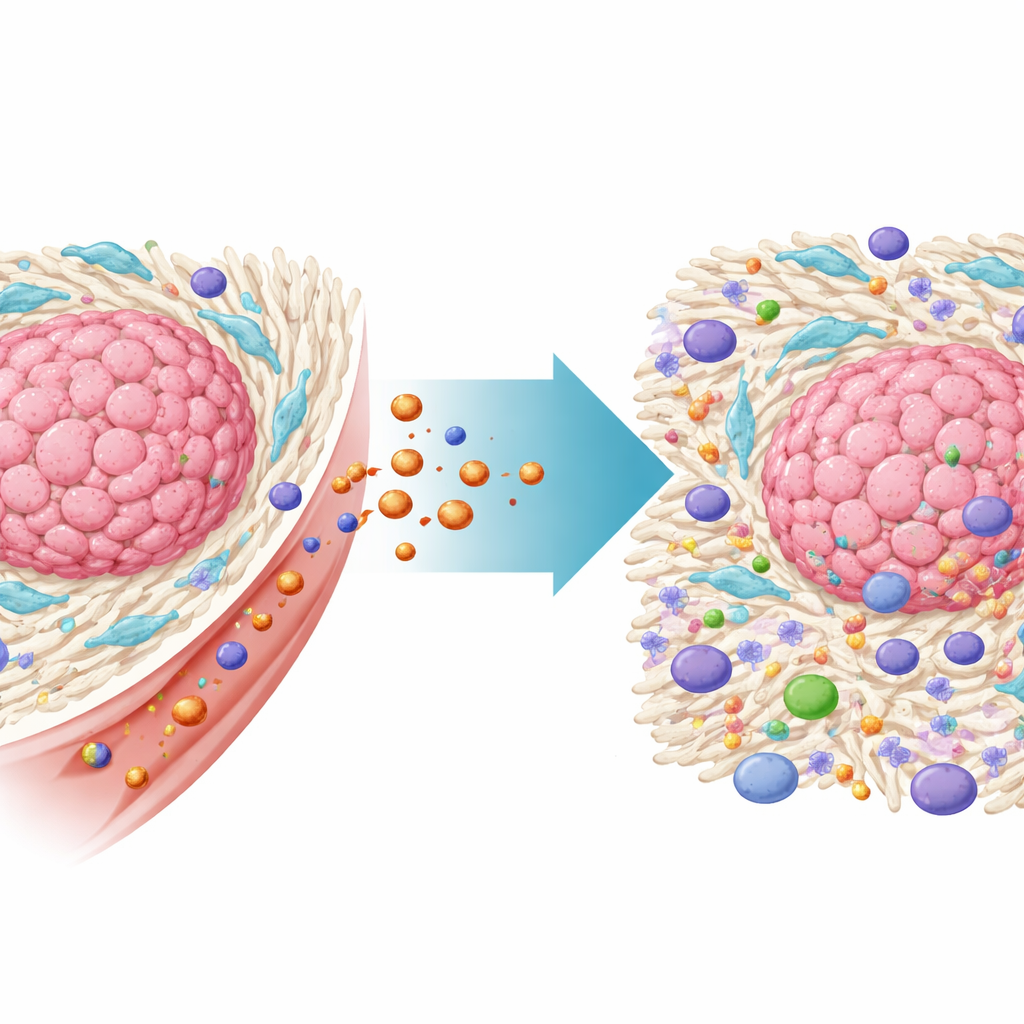
Die versteckten Helfer, die Tumoren abschirmen
Kolorektale Tumoren wachsen in einer komplexen Nachbarschaft nicht-krebsartiger Zellen, der sogenannten Tumormikroumgebung. Zu den wichtigsten gehören krebsassoziierte Fibroblasten (CAFs), eine Art Bindegewebszellen, die vom Tumor vereinnahmt werden. CAFs bauen ein dichtes Gerüst aus extrazellulärer Matrix um den Krebs auf, das physisch Immunzellen und Medikamente am Eindringen hindert. Zudem setzen sie chemische Signale frei, die die Immunantwort schwächen und Krebszellen helfen, Therapien zu widerstehen. Umfangreiche Patientendaten in dieser Studie bestätigten, dass kolorektale Karzinome mit hohem CAF-Anteil mit schlechterer Überlebensprognose und Immuntherapie-Resistenz verbunden sind, was die Notwendigkeit unterstreicht, diese Zellen direkt anzugreifen.
Eine intelligente Nanotherapie, die auf die Stützzellen des Tumors zielt
Die Forschenden entwickelten winzige Kupfer‑Eisen‑Magnetnanopartikel mit Kern‑Schale‑Struktur, die so gestaltet sind, dass sie besonders attraktiv für CAFs sind. Diese Partikel haben zwei zentrale physikalische Eigenschaften: Sie wandeln nahinfrarotes Laserlicht in Wärme um und katalysieren die Bildung toxischer sauerstoffbasierter Moleküle innerhalb von Zellen. Da CAFs von Natur aus mehr Nanopartikel aufnehmen als normale Fibroblasten oder viele Tumorzellen, werden sie zum primären Ziel. Das Team befestigte außerdem an der Oberfläche einiger Partikel ein kurzes DNA‑ähnliches Aptamer namens AS1411, das sie gezielter zu Fibroblasten und Tumorzellen leitet, die ein Protein namens Nucleolin auf ihrer Außenmembran zeigen.
Auslösen einer neuen Form des Zelltods und Umprogrammierung tumoraler Signale
Einmal in den CAFs, geben die Nanopartikel Eisen‑ und Kupferionen frei. Eisen treibt die Produktion reaktiver Sauerstoffspezies an, während Kupfer die Konzentration eines schützenden Enzyms namens GPX4 reduziert. Zusammengenommen treiben diese Veränderungen CAFs in die Ferroptose, eine Form des Zelltods, die durch unkontrollierte Oxidation von Zellmembranen ausgelöst wird. In Zellkulturversuchen und Tiermodellen erwiesen sich CAFs als anfälliger für diesen Prozess als normale Fibroblasten. Gleichzeitig veränderten die behandelten CAFs das Spektrum der von ihnen abgegebenen chemischen Botenstoffe: Signale, die normalerweise Tumorwachstum und Immunsuppression fördern, wurden reduziert, während solche, die Immunzellen anlocken und aktivieren, zunahmen. Infolgedessen waren Krebszellen, die den "umprogrammierten" Fibroblasten‑Sekreten ausgesetzt waren, weniger in der Lage zu wachsen, zu migrieren und invasive Eigenschaften anzunehmen.
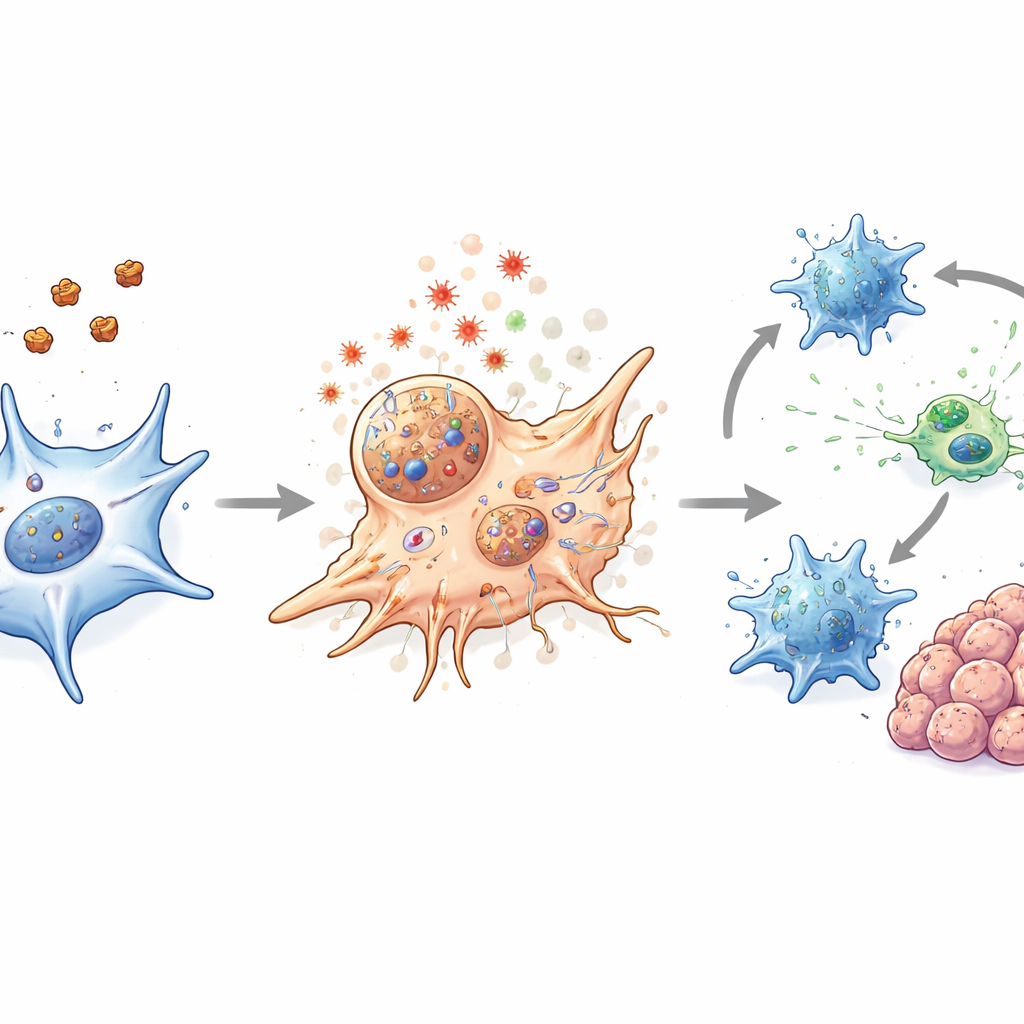
Wecken des Immunsystems innerhalb des Tumors
In Mausmodellen des kolorektalen Krebses — einschließlich standardisierter implantierter Tumoren, eines genetischen Modells, das spontan Darmtumoren entwickelt, sowie patientenabgeleiteter Tumoren und Organoide — verkleinerte die Nanopartikelbehandlung die Tumoren und erwies sich als sicher. Wichtig ist, dass die Therapie mehr bewirkte, als nur CAFs zu töten. Sie lockerte auch die physikalische Barriere um die Tumoren und veränderte die lokale Chemie so, dass sie die Immunaktivität förderte. dendritische Zellen, die als Wächter und Lehrmeister des Immunsystems fungieren, zeigten nach der Behandlung stärkere Reifungszeichen. Killer‑CD8‑T‑Zellen wurden aktiver und produzierten mehr Moleküle, die mit effektivem Tumorangriff assoziiert sind, obwohl ihre Gesamtzahlen nicht dramatisch anstiegen. In Kombination mit schonender Laserwärme wurden diese Effekte weiter verstärkt, ohne erkennbare Schädigung von normalem Gewebe.
Von Labor‑Modellen hin zu zukünftigen Therapien
Um zu prüfen, wie breit anwendbar dieser Ansatz in realen Situationen sein könnte, wandte das Team seine Strategie auf Tumorproben und Mini‑Tumoren (Organoide) an, die aus Patientengewebe gezüchtet wurden. Die Nanopartikeltherapie, insbesondere die Variante mit dem AS1411‑Targeting und der Laseraktivierung, schädigte das krebsartige Gewebe und die umliegenden Fibroblasten deutlich, während Organoide, die aus gesundem Kolongewebe gewachsen waren, weitgehend verschont blieben. In mehreren anspruchsvollen Modellen zeigte sich dasselbe Muster: CAF‑fokussierte Nanotherapie schwächte die Schutzschale des Tumors, erweckte lokale Immunantworten und verletzte Krebszellen direkt.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Die Studie legt nahe, dass der Angriff auf die Helfer des Tumors genauso wichtig sein kann wie der Angriff auf die Tumorzellen selbst. Durch den Einsatz ferroptosebasierter magnetischer Nanopartikel zur selektiven Deaktivierung krebsassoziierter Fibroblasten konnten die Forschenden sowohl physikalische Barrieren abbauen als auch chemische Bremsen des Immunsystems im kolorektalen Krebs lösen. Obwohl diese Arbeit noch präklinisch ist, weist sie auf eine neue Klasse von Behandlungsstrategien hin, die gezielte Nanotechnologie, kontrollierten Zelltod und Immunaktivierung kombinieren. Solche Ansätze könnten eines Tages resistente kolorektale Karzinome immuntherapie‑empfindlicher machen und die Ergebnisse für Patientinnen und Patienten verbessern, deren Tumoren derzeit schwer zu behandeln sind.
Zitation: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Schlüsselwörter: kolorektales Karzinom, Tumormikroumgebung, Nanopartikeltherapie, krebsassoziierte Fibroblasten, Ferroptose