Clear Sky Science · tr
Ferroptozis tabanlı nanoterapi ile immünsüpresif mikroçevrede kolon kanseri ile ilişkili fibroblastların iyileştirilmesi
Bu araştırma kolon kanseri hastaları için neden önemli
Birçok kolorektal kanser hastası, tümörlerinin etrafının sağlam bir destek hücreleri tabakasıyla çevrilmiş ve korunuyor olması nedeniyle günümüzün çığır açan immünoterapilerinden fayda görmüyor. Bu çalışma, özel olarak tasarlanmış manyetik nanoparçacıklar kullanarak bu kalkanı selektif şekilde hedef almanın yeni bir yolunu araştırıyor; böylece tümör bedenin kendi bağışıklık savunmalarına açılırken kanser hücrelerine doğrudan zarar verilmesine de yardımcı olunuyor.
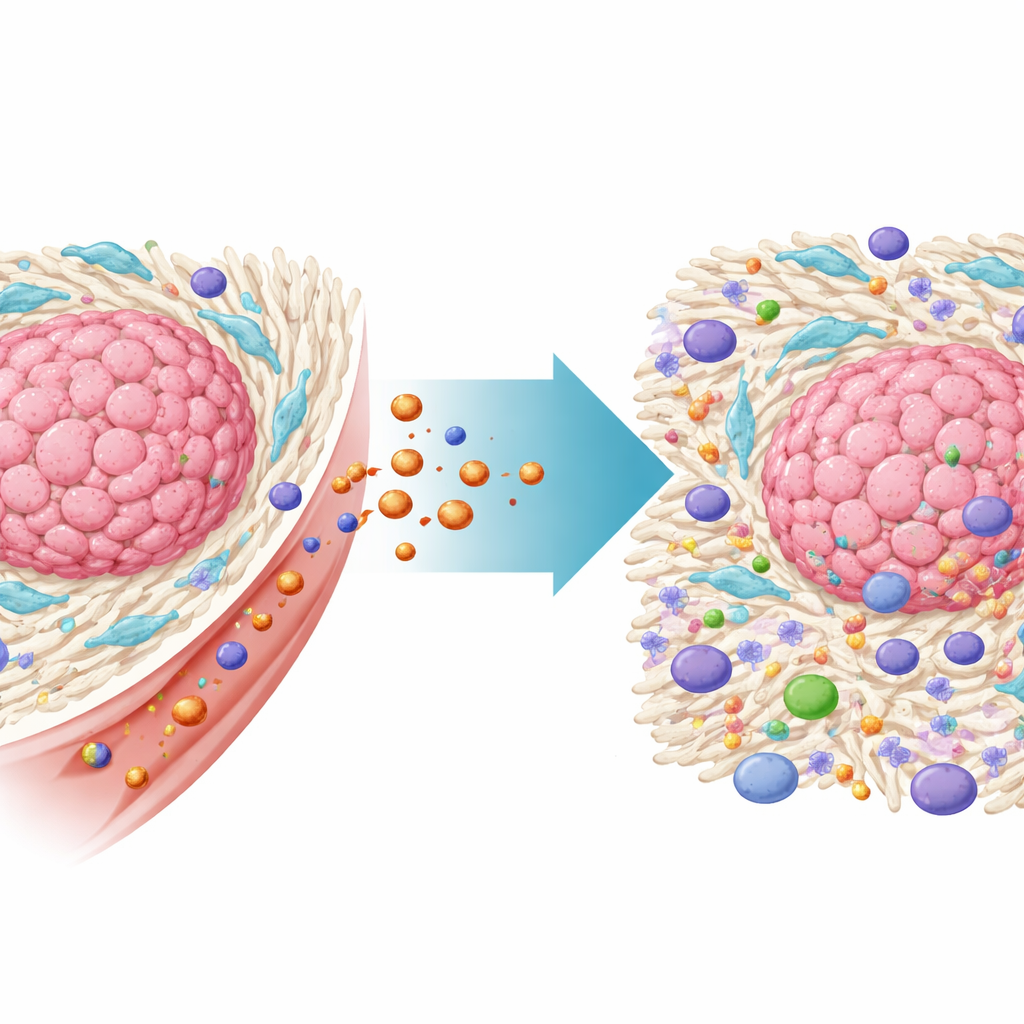
Tümörleri koruyan gizli yardımcılar
Kolorektal tümörler, tümör mikroçevresi olarak adlandırılan kanser olmayan hücrelerden oluşan karmaşık bir mahalle içinde büyür. Bunların en önemlilerinden biri, tümör tarafından ele geçirilen bir tür bağ dokusu hücresi olan kanser ile ilişkili fibroblastlar (CAF'ler)dir. CAF'ler kanserin etrafında yoğun bir ekstraselüler matris iskeleti inşa ederek bağışıklık hücrelerinin ve ilaçların içeri girmesini fiziksel olarak engeller. Ayrıca bağışıklık yanıtlarını zayıflatan ve kanser hücrelerinin tedaviye direnç geliştirmesine yardımcı olan kimyasal sinyaller salarlar. Bu çalışmadaki geniş hasta verileri, CAF bakımından zengin kolorektal kanserlerin daha kötü sağkalım ve immünoterapiye dirençle ilişkili olduğunu doğrulayarak bu hücrelerin doğrudan hedeflenmesi gerekliliğini vurguladı.
Tümörün destek hücrelerine yönelik akıllı bir nanoterapi
Araştırmacılar, özellikle CAF'lere çekici olacak şekilde tasarlanmış çekirdek-kabuk yapılı küçük bakır-demir manyetik nanoparçacıklar geliştirdiler. Bu parçacıkların iki önemli fiziksel özelliği var: yakın kızılötesi lazer ışığını ısıya dönüştürebilmeleri ve hücre içinde toksik oksijen bazlı moleküllerin oluşumunu katalize edebilmeleri. CAF'ler normal fibroblastlara veya birçok tümör hücresine göre daha fazla nanoparçacık alımını doğal olarak gerçekleştirdiğinden, onlar birincil hedef haline geliyor. Ekip ayrıca bazı parçacıkların yüzeyine AS1411 adında kısa DNA-benzeri bir aptamer bağlayarak, nükleolin adı verilen bir proteini hücre dış membranında gösteren fibroblastlara ve tümör hücrelerine parçacıkları daha etkili şekilde yönlendirdi.
Yeni bir hücre ölümü biçimini tetiklemek ve tümör sinyallerini yeniden düzenlemek
Nanoparçacıklar CAF'lerin içine girdikten sonra demir ve bakır iyonları salar. Demir reaktif oksijen türlerinin üretimini beslerken bakır GPX4 adlı koruyucu enzimin düzeylerini düşürür. Bu değişimler bir araya geldiğinde CAF'leri hücre zarlarının kontrolsüz oksidasyonu ile tetiklenen bir hücre ölümü biçimi olan ferroptozise itiyor. Hücre kültürlerinde ve hayvan modellerinde CAF'ler bu sürece normal fibroblastlardan daha hassas çıktı. Aynı zamanda tedavi edilen CAF'ler salgıladıkları kimyasal habercilerin karışımını değiştirdi: normalde tümör büyümesini ve bağışıklık baskısını teşvik eden sinyaller azaldı, bağışıklık hücrelerini çekip aktive etmeye yardımcı olan diğer sinyaller ise arttı. Sonuç olarak, “yeniden programlanmış” fibroblast salgılarına maruz kalan kanser hücreleri büyüme, göç ve invazif özellikler edinme konusunda daha zayıf hale geldi.
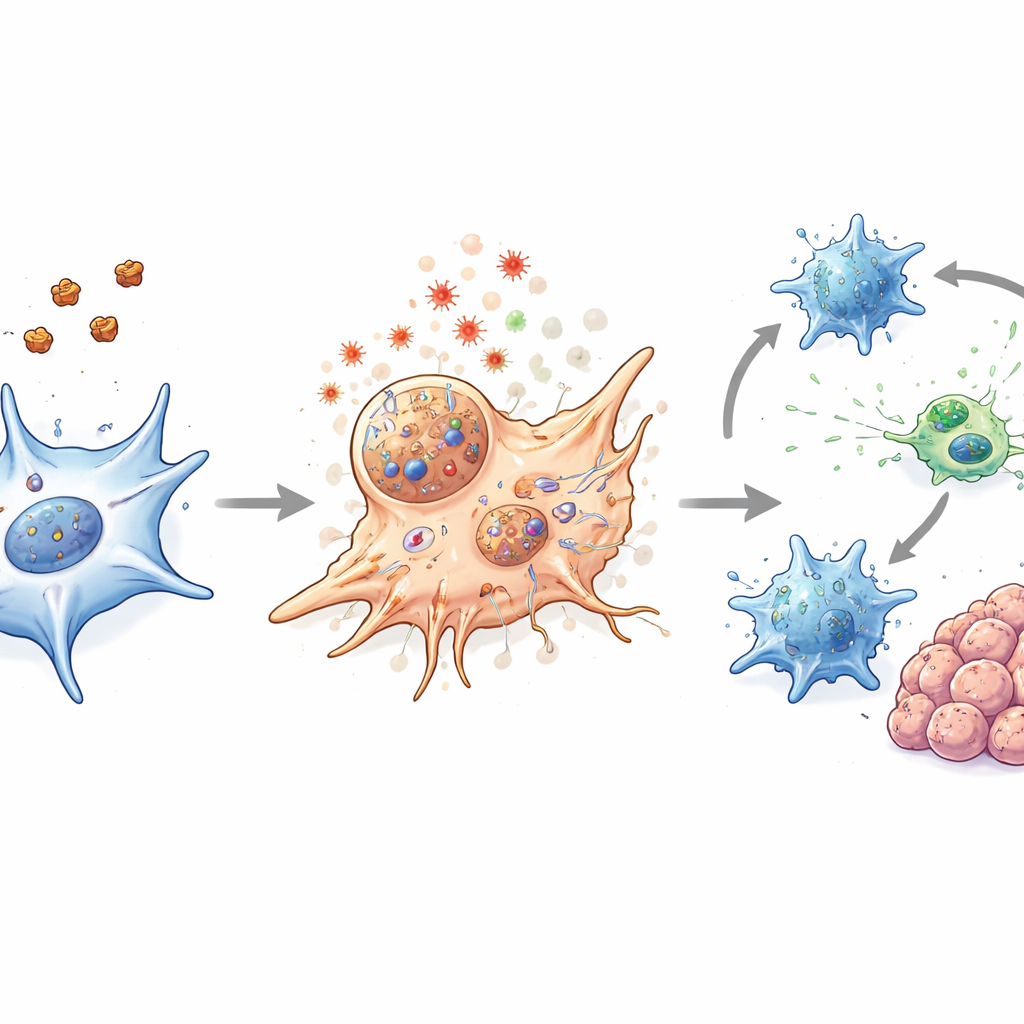
Tümör içindeki bağışıklık sistemini uyandırmak
Standart implante tümörleri içeren fare modelleri, spontan bağırsak tümörleri geliştiren genetik bir model ve hasta kaynaklı tümörler ile organoidleri içeren modellerde nanoparçacık tedavisi tümörleri küçülttü ve bunu güvenli bir şekilde yaptı. Önemli olarak, terapi yalnızca CAF'leri yok etmedi. Ayrıca tümör etrafındaki fiziksel bariyeri gevşetti ve bağışıklık aktivitesini teşvik edecek şekilde yerel kimyayı değiştirdi. Bağışıklık sisteminin bekçileri ve öğretmenleri olarak görev yapan dentritik hücreler tedavi sonrasında daha güçlü olgunlaşma belirtileri gösterdi. Katil CD8 T hücreleri daha aktif hale geldi ve etkili tümör saldırısıyla ilişkili daha fazla molekül üretti; bu, toplam sayıların dramatik biçimde değişmemesine rağmen gözlendi. Nanoparçacıklar nazik lazer ısıtma ile kombine edildiğinde bu etkiler normal dokulara belirgin zarar vermeden daha da güçlendirildi.
Laboratuvar modellerinden gelecekteki tedavilere
Bu yaklaşımın gerçek dünya koşullarında ne kadar genişçe işe yarayabileceğini test etmek için ekip stratejisini hastalardan alınan tümör örnekleri ve mini-tümörler (organoidler) üzerinde uyguladı. Özellikle AS1411 hedefleyici bileşeni taşıyan ve lazer aktivasyonu ile kombine edilen nanoparçacık terapisi, kanserli dokuları ve bunların çevresindeki fibroblastları güçlü biçimde zarar verirken sağlıklı kolon dokurundan yetiştirilen organoidleri büyük ölçüde korudu. Çok sayıda sofistike modelde aynı desen ortaya çıktı: CAF odaklı nanoterapi tümörün koruyucu kabuğunu zayıflattı, yerel bağışıklık yanıtlarını yeniden uyandırdı ve doğrudan kanser hücrelerine zarar verdi.
Geleceğin kanser bakımına ne anlama gelebilir
Çalışma, tümör yardımcılarına saldırmanın tümör hücrelerine saldırmak kadar önemli olabileceğini gösteriyor. Ferroptozis tabanlı manyetik nanoparçacıklar kullanarak kanser ile ilişkili fibroblastları seçici olarak devre dışı bırakan araştırmacılar, kolorektal kanserde hem fiziksel bariyerleri sökebildi hem de bağışıklık sistemi üzerindeki kimyasal frenleri kaldırabildi. Bu çalışma hâlâ preklinik aşamada olsa da hedefe yönelik nanoteknoloji, kontrollü hücre ölümü ve bağışıklık aktivasyonunu birleştiren yeni bir tedavi sınıfına işaret ediyor. Bu tür stratejiler, dirençli kolorektal kanserleri bir gün immünoterapiye daha duyarlı hâle getirip şu anda tedavisi zor olan tümörleri olan hastalar için sonuçları iyileştirebilir.
Atıf: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Anahtar kelimeler: kolorektal kanser, tümör mikroçevresi, nanoparçacık tedavisi, kanser ile ilişkili fibroblastlar, ferroptozis