Clear Sky Science · ru
Смягчение роли фибробластов, ассоциированных с колоректальным раком, в иммуносупрессивной микроокружении с помощью нанотерапии на основе ферроптоза
Почему это исследование важно для пациентов с раком толстой кишки
Многие пациенты с колоректальным раком не получают выгоды от современных прорывных иммунотерапий, поскольку их опухоли окружены и защищены плотным слоем вспомогательных клеток. В этом исследовании рассматривается новый способ прорвать эту защиту с помощью специально разработанных магнитных наночастиц, которые селективно повреждают эти вспомогательные клетки, открывая опухоль для собственных иммунных сил организма и одновременно помогая уничтожать раковые клетки.
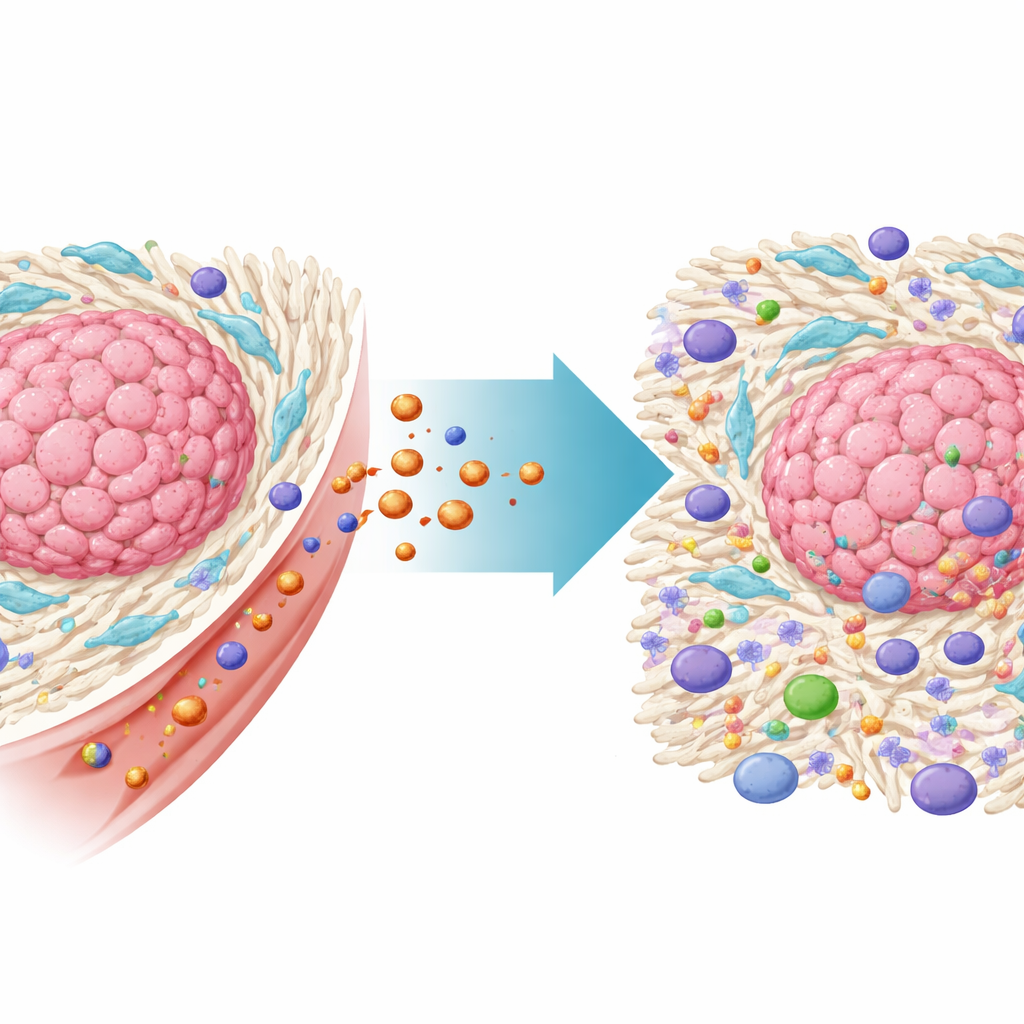
Скрытые помощники, которые защищают опухоль
Колоректальные опухоли развиваются в сложном окружении неклеточных клеток, называемом микроокружением опухоли. Одними из наиболее важных в этом окружении являются фибробласты, ассоциированные с раком (CAF) — тип соединительнотканных клеток, который оказывается скомпрометированным опухолью. CAF строят плотный каркас внеклеточного матрикса вокруг рака, что физически препятствует проникновению иммунных клеток и лекарств. Они также выделяют химические сигналы, ослабляющие иммунные ответы и помогающие раковым клеткам противостоять терапии. Масштабный анализ данных пациентов в этом исследовании подтвердил, что колоректальные раки, богатые CAF, связаны с худшей выживаемостью и сопротивляемостью к иммунотерапии, что подчеркивает необходимость прямого нацеливания на эти клетки.
Разумная нанотерапия, нацеленная на поддерживающие клетки опухоли
Исследователи разработали крошечные магнитные наночастицы из меди и железа с «ядро-оболочка» структурой, специально привлекательные для CAF. Эти частицы обладают двумя ключевыми физическими свойствами: они способны преобразовывать свет в ближнем инфракрасном диапазоне в тепло и катализировать образование токсичных кислородсодержащих молекул внутри клеток. Поскольку CAF естественно поглощают больше наночастиц, чем нормальные фибробласты или многие опухолевые клетки, они становятся основным мишенью. Команда также присоединила к поверхности некоторых частиц короткий ДНК-подобный аптамер AS1411, направляющий их более эффективно к фибробластам и опухолевым клеткам, на внешней мембране которых экспрессируется белок нуклеолин.
Инициация новой формы гибели клеток и перенастройка опухолевых сигналов
Попав в CAF, наночастицы высвобождают ионы железа и меди. Железо стимулирует образование реактивных форм кислорода, тогда как медь снижает уровень защитного фермента GPX4. Вместе эти изменения доводят CAF до ферроптоза — формы гибели клеток, вызванной неконтролируемой окислительной деградацией мембран. В культурах клеток и на животных моделях CAF оказались более уязвимыми к этому процессу по сравнению с нормальными фибробластами. В то же время лечёные CAF изменили набор химических медиаторов, которые они секретируют: сигналы, обычно поддерживающие рост опухоли и иммуносупрессию, были уменьшены, в то время как увеличились сигналы, помогающие привлекать и активировать иммунные клетки. В результате раковые клетки, подвергшиеся воздействию «перепрограммированных» секретов фибробластов, стали менее способными к росту, миграции и приобретению инвазивных свойств.
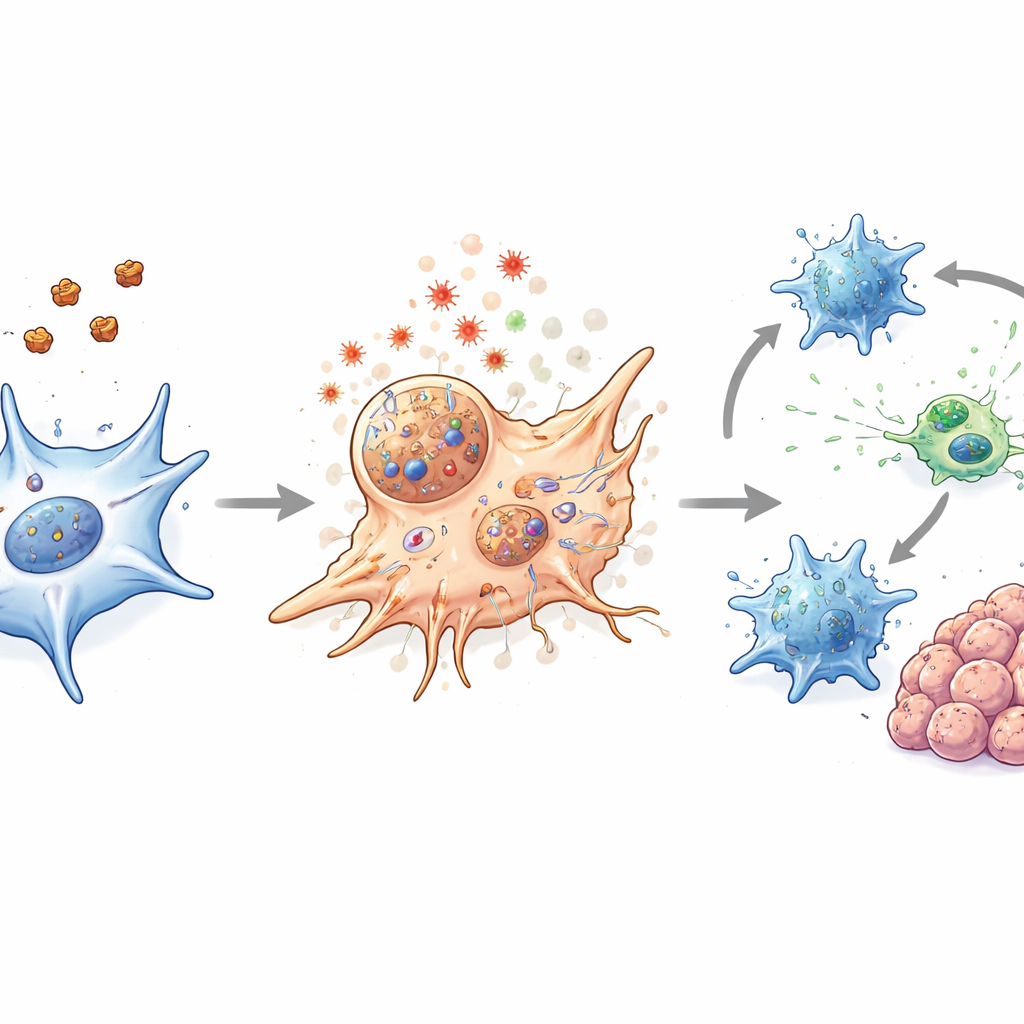
Пробуждение иммунной системы внутри опухоли
На мышиных моделях колоректального рака, включая стандартные имплантированные опухоли, генетическую модель с самопроизвольно развивающимися кишечными опухолями и опухоли и органоиды, полученные от пациентов, лечение наночастицами приводило к сокращению опухолей и было безопасным. Важно, что терапия сделала не только гибель CAF. Она также ослабила физический барьер вокруг опухолей и сместила локальную химию так, что это способствовало иммунной активности. Дендритные клетки, которые выступают в роли «часовых» и «учителей» иммунной системы, проявили признаки повышенной зрелости после лечения. Убийственные CD8+ Т-клетки стали более активными и вырабатывали больше молекул, связанных с эффективной атакой опухоли, хотя их общее число существенно не изменилось. При комбинировании наночастиц с мягким лазерным нагревом эти эффекты усиливались без заметного вреда для нормальных тканей.
От лабораторных моделей к будущим методам лечения
Чтобы проверить, насколько широко может сработать этот подход в реальных условиях, команда применила свою стратегию к образцам опухолей и мини-опухолям (органоидам), выращенным от пациентов. Нанотерапия, особенно версия с направляющим компонентом AS1411 в сочетании с лазерной активацией, сильно повреждала раковые ткани и окружающие их фибробласты, при этом в основном щадя органоиды, выращенные из здоровой ткани толстой кишки. В нескольких сложных моделях наблюдалась одна и та же картина: нанотерапия, ориентированная на CAF, ослабляла защитную оболочку опухоли, пробуждала местные иммунные ответы и напрямую повреждала раковые клетки.
Что это может значить для будущей онкологической помощи
Исследование показывает, что атака на помощников опухоли может быть столь же важной, как и атака на сами опухолевые клетки. Используя магнитные наночастицы, индуцирующие ферроптоз, для селективного нейтрализования фибробластов, ассоциированных с раком, исследователи смогли как разрушить физические барьеры, так и снять химические тормоза иммунной системы при колоректальном раке. Хотя эта работа пока остаётся на доклинической стадии, она указывает на новый класс терапий, сочетающих таргетную нанотехнологию, контролируемую гибель клеток и активацию иммунитета. Такие стратегии однажды могут сделать резистентные формы колоректального рака более отзывчивыми к иммунотерапии и улучшить исходы для пациентов, чьи опухоли в настоящее время трудно поддаются лечению.
Цитирование: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Ключевые слова: колоректальный рак, микроокружение опухоли, наночастичная терапия, фибробласты, ассоциированные с раком, ферроптоз