Clear Sky Science · he
שיפור פיברובלסטים הקשורים לסרטן המעי הגס בסביבה מיקרית מדכאת חיסונית באמצעות ננותרפיה מבוססת פרורפטוזיס
מדוע המחקר הזה חשוב למטופלים בסרטן המעי הגס
מטופלים רבים עם סרטן המעי הגס לא נהנים מההתקדמויות האחרותון של אימונותרפיות, מכיוון שהגידולים שלהם מוקפים ומוגנים על ידי שכבה קשיחה של תאי תמיכה. המחקר בוחן דרך חדשה לשבור את המגן הזה באמצעות ננו-חלקיקים מגנטיים מעוצבים במיוחד שפוגעים באופן בררני בתאי התמיכה הללו, פותחים את הגידול להגנות החיסוניות של הגוף ובמקביל מסייעים להרוג תאי סרטן.
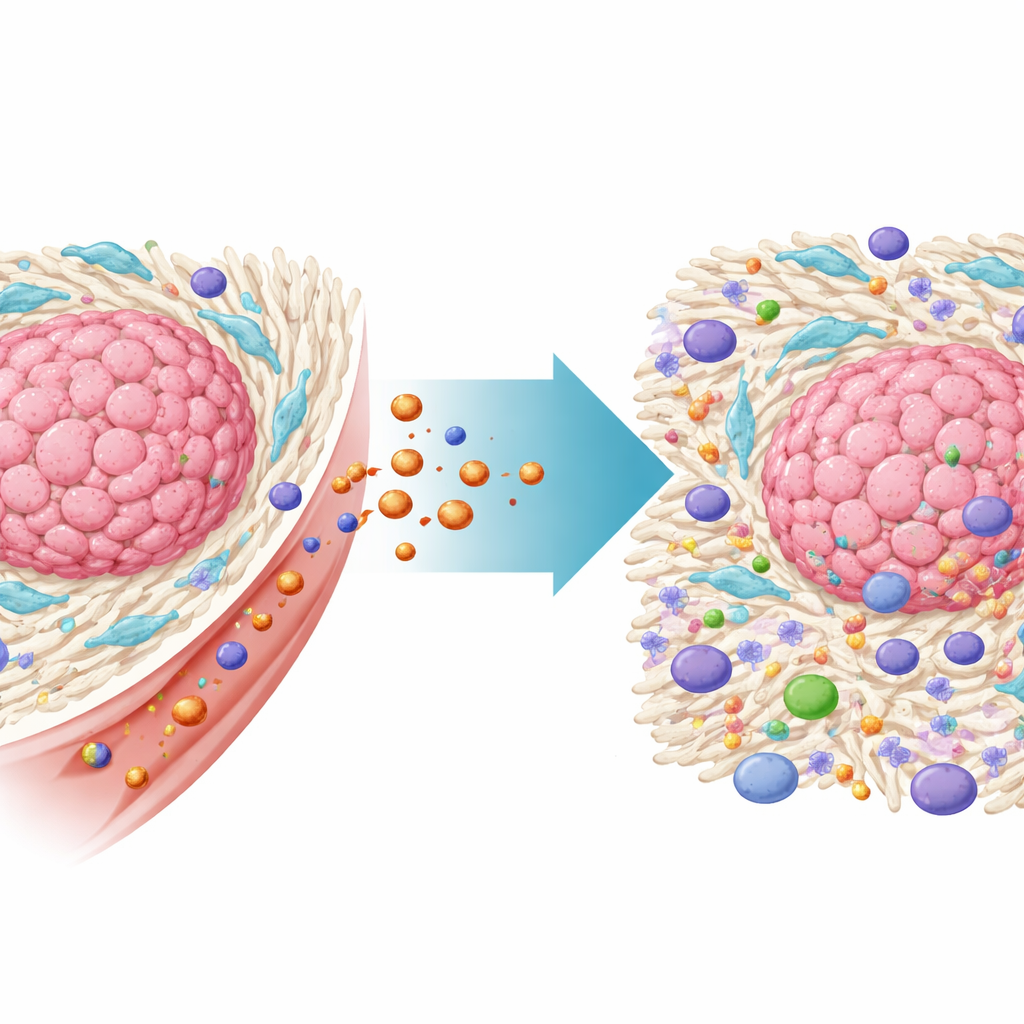
העוזרים הנסתרים שמגנים על הגידולים
גידולי המעי הגס גדלים בתוך סביבה מורכבת של תאים שאינם סרטניים הנקראת המיקרו-סביבה של הגידול. בין החשובים שבהם נמצאים פיברובלסטים מקושרי סרטן, או CAFs, סוג של תאי רקמת חיבור שנחטפים לטובת הגידול. CAFs בונים תפרחת צפופה של מטריקס חוץ-תאי סביב הסרטן, שמחסום פיזי מונע היכנסות של תאי חיסון ותרופות. הם גם משחררים אותות כימיים שמחלישים תגובות חיסוניות ועוזרים לתאי הסרטן לעמוד בטיפול. נתוני מטופלים בקנה מידה רחב במחקר זה איששו כי סרטן מעי גס עשיר ב-CAFs נקשר להישרדות נמוכה יותר ולעמידות לאימונותרפיה, מה שמדגיש את הצורך לטרגט תאים אלה באופן ישיר.
ננותרפיה חכמה המכוונת לתאי התמיכה של הגידול
החוקרים פיתחו ננו-חלקיקים מגנטיים מנחושת–ברזל זעירים במבנה ליבה-קליפה שנועדו להיות מושכים במיוחד ל-CAFs. לחלקיקים הללו שתי תכונות פיזיות מרכזיות: הם יכולים להמיר אור לייזר בתחום הקרוב לתת-אדום לחום, והם יכולים לזרז יצירה של מולקולות חמצן רעילות בתוך תאים. מכיוון ש-CAFs סופגים בטבעיות כמות גדולה יותר של ננו-חלקיקים מאשר פיברובלסטים נורמליים או רבים מתאים סרטניים, הם הופכים למטרה הראשית. הצוות גם חיבר לאזור החיצוני של חלק מהחלקיקים אפרמר (aptamer) קצר דמוי DNA בשם AS1411, שמכוון אותם ביעילות רבה יותר לפיברובלסטים ולתאי גידול המציגים חלבון בשם נוקלאולין על ממברנתם החיצונית.
הפעלת צורת מוות תאית חדשה וחידוש אותות הגידול
לאחר שנכנסים ל-CAFs, משחררים הננו-חלקיקים יוני ברזל ונחושת. הברזל דוחף את ייצור המינים החמצוניים הפעילים, בעוד הנחושת מורידה את רמות האנזים המגן GPX4. יחד, שינויים אלה דוחפים את ה-CAFs לפרורפטוזיס, צורת מוות תאית הנגרמת על ידי חמצון בלתי נשלט של ממברנות התא. במערכות תרבית ומודלי בעלי חיים, ה-CAFs היו פגיעים יותר לתהליך זה מאשר פיברובלסטים רגילים. במקביל, ה-CAFs שטופלו שינו את תערובת המולקולות הכימיות שהפרישו: אותות שבעבר עודדו גדילה של הגידול ודיכוי חיסוני הופחתו, בעוד שאחרים המסייעים לגיוס ולהפעלה של תאי חיסון עלו. כתוצאה מכך, תאי סרטן שנחשפו להפרשות ה"מופרמרות" של הפיברובלסטים הפכו לפחות מסוגלים לגדול, להגר ולהפגין תכונות פולשניות.
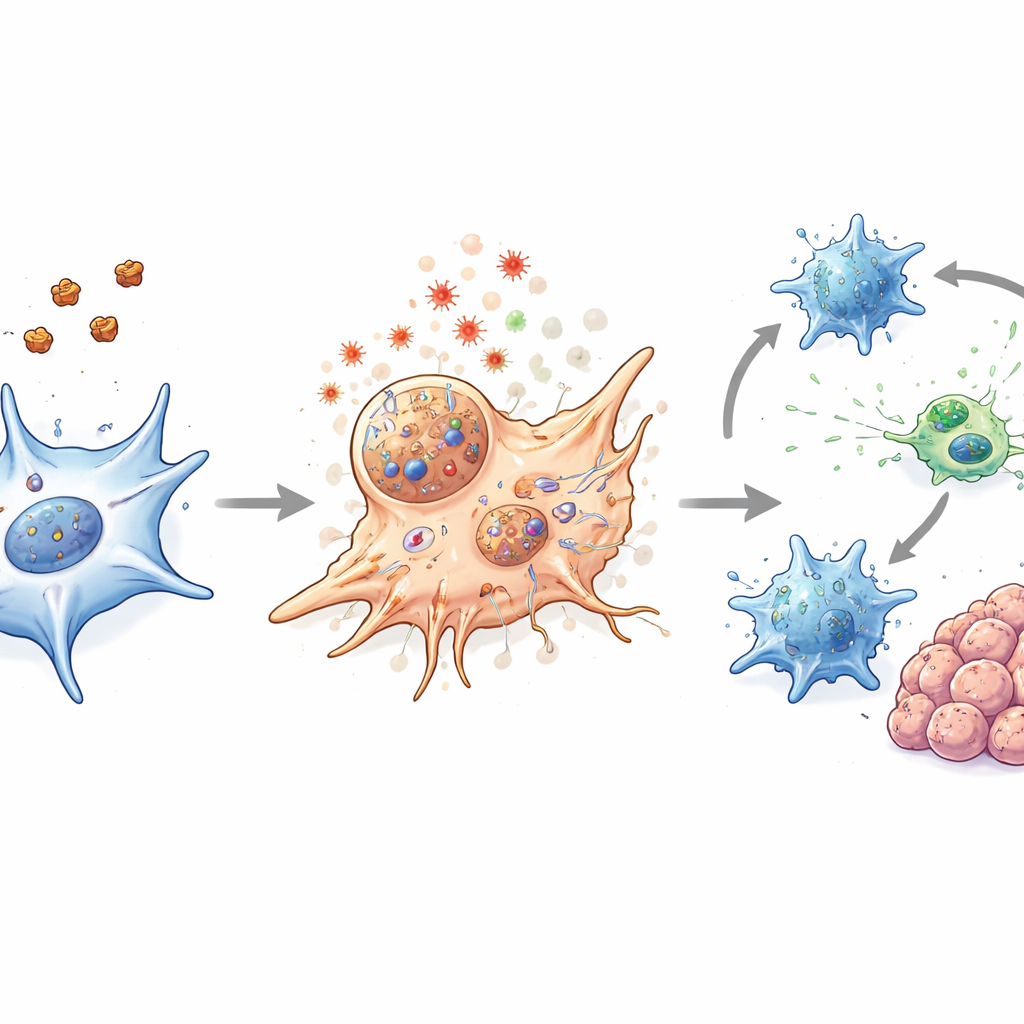
עירור מערכת החיסון בתוך הגידול
במודלים של עכברים עם סרטן המעי הגס, כולל גידולים מושתלים סטנדרטיים, מודל גנטי המפתח גידולים מעיים ספונטניים, וגידולים ואורגנואידים שמקורם בחולים, הטיפול בננו-חלקיקים כיווץ את הגידולים ובוצע בבטיחות. החשוב מכך, הטיפול עשה יותר מסתם להרוג CAFs. הוא גם ריכך את המחסום הפיזי סביב הגידולים ושינה את הכימיה המקומית באופן שעמד לעידוד פעילות חיסונית. תאי דנדריטיים, המשמשים כמשגיחים ומלמדים של מערכת החיסון, הראו סימנים חזקים יותר של הבשלה לאחר הטיפול. תאי T CD8 קוטלי-מטרה הפכו פעילים יותר וייצרו יותר מולקולות הקשורות להתקפה אפקטיבית על הגידול, אף שמספרם הכולל לא השתנה בצורה דרמטית. כאשר שילבו את הננו-חלקיקים עם חימום עדין באמצעות לייזר, השפעות אלה הוגברו ללא נזק ניכר לרקמות בריאות.
מלבד מודלים מעבדתיים לכיוון טיפולים עתידיים
כדי לבדוק עד כמה שיטה זו עשויה לעבוד בהקשרים בעולם האמיתי, הצוות יישם את האסטרטגיה על דגימות גידול ואורגנואידים שגודלו ממטופלים. הננותרפיה, ובמיוחד הגרסה הנושאת את רכיב המיקוד AS1411 ושילוב עם הפעלת לייזר, פגעה בעוצמה ברקמות סרטניות ובפיברובלסטים שסביבן בעוד שבעיקר חיסרה אורגנואידים שגודלו מרקמה קולונית בריאה. במגוון מודלים מורכבים, הופיעה אותה תבנית: ננותרפיה ממוקדת ב-CAF החלישה את הקליפה המגוננת של הגידול, העירתה תגובות חיסוניות מקומיות ופגעה ישירות בתאי הסרטן.
מה זה עשוי להצביע על טיפול עתידי בסרטן
המחקר מציע כי התקפה על עוזרי הגידול יכולה להיות חשובה לא פחות מהתקפה על תאי הגידול עצמם. באמצעות ננו-חלקיקים מגנטיים המבוססים על פרורפטוזיס כדי להשבית באופן סלקטיבי פיברובלסטים מקושרי סרטן, הצליחו החוקרים לפרק מחסומים פיזיים ולהרים בלמי כימיה על המערכת החיסונית בסרטן המעי הגס. אמנם עבודה זו נמצאת עדיין בשלב טרום-קליני, אך היא מצביעה על כיוון טיפולים חדש המשלב ננוטכנולוגיה ממוקדת, מוות תאי מבוקר והפעלת חיסון. אסטרטגיות כאלה עשויות יום אחד להפוך סרטןי מעי גס עמידים ליותר רגישים לאימונותרפיה ולשפר תוצאות למטופלים שהגידולים שלהם קשים לטיפול כיום.
ציטוט: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
מילות מפתח: סרטן המעי הגס, סביבה מיקרית של גידול, תרפיה באמצעות ננו-חלקיקים, פיברובלסטים מקושרי סרטן, פרורפטוזיס