Clear Sky Science · es
Mejora de los fibroblastos asociados al cáncer colorrectal en un microambiente inmunosupresor mediante nanoterapia basada en ferroptosis
Por qué esta investigación importa para pacientes con cáncer de colon
Muchas personas con cáncer colorrectal no se benefician de las inmunoterapias revolucionarias actuales porque sus tumores están rodeados y protegidos por una capa resistente de células de soporte. Este estudio explora una nueva forma de romper ese escudo usando nanopartículas magnéticas especialmente diseñadas que dañan selectivamente estas células de soporte, abriendo el tumor a las defensas inmunitarias del propio organismo y ayudando al mismo tiempo a eliminar las células cancerosas.
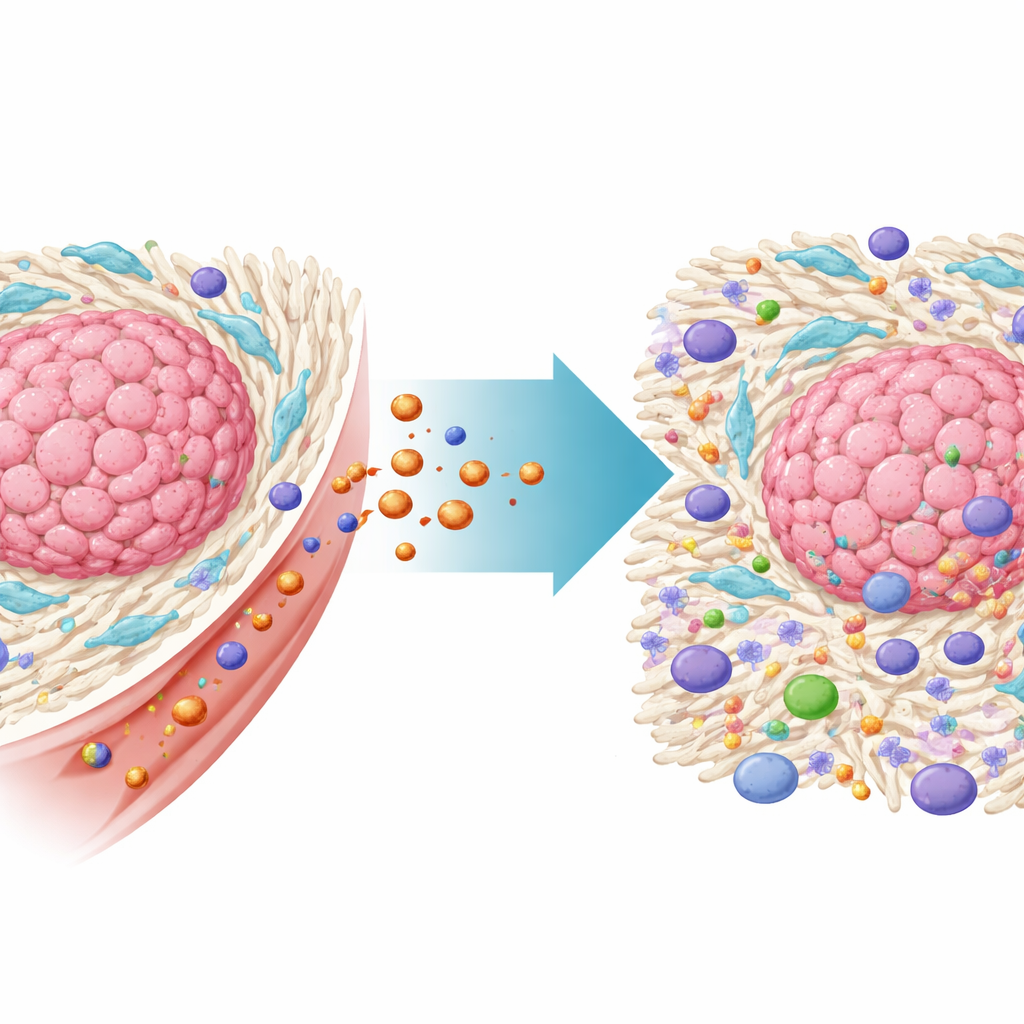
Los colaboradores ocultos que protegen a los tumores
Los tumores colorrectales crecen dentro de un vecindario complejo de células no cancerosas llamado microambiente tumoral. Entre las más importantes están los fibroblastos asociados al cáncer, o CAFs, un tipo de célula del tejido conectivo que es cooptada por el tumor. Los CAFs construyen un andamiaje denso de matriz extracelular alrededor del cáncer, que bloquea físicamente la entrada de células inmunitarias y fármacos. También liberan señales químicas que debilitan las respuestas inmunitarias y ayudan a las células cancerosas a resistir las terapias. Datos a gran escala de pacientes en este estudio confirmaron que los cánceres colorrectales ricos en CAFs se asociaban con una supervivencia peor y con resistencia a la inmunoterapia, subrayando la necesidad de dirigir estas células de forma directa.
Una nanoterapia inteligente dirigida a las células de soporte del tumor
Los investigadores desarrollaron diminutas nanopartículas magnéticas de cobre y hierro con una estructura núcleo–capa diseñadas para ser especialmente atractivas para los CAFs. Estas partículas tienen dos propiedades físicas clave: pueden convertir la luz láser del infrarrojo cercano en calor y pueden catalizar la formación de moléculas toxicas a base de oxígeno dentro de las células. Dado que los CAFs absorben naturalmente más nanopartículas que los fibroblastos normales o muchas células tumorales, se convierten en el objetivo principal. El equipo también añadió un aptámero corto similar al ADN llamado AS1411 en la superficie de algunas partículas, guiándolas con mayor eficiencia hacia fibroblastos y células tumorales que muestran una proteína llamada nucleolina en su membrana externa.
Inducir una nueva forma de muerte celular y reprogramar las señales tumorales
Una vez dentro de los CAFs, las nanopartículas liberan iones de hierro y cobre. El hierro alimenta la producción de especies reactivas de oxígeno, mientras que el cobre reduce los niveles de una enzima protectora llamada GPX4. Juntos, estos cambios llevan a los CAFs a la ferroptosis, una forma de muerte celular impulsada por la oxidación incontrolada de las membranas celulares. En cultivos y modelos animales, los CAFs resultaron más vulnerables a este proceso que los fibroblastos normales. Al mismo tiempo, los CAFs tratados modificaron la mezcla de mensajeros químicos que secretan: se redujeron señales que normalmente fomentan el crecimiento tumoral y la supresión inmune, mientras que aumentaron otras que ayudan a reclutar y activar células inmunitarias. Como resultado, las células cancerosas expuestas a las secreciones de los fibroblastos “reprogramados” mostraron menor capacidad para crecer, migrar y adoptar rasgos invasivos.
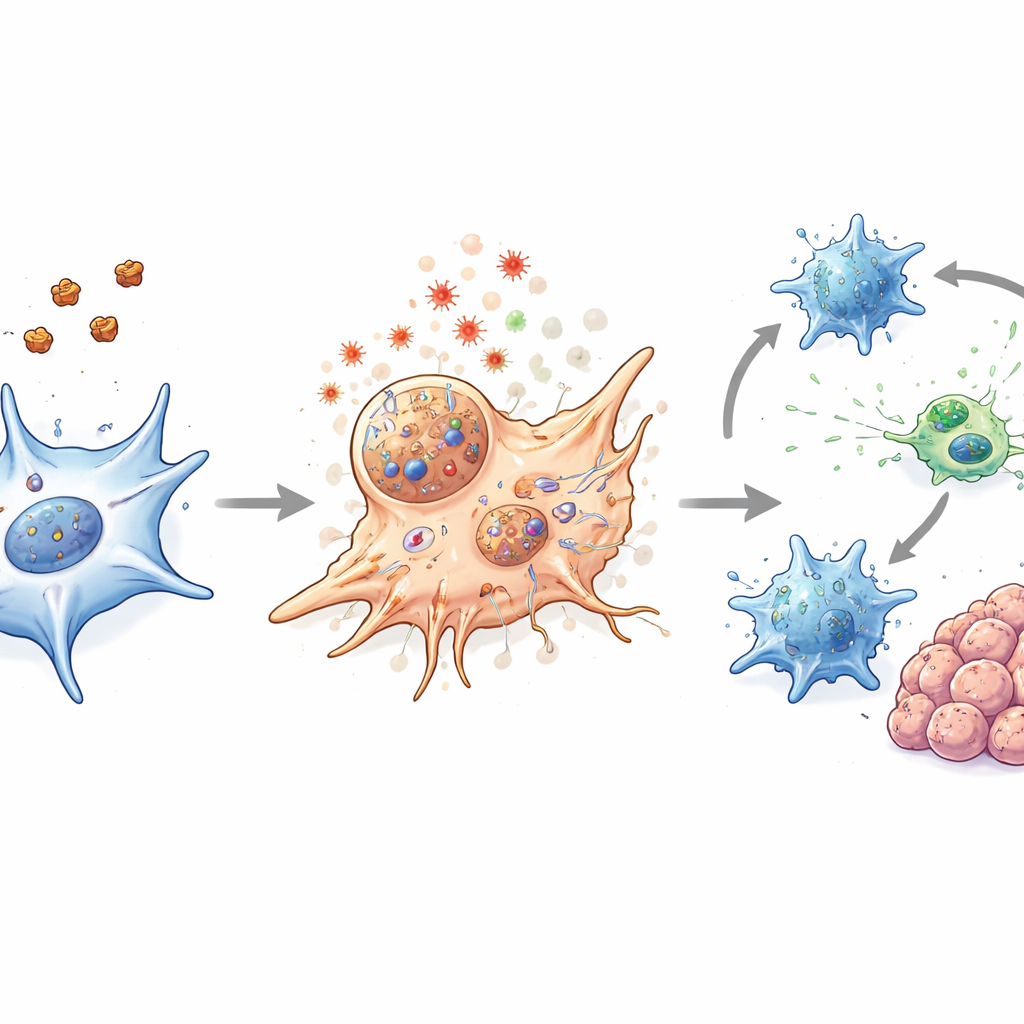
Despertando al sistema inmunitario dentro del tumor
En modelos murinos de cáncer colorrectal, incluidos tumores implantados estándar, un modelo genético que desarrolla tumores intestinales espontáneos y tumores y organoides derivados de pacientes, el tratamiento con nanopartículas redujo los tumores y lo hizo de forma segura. Importante: la terapia hizo más que solo matar CAFs. También aflojó la barrera física alrededor de los tumores y cambió la química local de modo que fomentó la actividad inmune. Las células dendríticas, que actúan como centinelas y formadoras del sistema inmune, mostraron signos más fuertes de maduración tras el tratamiento. Las células T CD8 citotóxicas se volvieron más activas y produjeron más moléculas asociadas con un ataque tumoral eficaz, aunque su número total no cambió de forma dramática. Cuando las nanopartículas se combinaron con calentamiento láser suave, estos efectos se amplificaron sin daño apreciable a los tejidos normales.
De los modelos de laboratorio hacia futuros tratamientos
Para evaluar cuán amplia podría ser esta estrategia en escenarios del mundo real, el equipo aplicó su enfoque a muestras tumorales y mini-tumores (organoides) cultivados a partir de pacientes. La nanoterapia, especialmente la versión que llevaba el componente de orientación AS1411 y combinada con activación láser, dañó fuertemente los tejidos cancerosos y sus fibroblastos circundantes mientras preservaba en gran medida los organoides derivados de tejido sano de colon. A través de múltiples modelos sofisticados, surgió el mismo patrón: la nanoterapia centrada en CAFs debilitó la coraza protectora del tumor, reavivó respuestas inmunitarias locales y lesionó directamente las células cancerosas.
Lo que esto podría significar para la atención oncológica futura
El estudio sugiere que atacar a los colaboradores del tumor puede ser tan importante como atacar a las propias células tumorales. Al usar nanopartículas magnéticas basadas en ferroptosis para desactivar selectivamente a los fibroblastos asociados al cáncer, los investigadores pudieron tanto desmantelar barreras físicas como levantar frenos químicos sobre el sistema inmunitario en el cáncer colorrectal. Aunque este trabajo aún se encuentra en fase preclínica, apunta hacia una nueva clase de tratamientos que combinan nanotecnología dirigida, muerte celular controlada y activación inmune. Tales estrategias podrían, algún día, hacer que los cánceres colorrectales resistentes sean más sensibles a la inmunoterapia y mejorar los resultados para pacientes cuyos tumores hoy son difíciles de tratar.
Cita: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Palabras clave: cáncer colorrectal, microambiente tumoral, terapia con nanopartículas, fibroblastos asociados al cáncer, ferroptosis