Clear Sky Science · ar
تحسين الخلايا الليفية المرتبطة بسرطان القولون والمستقيم في بيئة مكبوتة مناعياً بواسطة علاج نانوي قائم على الفيروبتوسيس
لماذا يهم هذا البحث مرضى سرطان القولون
العديد من المصابين بسرطان القولون والمستقيم لا يستفيدون من علاجات المناعة الثورية الحالية لأن أورامهم محاطة ومحمية بطبقة متينة من خلايا الدعم. تستكشف هذه الدراسة طريقة جديدة لاختراق ذلك الدرع باستخدام جسيمات مغناطيسية نانوية مصممة خصيصاً لتلحق الضرر بتلك الخلايا الداعمة بشكل انتقائي، فتفتح الورم أمام دفاعات الجسم المناعية وتساعد في الوقت نفسه على قتل الخلايا السرطانية.
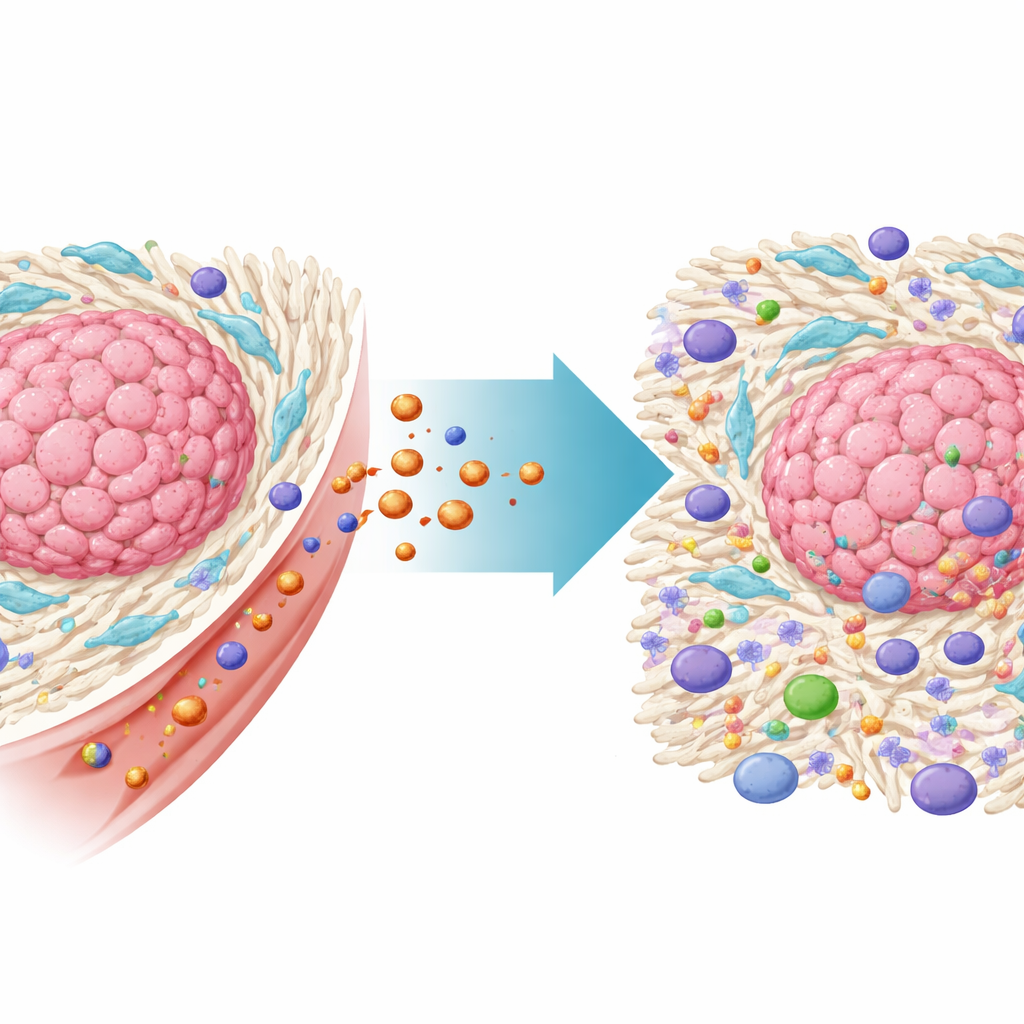
المساعدون الخفيون الذين يدرعون الأورام
تنمو أورام القولون والمستقيم داخل حي معقد من الخلايا غير السرطانية يُسمى البيئة الميكروية للورم. ومن أهم هذه الخلايا الخلايا الليفية المرتبطة بالسرطان أو CAFs، وهي نوع من خلايا النسيج الضام التي يستغلها الورم. تبني CAFs هيكلاً كثيفاً من المصفوفة خارج الخلوية حول السرطان، ما يمنع دخول الخلايا المناعية والأدوية من الناحية الفيزيائية. كما تُفرز إشارات كيميائية تضعف الاستجابات المناعية وتساعد الخلايا السرطانية على مقاومة العلاج. أكدت بيانات المرضى واسعة النطاق في هذه الدراسة أن سرطانات القولون والمستقيم الغنية بـ CAFs كانت مرتبطة ببقاء أقل ومقاومة للعلاج المناعي، مما يبرز الحاجة لاستهداف هذه الخلايا مباشرة.
علاج نانوي ذكي موجه إلى خلايا دعم الورم
طور الباحثون جسيمات نانوية مغناطيسية صغيرة من النحاس والحديد ذات بنية قلب-غلاف مصممة لتكون جذابة بشكل خاص لـ CAFs. تتمتع هذه الجسيمات بخاصيتين فيزائيتين رئيسيتين: يمكنها تحويل ضوء الليزر القريب من تحت الحمراء إلى حرارة، ويمكنها تحفيز تكوّن جزيئات أكسجين سامة داخل الخلايا. لأن CAFs تمتص الجسيمات النانوية طبيعياً أكثر من الخلايا الليفية الطبيعية أو العديد من خلايا الورم، تصبح هي الهدف الأساسي. كما أرفق الفريق أبتمر قصير شبيه بالحمض النووي يُدعى AS1411 على سطح بعض الجسيمات لتوجيهها بكفاءة أكبر نحو الخلايا الليفية وخلايا الورم التي تُظهر بروتيناً يُدعى نوكلولين على غشائها الخارجي.
إطلاق شكل جديد من موت الخلايا وإعادة توصيل إشارات الورم
بمجرد دخولها إلى CAFs، تطلق الجسيمات أيونات الحديد والنحاس. يمد الحديد إنتاج أنواع الأكسجين التفاعلية، بينما يخفض النحاس مستويات إنزيم واقٍ يُدعى GPX4. معاً، تدفع هذه التغييرات CAFs نحو الفيروبتوسيس، وهو شكل من الموت الخلوي ناتج عن أكسدة غير مضبوطة لأغشية الخلايا. في التجارب المخبرية ونماذج الحيوان، أظهرت CAFs قابلية أكبر لهذا العملية مقارنة بالخلايا الليفية الطبيعية. وفي الوقت نفسه، غيرت CAFs المعالجة مزيج المرسلات الكيميائية التي تفرزها: انخفضت الإشارات التي تشجع عادة نمو الورم وكبت المناعة، بينما زادت إشارات أخرى تساعد على استقطاب وتنشيط الخلايا المناعية. ونتيجة لذلك، أصبحت الخلايا السرطانية المعرضة لإفرازات الخلايا الليفية “المعاد برمجتها” أقل قدرة على النمو والهجرة وامتلاك صفات غازية.
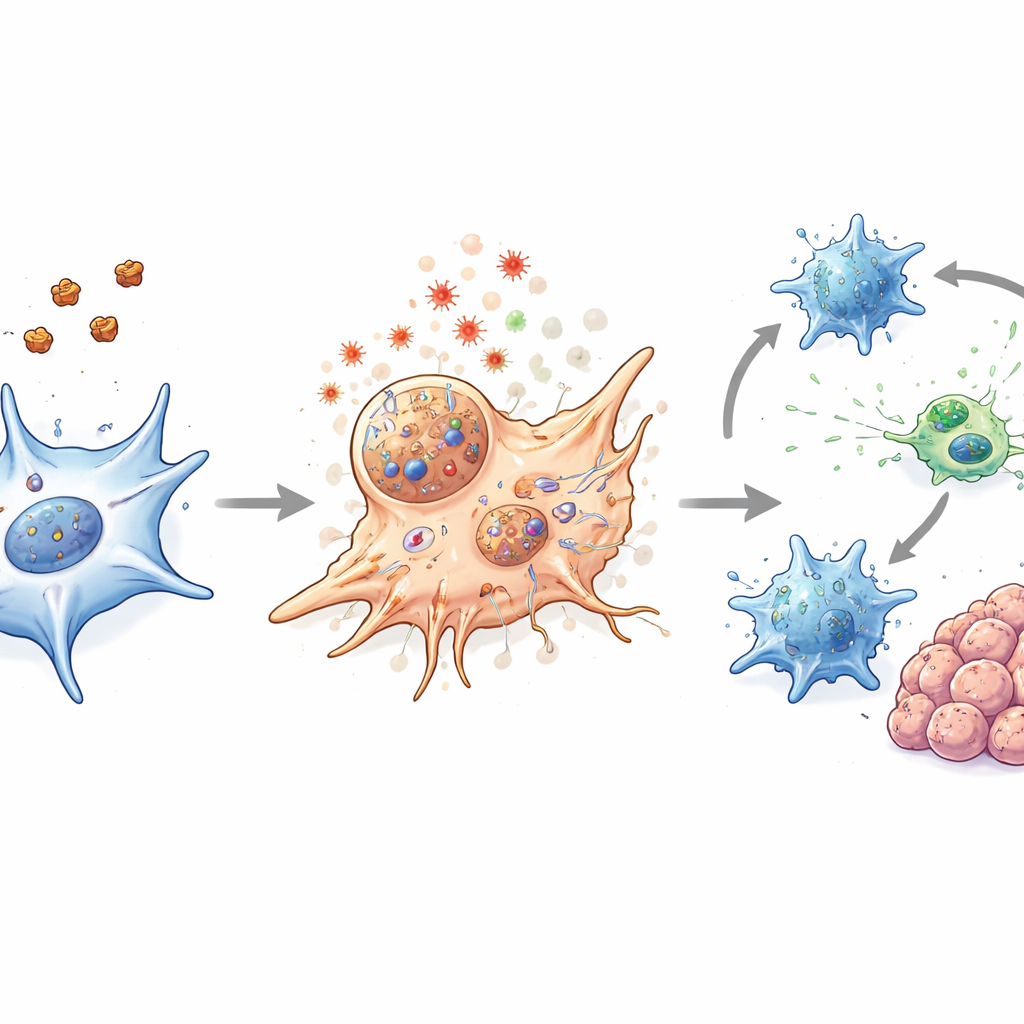
إيقاظ الجهاز المناعي داخل الورم
في نماذج الفئران لسرطان القولون والمستقيم، بما في ذلك الأورام المزروعة التقليدية، ونموذج جيني يُطور أوراماً معوية عفوية، وأورام مشتقة من مرضى وزرعيات أعضاء صغيرة، قلّص العلاج بالجسيمات النانوية حجم الأورام وفعل ذلك بأمان. والأهم أن العلاج لم يقتصر على قتل CAFs فحسب؛ بل أرخى أيضاً الحاجز الفيزيائي حول الأورام وغير الكيمياء المحلية بطريقة شجعت النشاط المناعي. أظهرت الخلايا التغصنية، التي تعمل كحرس ومعلمين للجهاز المناعي، علامات أقوى على النضج بعد العلاج. أصبحت خلايا CD8 القاتلة أكثر نشاطاً وأنتجت مزيداً من الجزيئات المرتبطة بهجوم فعال على الورم، رغم أن أعدادها الإجمالية لم تتغير بشكل كبير. وعند الجمع بين الجسيمات النانوية والتسخين الليزري اللطيف، تضاعفت هذه التأثيرات دون أذى ملحوظ للأنسجة الطبيعية.
من النماذج المخبرية نحو العلاجات المستقبلية
لاختبار مدى قابلية هذه الاستراتيجية للتطبيق في مواقف واقعية، طبّق الفريق نهجه على عينات أورام وزرعيات صغيرة (أورجانويدات) نمت من مرضى. ألحق العلاج بالجسيمات النانوية، خصوصاً النسخة المحمّلة بعامل الاستهداف AS1411 والمُفعَّلة بالليزر، أضراراً كبيرة بالأنسجة السرطانية وخلاياها الليفية المحيطة بينما حفظت إلى حد كبير الأورجانويدات النامية من نسيج القولون الصحي. عبر نماذج متقدمة متعددة، ظهر النمط نفسه: العلاج النانوي الموجه لـ CAF أضعف الدرع الحامي للورم، أيقظ الاستجابات المناعية المحلية، وأصاب الخلايا السرطانية مباشرة.
ما الذي قد يعنيه هذا لرعاية السرطان في المستقبل
تقترح الدراسة أن مهاجمة مساعدي الورم قد تكون مهمة بقدر مهاجمة الخلايا الورمية نفسها. باستخدام جسيمات نانوية مغناطيسية قائمة على الفيروبتوسيس لتعطيل الخلايا الليفية المرتبطة بالسرطان بشكل انتقائي، تمكن الباحثون من تفكيك الحواجز الفيزيائية ورفع المكابح الكيميائية عن الجهاز المناعي في سرطان القولون والمستقيم. ومع أن هذا العمل لا يزال في مرحلة ما قبل السريرية، فإنه يشير إلى فئة جديدة من العلاجات التي تجمع بين تقنيات النانو المستهدفة، والموت الخلوي المتحكم به، وتنشيط المناعة. قد تجعل مثل هذه الاستراتيجيات يوماً ما سرطانات القولون المقاومة أكثر استجابة للعلاج المناعي وتحسن نتائج المرضى الذين يصعب علاج أورامهم حالياً.
الاستشهاد: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
الكلمات المفتاحية: سرطان القولون والمستقيم, البيئة الميكروية للورم, علاج بجسيمات نانوية, الخلايا الليفية المرتبطة بالسرطان, الفيروبتوسيس