Clear Sky Science · fr
Amélioration des fibroblastes associés au cancer colorectal dans un microenvironnement immunosuppresseur par une nanothérapie à base de ferroptose
Pourquoi cette recherche importe pour les patients atteints de cancer du côlon
Beaucoup de personnes atteintes de cancer colorectal ne bénéficient pas des immunothérapies révolutionnaires actuelles parce que leurs tumeurs sont entourées et protégées par une couche résistante de cellules de soutien. Cette étude explore une nouvelle façon de percer ce bouclier en utilisant des nanoparticules magnétiques spécialement conçues qui endommagent sélectivement ces cellules de soutien, ouvrant la tumeur aux défenses immunitaires de l’organisme tout en contribuant à éliminer les cellules cancéreuses.
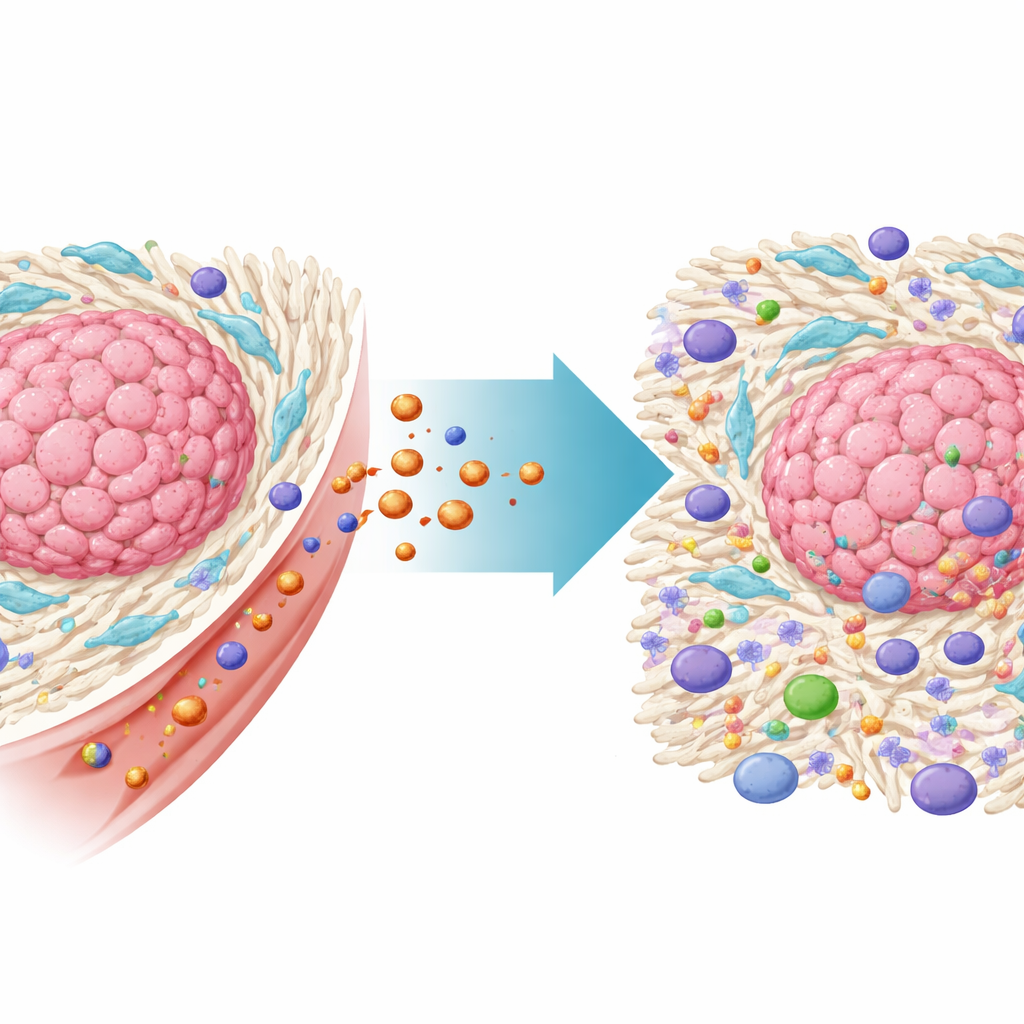
Les auxiliaires cachés qui protègent les tumeurs
Les tumeurs colorectales se développent au sein d’un voisinage complexe de cellules non cancéreuses appelé microenvironnement tumoral. Parmi les plus importantes figurent les fibroblastes associés au cancer, ou FAC, un type de cellule du tissu conjonctif qui est détourné par la tumeur. Les FAC construisent un échafaudage dense de matrice extracellulaire autour du cancer, ce qui empêche physiquement les cellules immunitaires et les médicaments de pénétrer. Elles libèrent aussi des signaux chimiques qui affaiblissent les réponses immunitaires et aident les cellules cancéreuses à résister aux traitements. Des données issues d’un large cohort de patients dans cette étude ont confirmé que les cancers colorectaux riches en FAC étaient associés à une survie moindre et à une résistance à l’immunothérapie, soulignant la nécessité de cibler directement ces cellules.
Une nanothérapie intelligente ciblant les cellules de soutien de la tumeur
Les chercheurs ont développé de petites nanoparticules magnétiques cuivre–fer avec une structure cœur-coquille conçue pour être particulièrement attractives pour les FAC. Ces particules possèdent deux propriétés physiques clés : elles peuvent convertir la lumière laser proche infrarouge en chaleur, et elles peuvent catalyser la formation de molécules oxygénées toxiques à l’intérieur des cellules. Parce que les FAC accumulent naturellement plus de nanoparticules que les fibroblastes normaux ou de nombreuses cellules tumorales, elles deviennent la cible principale. L’équipe a aussi greffé à la surface de certaines particules un aptamère court de type ADN appelé AS1411, les guidant plus efficacement vers les fibroblastes et les cellules tumorales qui expriment une protéine nommée nucléoiline à leur membrane externe.
Déclencher une nouvelle forme de mort cellulaire et reprogrammer les signaux tumoraux
Une fois à l’intérieur des FAC, les nanoparticules libèrent des ions fer et cuivre. Le fer alimente la production d’espèces réactives de l’oxygène, tandis que le cuivre abaisse les niveaux d’une enzyme protectrice appelée GPX4. Ensemble, ces changements poussent les FAC vers la ferroptose, une forme de mort cellulaire provoquée par une oxydation incontrôlée des membranes cellulaires. En culture et dans des modèles animaux, les FAC se sont révélées plus vulnérables à ce processus que les fibroblastes normaux. Parallèlement, les FAC traitées ont modifié la composition des messagers chimiques qu’elles sécrètent : les signaux qui favorisent habituellement la croissance tumorale et l’immunosuppression ont été réduits, tandis que d’autres aidant au recrutement et à l’activation des cellules immunitaires ont augmenté. En conséquence, les cellules cancéreuses exposées aux sécrétions « reprogrammées » des fibroblastes ont montré une capacité moindre à proliférer, migrer et adopter des traits invasifs.
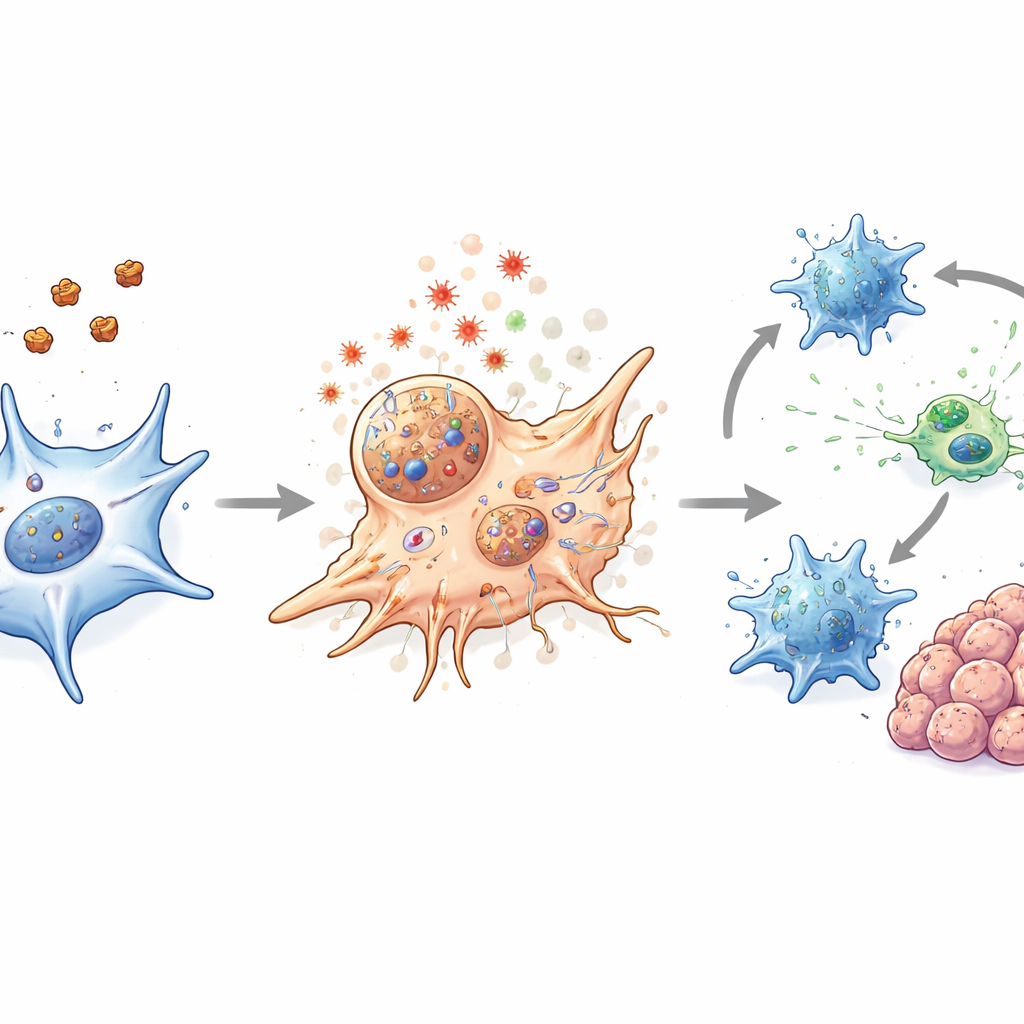
Réveiller le système immunitaire à l’intérieur de la tumeur
Dans des modèles murins de cancer colorectal, incluant des tumeurs implantées standards, un modèle génétique développant des tumeurs intestinales spontanées, et des tumeurs et organoïdes dérivés de patients, le traitement par nanoparticules a réduit la taille des tumeurs tout en s’avérant sûr. Il est important de noter que la thérapie n’a pas seulement tué les FAC. Elle a aussi assoupli la barrière physique autour des tumeurs et modifié la chimie locale de façon à favoriser l’activité immunitaire. Les cellules dendritiques, qui jouent le rôle de sentinelles et de formatrices du système immunitaire, ont montré des signes accrus de maturation après le traitement. Les lymphocytes T CD8 tueurs sont devenus plus actifs et ont produit davantage de molécules associées à une attaque tumorale efficace, même si leur nombre global n’a pas changé de façon spectaculaire. Lorsque les nanoparticules ont été combinées à un réchauffement laser doux, ces effets ont été amplifiés sans dommages notables aux tissus sains.
Des modèles de laboratoire vers de futurs traitements
Pour évaluer l’applicabilité de cette approche dans des contextes réels, l’équipe a appliqué sa stratégie à des échantillons tumoraux et à des mini-tumeurs (organoïdes) dérivés de patients. La nanothérapie, en particulier la version munie du composant de ciblage AS1411 et combinée à une activation laser, a fortement endommagé les tissus cancéreux et leurs fibroblastes environnants tout en épargnant largement les organoïdes issus de tissu colique sain. À travers plusieurs modèles sophistiqués, le même schéma est apparu : la nanothérapie ciblant les FAC a affaibli l’enveloppe protectrice de la tumeur, réanimé les réponses immunitaires locales et blessé directement les cellules cancéreuses.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
L’étude suggère que s’attaquer aux auxiliaires de la tumeur peut être aussi important que d’attaquer les cellules tumorales elles‑mêmes. En utilisant des nanoparticules magnétiques induisant la ferroptose pour désactiver sélectivement les fibroblastes associés au cancer, les chercheurs ont pu à la fois démanteler les barrières physiques et lever les freins chimiques sur le système immunitaire dans le cancer colorectal. Bien que ce travail en soit encore au stade préclinique, il ouvre la voie à une nouvelle classe de traitements combinant nanotechnologie ciblée, induction contrôlée de la mort cellulaire et activation immunitaire. De telles stratégies pourraient un jour rendre les cancers colorectaux résistants plus sensibles à l’immunothérapie et améliorer le pronostic des patients dont les tumeurs sont aujourd’hui difficiles à traiter.
Citation: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Mots-clés: cancer colorectal, microenvironnement tumoral, thérapie par nanoparticules, fibroblastes associés au cancer, ferroptose