Clear Sky Science · sv
Förbättring av kolorektalcancer-associerade fibroblaster i ett immunsuppressivt mikromiljö med ferroptos-baserad nanoterapi
Varför denna forskning betyder något för patienter med tjock- och ändtarmscancer
Många personer med kolorektalcancer får inte nytta av dagens banbrytande immunterapier eftersom deras tumörer är omgivna och skyddade av ett hårt lager stödjeceller. Denna studie undersöker en ny metod för att bryta det skyddet med särskilt utformade magnetiska nanopartiklar som selektivt skadar dessa stödjeceller, öppnar upp tumören för kroppens egna immunsvar och samtidigt hjälper till att döda cancerceller.
De dolda hjälparna som skyddar tumörer
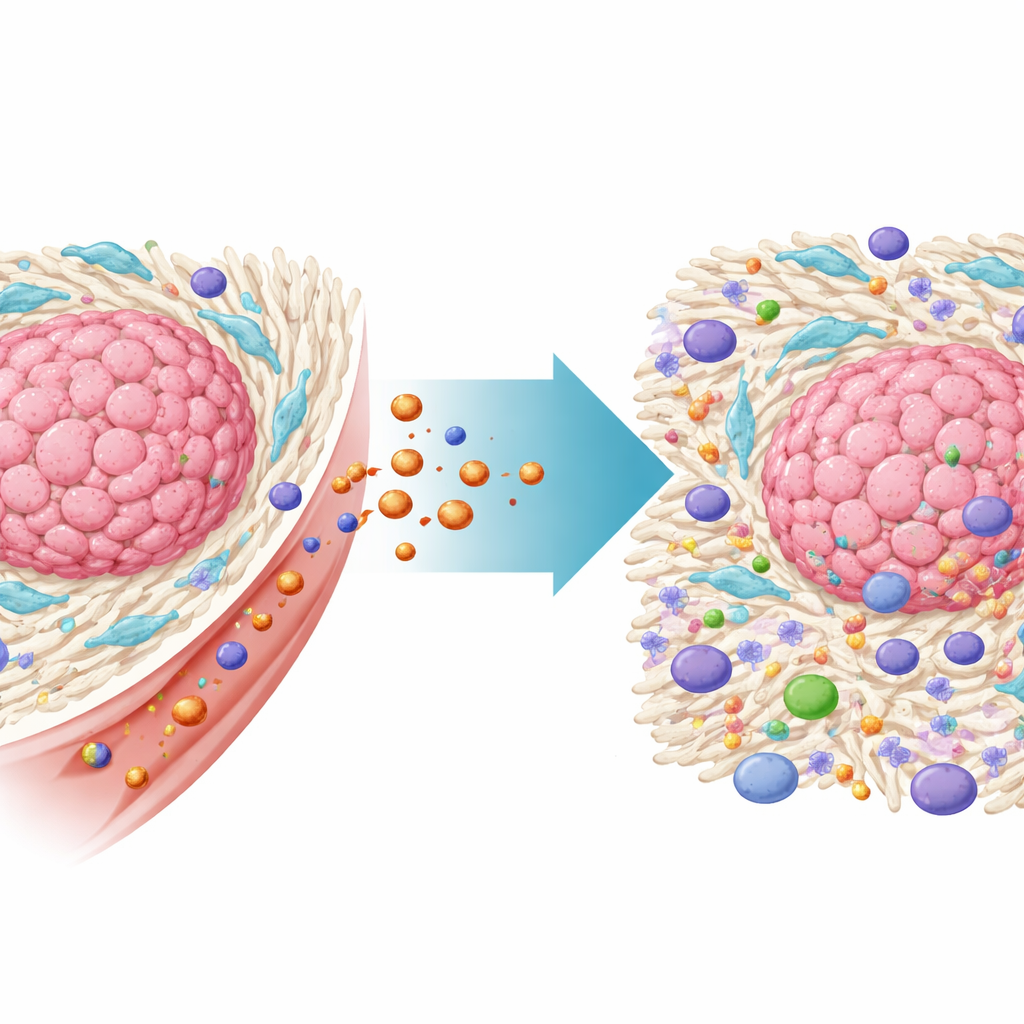
Kolorektala tumörer växer i ett komplext grannskap av icke-cancerösa celler som kallas tumörmikromiljön. Bland de viktigaste är cancerassocierade fibroblaster, eller CAFs, en typ av bindvävscell som kapats av tumören. CAFs bygger ett tätt skelett av extracellulär matrix runt cancern, vilket fysiskt blockerar immunceller och läkemedel från att tränga in. De utsöndrar också kemiska signaler som försvagar immunsvar och hjälper cancerceller att motstå behandling. Storskaliga patientdata i denna studie bekräftade att kolorektalcancer med rikliga CAFs var kopplade till sämre överlevnad och resistens mot immunterapi, vilket understryker behovet av att rikta in sig på dessa celler direkt.
En smart nanoterapi riktad mot tumörens stödjeceller
Forskarna utvecklade små koppar–järn-magnetiska nanopartiklar med en kärna-skal-struktur designade för att vara särskilt attraktiva för CAFs. Dessa partiklar har två viktiga fysikaliska egenskaper: de kan omvandla nära-infrarött laserljus till värme, och de kan katalysera bildandet av toxisk syrebaserad molekyler inne i celler. Eftersom CAFs naturligt tar upp fler nanopartiklar än normala fibroblaster eller många tumörceller, blir de det primära målet. Teamet fäste också en kort DNA-lik aptamer kallad AS1411 på ytan av vissa partiklar, för att styra dem mer effektivt till fibroblaster och tumörceller som visar proteinet nukleolin på sitt yttermembran.
Utlösning av en ny form av celldöd och omprogrammering av tumörsignaler
När nanopartiklarna väl kommit in i CAFs frigör de järn- och kopparjoner. Järn driver produktionen av reaktiva syreradikaler, medan koppar sänker nivåerna av ett skyddande enzym kallat GPX4. Tillsammans skjuter dessa förändringar CAFs in i ferroptos, en form av celldöd driven av okontrollerad oxidation av cellmembran. I odlingsskålar och djurmodeller visade CAFs sig vara mer sårbara för denna process än normala fibroblaster. Samtidigt förändrade de behandlade CAFs blandningen av kemiska budbärare de utsöndrade: signaler som normalt uppmuntrar tumörtillväxt och immunsuppression minskade, medan andra som hjälper till att rekrytera och aktivera immunceller ökade. Som ett resultat blev cancerceller som exponerades för de "omprogrammerade" fibroblastsekretenserna mindre kapabla att växa, migrera och anta invasiva egenskaper.
Att väcka immunsystemet inne i tumören
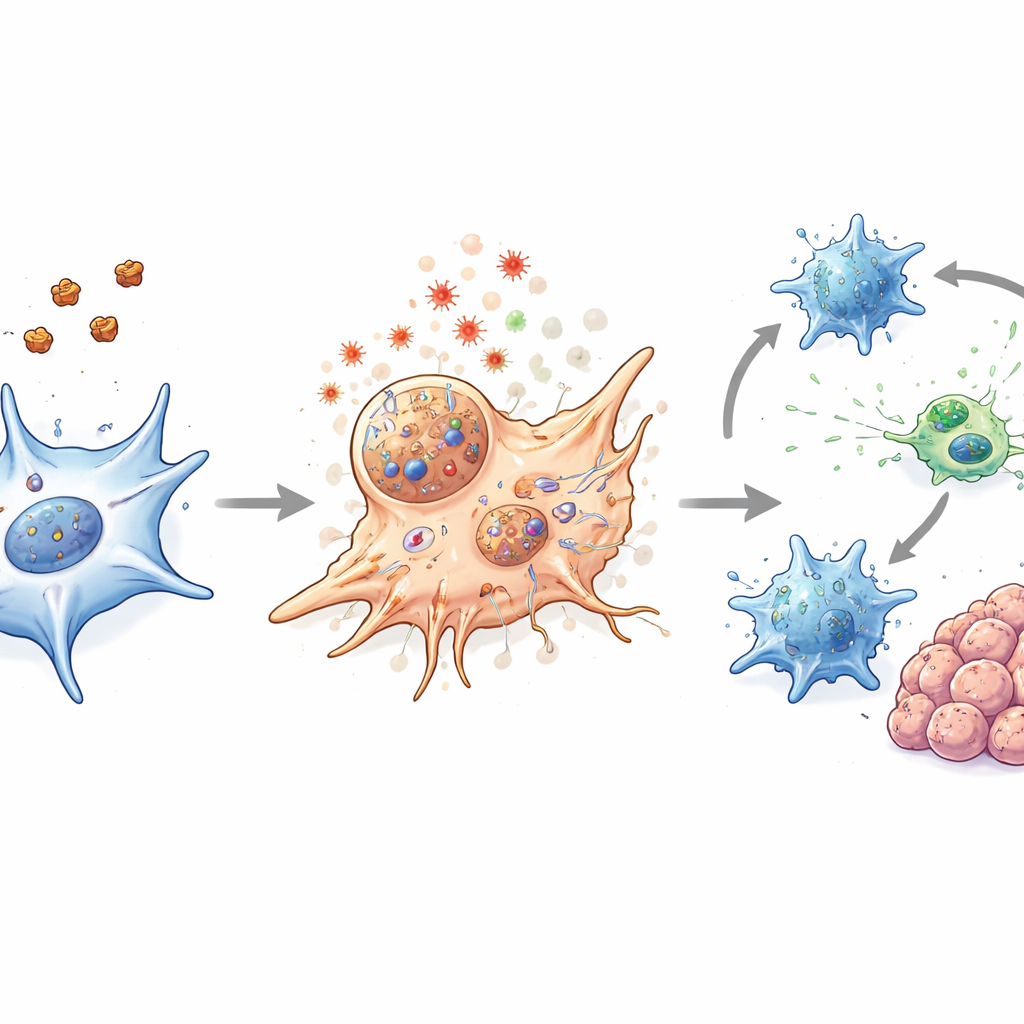
I musmodeller av kolorektalcancer, inklusive standardinplanterade tumörer, en genetisk modell som utvecklar spontana tarmtumörer, samt tumörer och organoider härledda från patienter, krympte nanopartikelbehandlingen tumörerna och gjorde det på ett säkert sätt. Viktigt är att terapin gjorde mer än att bara döda CAFs. Den lossade också det fysiska barriärskiktet runt tumörer och ändrade den lokala kemin på ett sätt som uppmuntrade immunaktivitet. Dendritiska celler, som fungerar som immunsystemets vakter och lärare, visade starkare tecken på mognad efter behandling. Dödar-CD8 T-celler blev mer aktiva och producerade fler molekyler förknippade med effektiv tumörattack, trots att deras totala antal inte förändrades dramatiskt. När nanopartiklar kombinerades med mild laseruppvärmning förstärktes dessa effekter ytterligare utan märkbar skada på normalt vävnad.
Från laboratoriemodeller mot framtida behandlingar
För att testa hur brett denna strategi kan fungera i verkliga kliniska inställningar tillämpade teamet sin metod på tumörprover och mini-tumörer (organoider) odlade från patienter. Nanopartikelterapin, särskilt versionen med AS1411-målriktning och i kombination med laseraktivering, skadade starkt cancerösa vävnader och deras omgivande fibroblaster samtidigt som organoider odlade från frisk tarmvävnad i huvudsak sparades. Över flera sofistikerade modeller framträdde samma mönster: CAF-fokuserad nanoterapi försvagade tumörens skyddande skal, återuppväckte lokala immunsvar och skadade direkt cancerceller.
Vad detta kan innebära för framtidens cancervård
Studien antyder att det kan vara lika viktigt att angripa tumörens hjälpare som att angripa tumörcellerna själva. Genom att använda ferroptos-baserade magnetiska nanopartiklar för att selektivt inaktivera cancerassocierade fibroblaster kunde forskarna både avlägsna fysiska barriärer och lyfta kemiska bromsar på immunsystemet vid kolorektalcancer. Även om arbetet fortfarande befinner sig i preklinisk fas pekar det mot en ny klass av behandlingar som kombinerar riktad nanoteknologi, kontrollerad celldöd och immunaktivering. Sådana strategier skulle en dag kunna göra resistenta kolorektala tumörer mer mottagliga för immunterapi och förbättra prognosen för patienter vars tumörer i dag är svåra att behandla.
Citering: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Nyckelord: kolorektalcancer, tumörmikromiljö, nanopartikelterapi, cancerassocierade fibroblaster, ferroptos