Clear Sky Science · it
Miglioramento dei fibroblasti associati al cancro colorettale nell’ambiente immunosoppressivo mediante nanoterapia basata sulla ferroptosi
Perché questa ricerca è importante per i pazienti con tumore del colon
Molte persone con cancro colorettale non traggono beneficio dalle attuali immunoterapie rivoluzionarie perché i loro tumori sono circondati e protetti da uno spesso strato di cellule di supporto. Questo studio esplora un nuovo modo per rompere quello scudo usando nanoparticelle magnetiche progettate appositamente che danneggiano selettivamente queste cellule di supporto, aprendo il tumore alle difese immunitarie dell’organismo e contribuendo al contempo a uccidere le cellule tumorali.
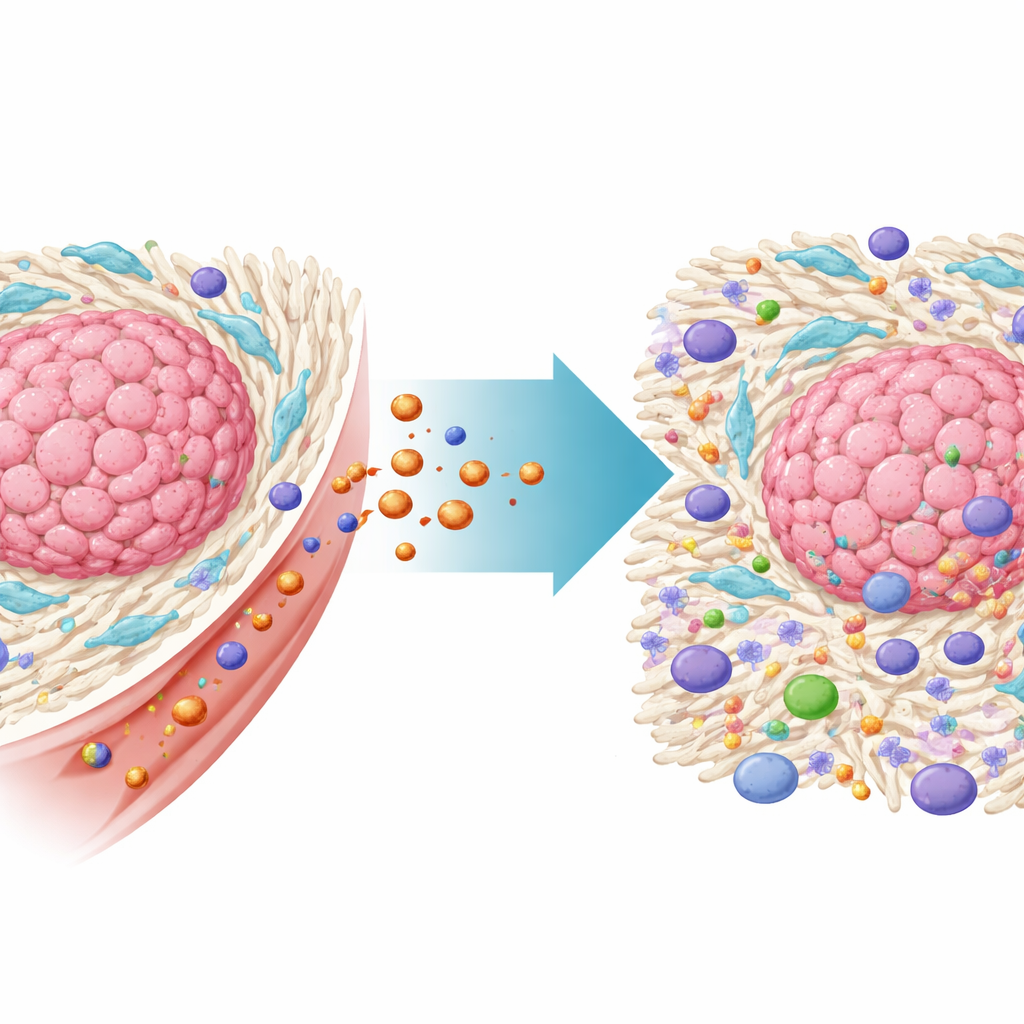
Gli aiutanti nascosti che proteggono i tumori
I tumori colorettali crescono all’interno di un quartiere complesso di cellule non cancerose chiamato microambiente tumorale. Tra le più importanti ci sono i fibroblasti associati al cancro, o CAF, un tipo di cellula del tessuto connettivo che viene cooptata dal tumore. I CAF costruiscono un denso impalcato di matrice extracellulare attorno al cancro, che fisicamente impedisce l’ingresso delle cellule immunitarie e dei farmaci. Rilasciano inoltre segnali chimici che indeboliscono le risposte immunitarie e aiutano le cellule tumorali a resistere alle terapie. Dati su larga scala dei pazienti in questo studio hanno confermato che i carcinomi colorettali ricchi di CAF sono associati a una sopravvivenza peggiore e a resistenza all’immunoterapia, sottolineando la necessità di colpire direttamente queste cellule.
Una nanoterapia intelligente mirata alle cellule di supporto del tumore
I ricercatori hanno sviluppato piccolissime nanoparticelle magnetiche rame–ferro con una struttura core–shell progettata per essere particolarmente attraente per i CAF. Queste particelle hanno due proprietà fisiche chiave: possono convertire la luce laser nel vicino infrarosso in calore e possono catalizzare la formazione di molecole ossigenate tossiche all’interno delle cellule. Poiché i CAF assorbono naturalmente più nanoparticelle rispetto ai fibroblasti normali o a molte cellule tumorali, diventano il bersaglio primario. Il gruppo ha inoltre attaccato alla superficie di alcune particelle un breve aptamero simile al DNA chiamato AS1411, che li guida più efficacemente verso fibroblasti e cellule tumorali che esprimono sulla membrana esterna una proteina chiamata nucleolina.
Indurre una nuova forma di morte cellulare e rimodulare i segnali tumorali
Una volta all’interno dei CAF, le nanoparticelle rilasciano ioni di ferro e rame. Il ferro alimenta la produzione di specie reattive dell’ossigeno, mentre il rame riduce i livelli di un enzima protettivo chiamato GPX4. Insieme, questi cambiamenti spingono i CAF verso la ferroptosi, una forma di morte cellulare guidata dall’ossidazione incontrollata delle membrane cellulari. In colture e modelli animali, i CAF si sono dimostrati più vulnerabili a questo processo rispetto ai fibroblasti normali. Allo stesso tempo, i CAF trattati hanno modificato il mix di messaggeri chimici che secernono: segnali che normalmente favoriscono la crescita tumorale e la soppressione immunitaria sono stati ridotti, mentre altri che aiutano a reclutare e attivare le cellule immunitarie sono aumentati. Di conseguenza, le cellule tumorali esposte alle secrezioni dei fibroblasti “riprogrammati” sono diventate meno capaci di crescere, migrare e acquisire tratti invasivi.
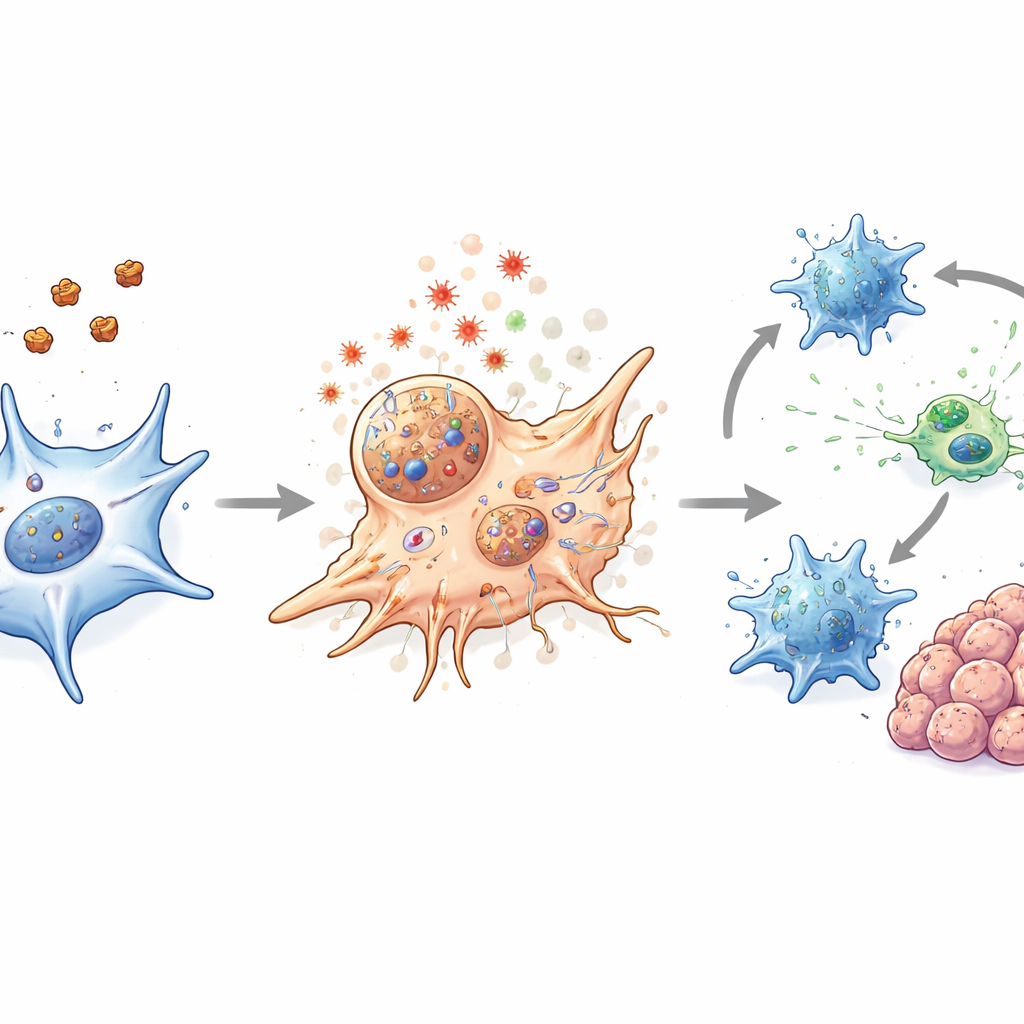
Risvegliare il sistema immunitario all’interno del tumore
Nei modelli murini di cancro colorettale, inclusi tumori impiantati standard, un modello genetico che sviluppa tumori intestinali spontanei e tumori e organoidi derivati da pazienti, il trattamento con nanoparticelle ha ridotto le dimensioni dei tumori e lo ha fatto in modo sicuro. È importante sottolineare che la terapia ha fatto più che eliminare i CAF. Ha anche allentato la barriera fisica attorno ai tumori e ha modificato la chimica locale in modo da favorire l’attività immunitaria. Le cellule dendritiche, che fungono da sentinelle e istruttrici del sistema immunitario, hanno mostrato segni più forti di maturazione dopo il trattamento. Le cellule T CD8 citotossiche sono diventate più attive e hanno prodotto più molecole associate a un attacco tumorale efficace, anche se il loro numero complessivo non è cambiato drasticamente. Quando le nanoparticelle sono state combinate con un lieve riscaldamento laser, questi effetti sono stati ulteriormente amplificati senza danni evidenti ai tessuti normali.
Dai modelli di laboratorio verso trattamenti futuri
Per verificare quanto ampiamente questo approccio potrebbe funzionare in contesti clinici reali, il team ha applicato la propria strategia a campioni tumorali e mini-tumori (organoidi) coltivati da pazienti. La terapia con nanoparticelle, in particolare la versione dotata del componente di targeting AS1411 e combinata con l’attivazione laser, ha danneggiato fortemente i tessuti cancerosi e i fibroblasti circostanti risparmiando in larga misura gli organoidi cresciuti da tessuto colon-rettale sano. In più modelli sofisticati è emerso lo stesso schema: la nanoterapia focalizzata sui CAF ha indebolito il guscio protettivo del tumore, ha risvegliato le risposte immunitarie locali e ha danneggiato direttamente le cellule tumorali.
Cosa potrebbe significare per la cura del cancro in futuro
Lo studio suggerisce che attaccare gli aiutanti del tumore può essere importante quanto attaccare le cellule tumorali stesse. Usando nanoparticelle magnetiche basate sulla ferroptosi per disabilitare selettivamente i fibroblasti associati al cancro, i ricercatori sono riusciti sia a smantellare le barriere fisiche sia a sollevare i freni chimici sul sistema immunitario nel cancro colorettale. Pur essendo ancora a uno stadio preclinico, questo lavoro indica una nuova classe di trattamenti che combinano nanotecnologia mirata, morte cellulare controllata e attivazione immunitaria. Tali strategie potrebbero un giorno rendere i carcinomi colorettali resistenti più sensibili all’immunoterapia e migliorare gli esiti per i pazienti i cui tumori oggi sono difficili da trattare.
Citazione: Wang, S., Wang, Z., Wu, C. et al. Amelioration of colorectal cancer-associated fibroblasts in immunosuppressive microenvironment by ferroptosis-based nanotherapy. Nat Commun 17, 2778 (2026). https://doi.org/10.1038/s41467-026-69462-5
Parole chiave: cancro colorettale, microambiente tumorale, terapia con nanoparticelle, fibroblasti associati al cancro, ferroptosi