Clear Sky Science · zh
GID/CTLH E3 连接酶复合体控制恶性疟原虫(Plasmodium falciparum)性别发育的细胞命运程序
这项疟疾研究为何重要
疟疾每年仍导致数十万人死亡,阻止寄生虫从人类传播到蚊子是终结该病的关键目标。本文揭示了疟原虫 Plasmodium falciparum 内部一个隐蔽的控制系统,该系统决定其性别型细胞(称为配子体)是否能够正确成熟并变得对蚊子具有传染性。通过说明一小组蛋白质如何微调这一决策,研究为开发可阻断传播的药物或疫苗指明了新的靶点,有助于在全球范围内遏制疟疾。
寄生虫迈向传染性的漫长道路
为了传播,P. falciparum 必须将部分血液期形式转化为专门的性细胞——雄性和雌性配子体,这一过程需耗时约 10–12 天。在这段缓慢的转变中,寄生虫的形态、代谢以及与红细胞的相互作用都会被彻底重塑。早期研究揭示了寄生虫 DNA 中的一个主开关如何激活进入性发育的决定,但对于寄生虫随后如何协调数千个分子步骤以形成成熟、可被蚊子感染的 V 期配子体知之甚少。作者们怀疑,除了基因的开关调控外,寄生虫还依赖受控的蛋白质降解来保持发育进程的正常进行。
性别发育的分子裁判
本研究关注一台被称为 GID/CTLH E3 连接酶复合体的蛋白质机器,此处称为 PfGID。E3 连接酶像标记装置一样,将小的泛素分子连接到选定蛋白上,以标记其被降解或被调整。通过扫描疟原虫基因组并与相关生物比较,研究人员鉴定出六个组分可以组装成 PfGID 复合体。他们证明这些蛋白在寄生虫内组成了一个保守的骨架,并在无性生长与配子体发育期间始终保持活性。引人注目的是,当任何 PfGID 亚基被删除时,寄生虫仍可在红细胞内增殖,但性发育在中途停滞。所得配子体呈现出停滞于中间形态的特征,并完全无法感染蚊子,证明 PfGID 对传播至关重要。
PfGID 如何引导雄性与雌性命运
为了解失去 PfGID 时出现的问题,研究组检查了突变寄生虫的全局 RNA 与蛋白质模式。他们发现关键过程如 RNA 加工、蛋白质合成和蛋白质回收被误调控,通常在雄性与雌性配子体中富集的蛋白质遭到严重扰动。具体而言,许多雄性特异性蛋白的丰度下降,而成熟配子体的标志在两性中都被削弱。
两条交织的控制臂:DNA 组织与信息沉默
PfDPL 似乎主要在塑造雄性谱系中发挥作用。它定位于发育中配子体的细胞核,并与组蛋白、染色质重塑因子、核孔及其它控制 DNA 包装与读取的因子相关联。当移除 PfDPL 时,雄性配子体中 DNA 复制、细胞分裂、鞭毛组装和受精所需的蛋白显著减少,雄性外鞭毛形成(雄性配子以爆发式释放精子样形式)几乎消失。相反,GD1 在细胞质中发挥作用,聚集成称为 P 体的小颗粒。这些结构作为信使 RNA 的储存与沉默中心。作者显示 GD1 与数个经典的翻译抑制因子配对,并结合数百个 RNA 信息分子,包括许多编码关键配子体因子的 mRNA。当 GD1 水平过低或过高——无论是被删除、过表达,还是因 PfGID 不能充分降解而累积——P 体组分的平衡被打破,配子体在早期发育阶段停滞。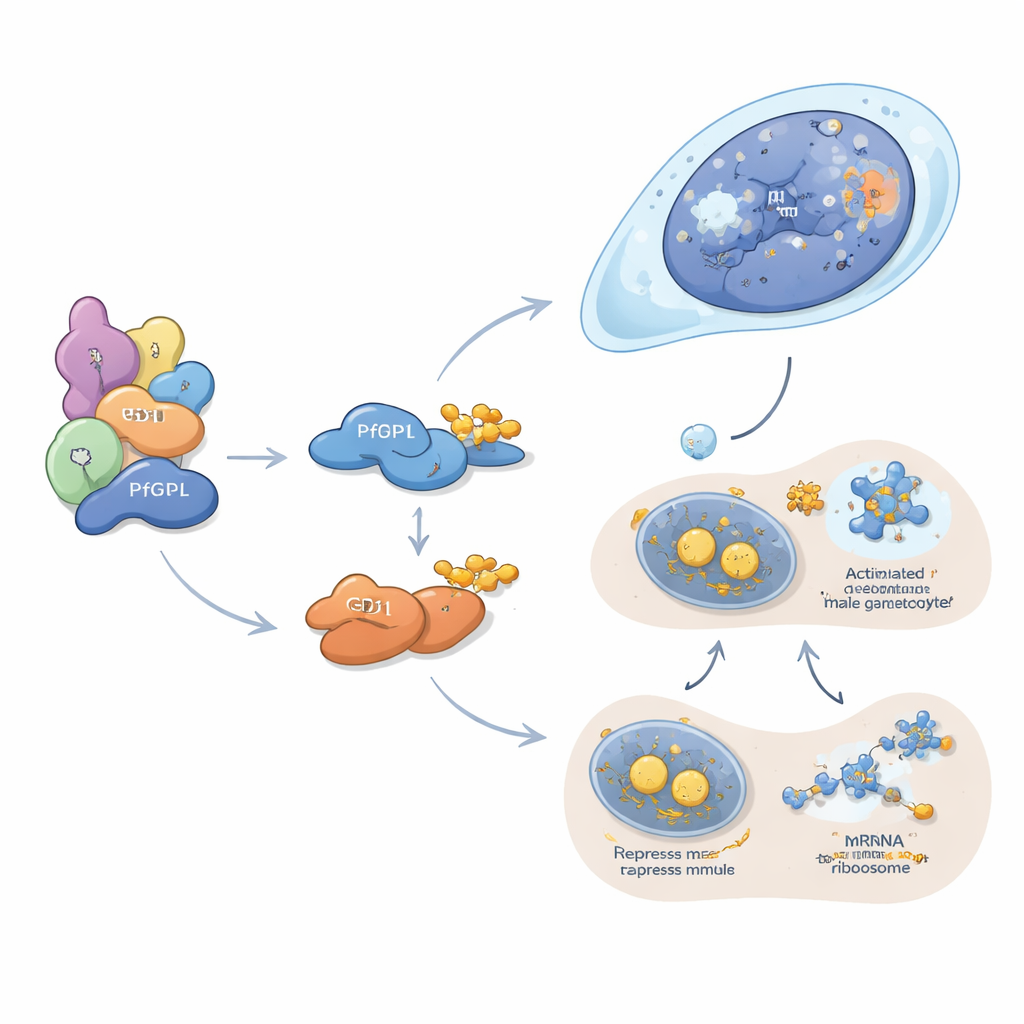
一个精细调整的寄生虫传播计时器
总体上,这些发现支持这样一个模型:PfGID 复合体作为分子裁判,在精确时刻调节 PfDPL 与 GD1 的数量和活性。通过在这些蛋白固有的柔性区段上添加或移除泛素标记,PfGID 可以快速调整 PfDPL 在细胞核中组织雄性特异基因的能力以及 GD1 将关键信使 RNA 保持在沉默状态的紧密程度。如果这一计时被扰乱,雄性与雌性配子体均无法成熟,寄生虫也就无法迁移到蚊子身上。对于普通读者来说,要点是:疟原虫依赖一个复杂的蛋白“质量控制”与信息沉默网络来变得具有传染性。针对 PfGID、PfDPL、GD1 或它们的相互作用,可能为在寄生虫到达蚊子之前将其“冻结”提供新的途径,从而切断传播链。
引用: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
关键词: 疟疾传播, 恶性疟原虫配子体, 泛素连接酶, RNA 翻译抑制, 寄生虫细胞命运