Clear Sky Science · sv
GID/CTLH E3-ligas komplex styr cellödesprogram för sexuell utveckling hos Plasmodium falciparum
Varför denna malariastudie är viktig
Malaria dödar fortfarande hundratusentals människor varje år, och att stoppa parasiten från att överföras från människa till mygga är ett centralt mål för att utrota sjukdomen. Denna artikel avslöjar ett dolt kontrollsystem inne i malariaparasiten Plasmodium falciparum som avgör om dess sexuella former, kallade gametocyter, mognar korrekt och blir infektiösa för myggor. Genom att förklara hur en liten grupp proteiner finslipar detta beslut pekar studien på nya mål för läkemedel eller vacciner som kan blockera transmission och bidra till att begränsa malaria globalt.
Parasitens långa väg mot att bli infektiös
För att spridas måste P. falciparum omvandla några av sina blodstadier till specialiserade sexuella celler, manliga och kvinnliga gametocyter, som utvecklas under 10–12 dagar. Under denna långsamma omvandling remodelleras parasitens form, ämnesomsättning och interaktion med röda blodkroppar fullständigt. Tidigare arbete hade visat hur en huvudbrytare i parasitens DNA sätter igång beslutet att gå in i den sexuella banan, men mycket mindre var känt om hur parasiten därefter koordinerar de tusentals molekylära stegen som krävs för att nå fullbildade, myggredo stadium V-gametocyter. Författarna misstänkte att parasiten, utöver att slå på och av gener, också förlitar sig på kontrollerad proteinneringsprocess för att hålla utvecklingen på rätt spår.
En molekylär domare för sexuell utveckling
Studien fokuserar på en proteinmaskin kallad GID/CTLH E3-ligas komplexet, här benämnt PfGID. E3-ligaser fungerar som märkningsapparater, fäster små ubiquitinmolekyler på utvalda proteiner för att markera dem för nedbrytning eller anpassning. Genom att skanna malariagenomet och jämföra det med närbesläktade organismer identifierade forskarna sex komponenter som monteras till ett PfGID-komplex. De visade att dessa proteiner bildar ett bevarat skelett inom parasiten och är aktiva både under asextuell tillväxt och under gametocytutveckling. Slående nog, när någon av PfGID-subenheterna raderades kunde parasiten fortfarande föröka sig i röda blodkroppar, men den sexuella utvecklingen stannade av runt mitten. De resulterande gametocyterna såg ut att fastna i en intermediär form och kunde helt misslyckas med att infektera myggor, vilket visar att PfGID är avgörande för transmission.
Hur PfGID styr manliga och kvinnliga öden
För att förstå vad som går fel när PfGID försvinner undersökte teamet globala RNA- och proteinmönster i de mutanta parasiterna. De fann att nyckelprocesser som RNA-bearbetning, proteintillverkning och proteinåtervinning var dysreglerade, och att proteiner som normalt är förhöjda i manliga respektive kvinnliga gametocyter var hårt påverkade. Särskilt minskade mängden av många manliga specifika proteiner, medan markörer för mogna gametocyter reducerades i båda könen. 
Två sammanflätade kontrollarmar: DNA-organisation och meddelandes tystnad
PfDPL verkar huvudsakligen arbeta med att forma den manliga linjen. Det lokaliserar till kärnan i utvecklande gametocyter och associerar med histoner, kromatinombyggare, nukleära porer och andra faktorer som styr hur DNA packas och läses. När PfDPL tas bort minskar proteiner som krävs för DNA-replikation, celldelning, flagelluppbyggnad och befruktning i manliga gameter kraftigt, och manlig exflagellering—den explosiva utsläppningen av spermieliknande former—nästan försvinner. I kontrast verkar GD1 fungera i cytoplasman, där det klustrar i små granuler kända som P-kroppar. Dessa strukturer fungerar som lagrings- och tystningsnav för budbärar-RNA. Författarna visar att GD1 samarbetar med flera klassiska translationsrepressorer och binder hundratals RNA-meddelanden, inklusive många som kodar för viktiga gametocytfaktorer. När GD1-nivåerna är antingen för låga eller för höga—eftersom det är raderat, överuttryckt eller otillräckligt nedbrutet av PfGID—blir P-kroppskomponenter obalanserade och gametocyter stannar upp tidigt i utvecklingen. 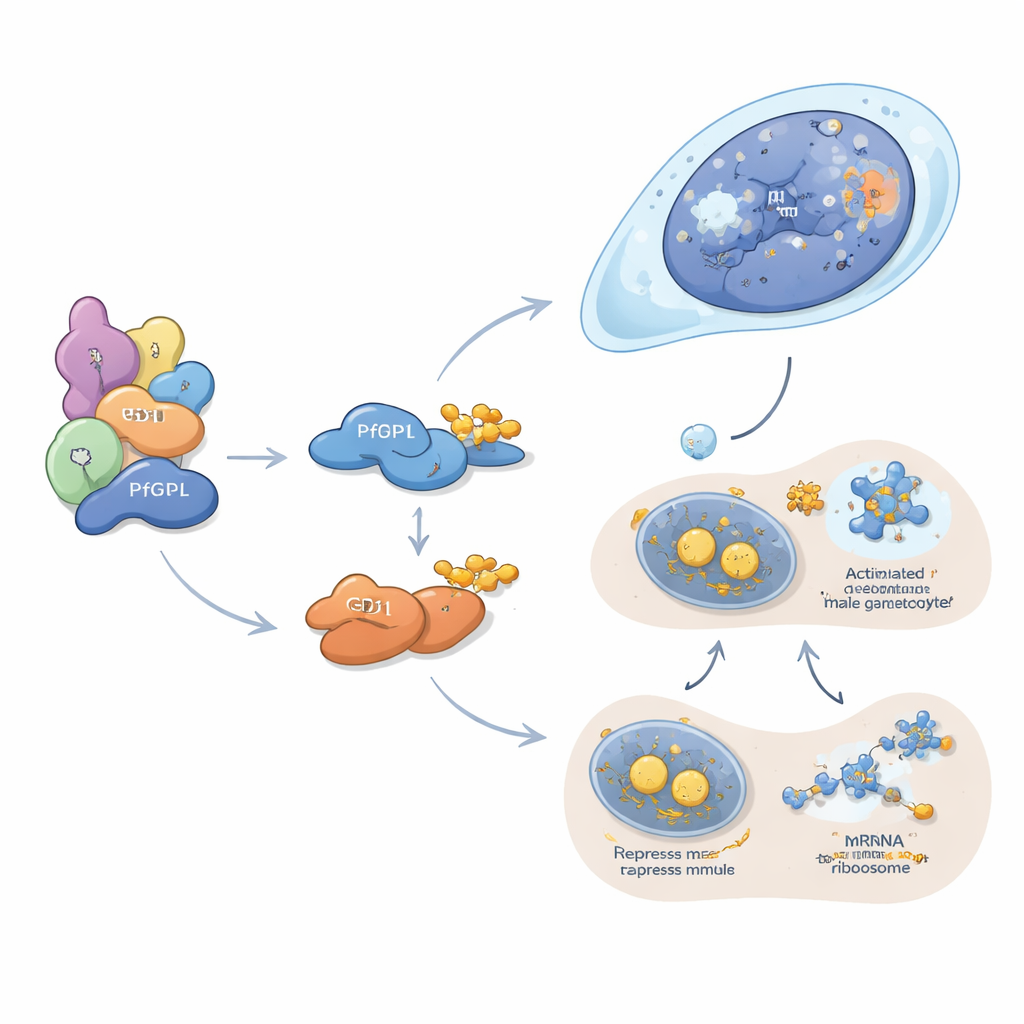
En fint ställd timer för parasittransmission
Tillsammans stöder resultaten en modell där PfGID-komplexet fungerar som en molekylär domare som ställer in mängden och aktiviteten hos PfDPL och GD1 vid precisa tidpunkter. Genom att lägga till eller ta bort ubiquitinmärken på intrinsikt flexibla regioner i dessa proteiner kan PfGID snabbt justera hur effektivt PfDPL organiserar manliga-specifika gener i kärnan och hur hårt GD1 håller viktiga RNA-meddelanden i ett tyst läge. Om denna timing rubbas mognar inte manliga och kvinnliga gametocyter, och parasiten kan inte övergå till myggan. För en lekmannan läsare är slutsatsen att malariaparasiter förlitar sig på ett sofistikerat protein-”kvalitetskontroll”- och meddelande-tystningsnätverk för att bli infektiösa. Att rikta in PfGID, PfDPL, GD1 eller deras interaktioner skulle därmed kunna erbjuda nya sätt att frysa parasiten innan den når myggan och bryta kedjan av transmission.
Citering: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Nyckelord: malariatransmission, Plasmodium falciparum gametocyter, ubiquitinligas, RNA-translationell reprimering, parasitens cellöde