Clear Sky Science · nl
GID/CTLH E3-ligasecomplex stuurt celdifferentiatie voor de seksuele ontwikkeling van Plasmodium falciparum
Waarom deze malariestudie ertoe doet
Malaria doodt nog steeds honderden duizenden mensen per jaar, en het stoppen van de overdracht van de parasiet van mens naar mug is een sleuteldoel voor het uitroeien van de ziekte. Dit artikel onthult een verborgen regelsysteem in de malariaparasiet Plasmodium falciparum dat bepaalt of de seksuele vormen, gametocyten genoemd, goed rijpen en besmettelijk worden voor muggen. Door uit te leggen hoe een kleine groep eiwitten deze beslissing fijn afstemt, wijst de studie op nieuwe doelwitten voor geneesmiddelen of vaccins die transmissie kunnen blokkeren en zo helpen malaria wereldwijd terug te dringen.
De lange weg van de parasiet naar besmettelijkheid
Om zich te verspreiden moet P. falciparum sommige van zijn bloedstadia omzetten in gespecialiseerde seksuele cellen, mannelijke en vrouwelijke gametocyten, die zich over 10–12 dagen ontwikkelen. Tijdens deze trage transformatie worden vorm, stofwisseling en de interactie met de rode bloedcel volledig heringericht. Eerder werk liet zien hoe een hoofdschakel in het DNA van de parasiet de beslissing om de seksuele weg in te slaan activeert, maar veel minder was bekend over hoe de parasiet vervolgens de duizenden moleculaire stappen coördineert die nodig zijn om volledig gevormde, mugklare stadium V-gametocyten te bereiken. De auteurs veronderstelden dat de parasiet, naast het aan- en uitzetten van genen, ook vertrouwt op gecontroleerde eiwitafbraak om de ontwikkeling op koers te houden.
Een moleculaire scheidsrechter voor seksuele ontwikkeling
De studie richt zich op een eiwitmachine die het GID/CTLH E3-ligasecomplex wordt genoemd, hier PfGID genoemd. E3-ligases werken als labelapparaten: ze hechten kleine ubiquitinemoleculen aan geselecteerde eiwitten om ze te markeren voor afbraak of aanpassing. Door het malariagenoom te doorzoeken en te vergelijken met verwante organismen identificeerden de onderzoekers zes componenten die samen een PfGID-complex vormen. Ze toonden aan dat deze eiwitten een geconserveerd skelet binnen de parasiet vormen en actief zijn gedurende zowel aseksuele groei als gametocytontwikkeling. Opvallend was dat, wanneer een van de PfGID-subunits werd verwijderd, de parasiet nog steeds in rode bloedcellen kon vermenigvuldigen, maar de seksuele ontwikkeling stokte ongeveer halverwege. De resulterende gametocyten leken vast te zitten in een tussenvorm en faalden volledig om muggen te infecteren, wat PfGID als essentieel voor transmissie onthult.
Hoe PfGID mannelijke en vrouwelijke lotsbestemmingen stuurt
Om te begrijpen wat er misgaat wanneer PfGID ontbreekt, onderzocht het team globale RNA- en eiwitpatronen in de gemuteerde parasieten. Ze vonden dat kernprocessen zoals RNA-bewerking, eiwitsynthese en eiwitherstel ontregeld waren, en dat eiwitten die normaal verrijkt zijn in mannelijke en vrouwelijke gametocyten sterk verstoord waren. In het bijzonder daalde de hoeveelheid van veel mannelijk-specifieke eiwitten, terwijl merkers van rijpe gametocyten in beide geslachten werden verminderd. 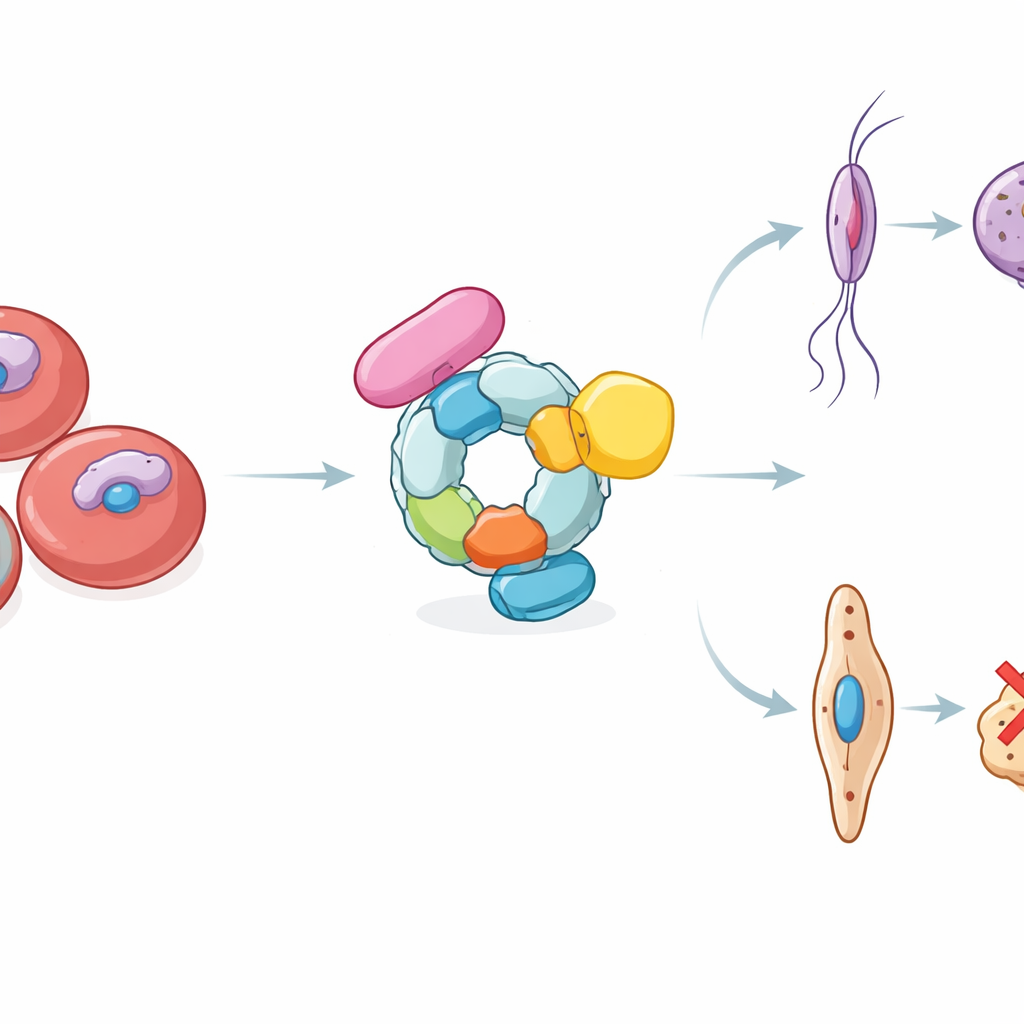
Twee verstrengelde regelarmen: DNA-organisatie en boodschapperstillegging
PfDPL lijkt vooral in de mannelijke lijn te werken. Het lokaliseert naar de kern van ontwikkelende gametocyten en associeert met histonen, chromatineremodellers, kernporiën en andere factoren die bepalen hoe DNA wordt verpakt en afgelezen. Wanneer PfDPL wordt verwijderd, nemen eiwitten die nodig zijn voor DNA-replicatie, celdeling, flagelassemblage en de bevruchting in mannelijke gameten sterk af, en mannelijke exflagellatie—de explosieve afgifte van sperma-achtige vormen—verdwijnt bijna. Daarentegen werkt GD1 in het cytoplasma, waar het zich clustert in kleine korrels die bekendstaan als P-bodies. Deze structuren fungeren als opslag- en stilleggingshubs voor boodschapper-RNAs. De auteurs tonen aan dat GD1 samenwerkt met meerdere klassieke translatierepressoren en honderden RNA-boodschappen bindt, inclusief vele die sleutelfactoren voor gametocyten coderen. Wanneer GD1-niveaus ofwel te laag of te hoog zijn—omdat het verwijderd, overgedrukt of onvoldoende afgebroken wordt door PfGID—geraakt de balans van P-bodycomponenten verstoord en stokt de gametocytontwikkeling vroegtijdig. 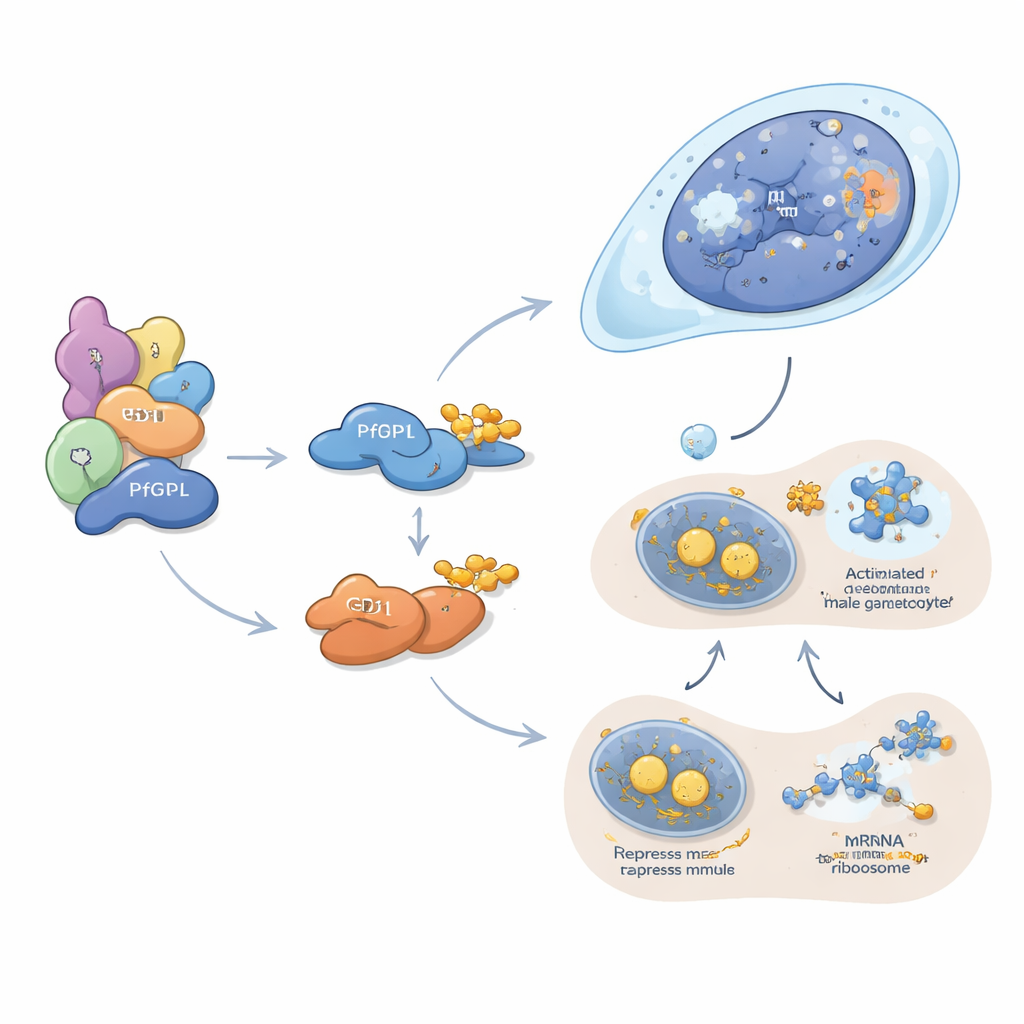
Een fijn afgestelde timer voor parasiettransmissie
Gezamenlijk ondersteunen de bevindingen een model waarin het PfGID-complex fungeert als moleculaire scheidsrechter die de hoeveelheid en activiteit van PfDPL en GD1 op precies het juiste moment afstemt. Door ubiquitinelabels toe te voegen of te verwijderen op intrinsiek flexibele regio’s van deze eiwitten kan PfGID snel aanpassen hoe sterk PfDPL mannelijkspecifieke genen in de kern organiseert en hoe stevig GD1 belangrijke RNA-boodschappen in een stilstaande staat houdt. Als deze timing verstoord raakt, rijpen mannelijke en vrouwelijke gametocyten niet, en kan de parasiet niet naar de mug overgaan. Voor de niet-specialist is de kernboodschap dat malariaparasieten vertrouwen op een verfijnd eiwit-“kwaliteitscontrole”- en boodschapstilleggingsnetwerk om besmettelijk te worden. Het richten op PfGID, PfDPL, GD1 of hun interacties kan daarom nieuwe manieren bieden om de parasiet stil te zetten voordat hij de mug bereikt en zo de transmissieketen te doorbreken.
Bronvermelding: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Trefwoorden: malariatransmissie, Plasmodium falciparum gametocyten, ubiquitine-ligase, translatie-repressie van RNA, parasiet celdifferentiatie