Clear Sky Science · he
קומפלקס E3 ליגאז GID/CTLH שולט בתכניות גורל תאי להתפתחות המינית של Plasmodium falciparum
מדוע המחקר הזה על המלריה חשוב
מלריה עדיין הורגת מאות אלפי אנשים מדי שנה, ומניעת מעבר הטפיל מאדם ליתוש היא מטרה מרכזית בכיבוי המחלה. מאמר זה חושף מערכת בקרה נסתרת בתוך הטפיל Plasmodium falciparum שמחליטה האם הצורות המיניות שלו, המכונות גמטוציטים, יתפתחו כראוי ויהפכו לזיהומיות ליתושים. על ידי הבהרת האופן שבו קבוצה קטנה של חלבונים מכווננת את ההחלטה הזו, המחקר מצביע על מטרות חדשות אפשריות לתרופות או חיסונים שיכולים לחסום העברה ולסייע להפחתת המלריה בעולם.
הדרך הארוכה של הטפיל להיות זיהומי
כדי להתפשט, P. falciparum חייב להפוך חלק מצורותיו שלב הדם לתאים מיניים מתמחים, גמטוציטים זכריים ונקביים, שמפתחים במשך 10–12 ימים. במהלך השינוי האיטי הזה צורת הטפיל, המטבוליזם שלו והאינטראקציה עם תא הדם האדום עוברים שינוי מוחלט. עבודות קודמות חשפו כיצד מתג מאסטר בדנ״א של הטפיל מדליק את ההחלטה להיכנס לנתיב המיני, אך ידוע פחות כיצד הטפיל מתאם אחר כך את אלפי השלבים המולקולריים הדרושים להגיע לגמטוציטים בשלב V בוגרים ומוכנים ליתוש. החוקרים חשדו כי מעבר לבקרה על ביטוי גנים, הטפיל גם נשען על השמדת חלבונים מבוקרת כדי לשמור על מסלול ההתפתחות.
שופט מולקולרי להתפתחות המינית
המחקר מתמקד במכונה חלבונית שנקראת קומפלקס E3 ליגאז GID/CTLH, המכונה כאן PfGID. ליגאזים E3 פועלים כמו מכשירי תגית—מצמידים מולקולות אוביקוויטין קטנות לחלבונים מסוימים כדי לסמן אותם לפירוק או להתאמה. באמצעות סריקה של הגנום של הטפיל והשוואתו לאורגניזמים קרובים, החוקרים זיהו שישה רכיבים שמתאספים לקומפלקס PfGID. הם הראו כי חלבונים אלה יוצרים שלד שמור בתוך הטפיל ופועלים הן במהלך הצמיחה הא-מינית והן בהתפתחות הגמטוציטים. באופן מעניין, כאשר כל אחד מתתי-היחידות של PfGID הוסר, הטפיל עדיין יכול היה להתרבות בתאי דם אדומים, אך ההתפתחות המינית נעצרה סביב נקודת האמצע. הגמטוציטים שהתפתחו נראו תקועים במצב ביניים וכשלו לחלוטין בזיהום יתושים, מה שמראה כי PfGID חיוני להעברה.
כיצד PfGID מכוון גורלות זכריים ונקביים
כדי להבין מה משתבש כאשר PfGID חסר, הצוות בחן דפוסי RNA וחלבון גלובליים בטפילים המוטנטים. הם מצאו כי תהליכים מרכזיים כגון עיבוד RNA, ייצור חלבונים ומחזור חלבונים היו מופרעים, ושהרמות של חלבונים הרגילים לעושר בגמטוציטים זכריים ונקביים הופרעו בחוזקה. במיוחד, שפעם של חלבונים ספציפיים לזכרים ירד, בעוד שסמנים של גמטוציטים בוגרים ירדו בשני המינים. 
שתי זרועות בקרה משולבות: ארגון דנ"א ושתקת מסרים
נראה כי PfDPL פועל בעיקר בעיצוב הקו הזכרי. הוא ממוקם בגרעין של גמטוציטים מתפתחים ומתאסף עם היסטונים, מתמרים כרומטין, נקבים גרעיניים וגורמים אחרים השולטים באריזת וקריאת הדנ"א. כשה-PfDPL מוסר, חלבונים הנחוצים לשכפול דנ"א, חלוקת תאים, בניית שוטון והפריה בגמטות זכריות קטנים בחדות, ואקספלקציית זכר—שחרור חזק של צורות דמויות תאי זרע—כמעט נעלמת. לעומת זאת, GD1 פועל בציטופלזמה, שם הוא מצטבר לגרגרים זעירים הידועים כגופי P. מבנים אלה משמשים מאגרי אחסון והשתקה עבור מסרי mRNA. המחברים מראים כי GD1 משתף פעולה עם מספר מדכאי תרגום קלאסיים וקושר מאות מסרים של RNA, כולל רבים המקודדים לגורמי גמטוציט מרכזיים. כאשר רמות GD1 הן נמוכות מדי או גבוהות מדי—בגלל הסרה, ביטוי יתר או חוסר פירוק מספיק על ידי PfGID—רכיבי גופי P מאבדים איזון, והגמטוציטים נעצרים בשלבים מוקדמים של התפתחות. 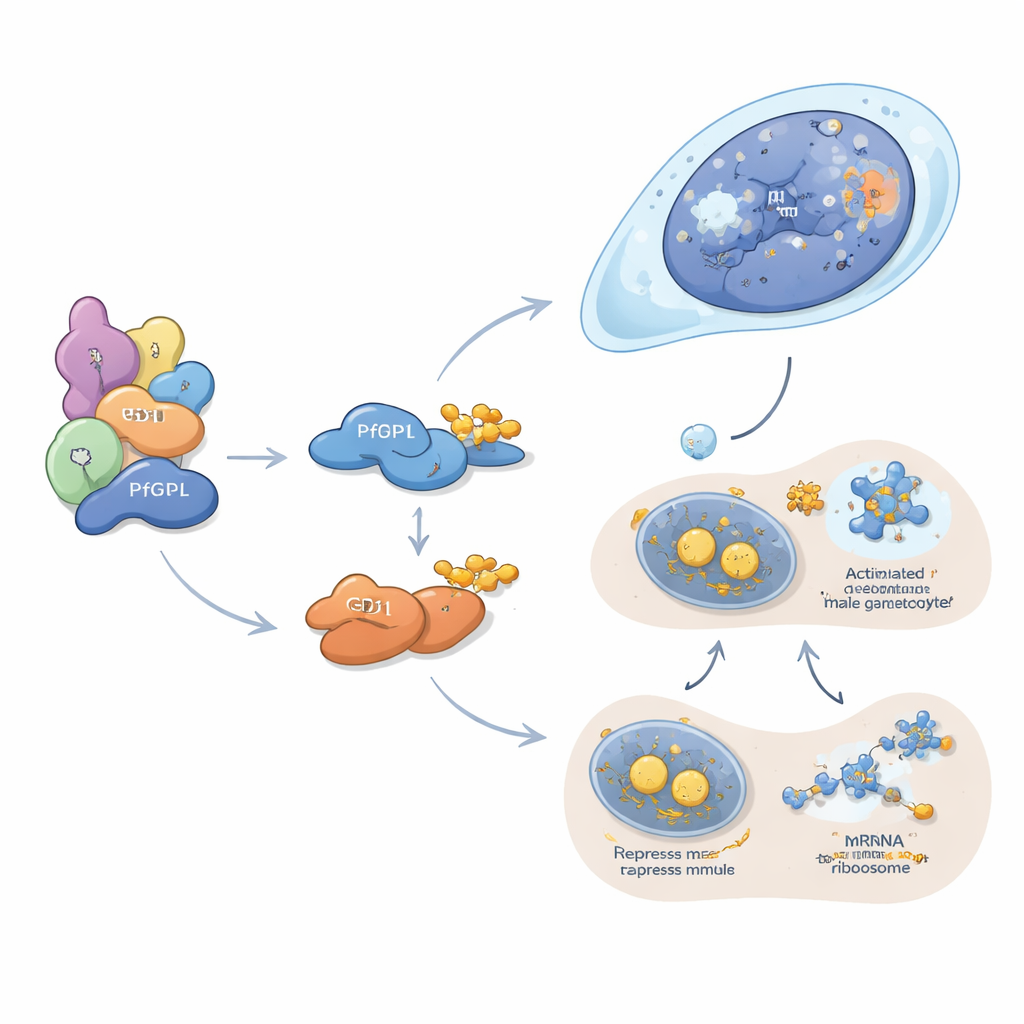
שעון מכוון לדייק זמן העברת הטפיל
הממצאים תומכים בדגם שבו קומפלקס PfGID פועל כשופט מולקולרי, מכוונן את כמות ופעילות PfDPL ו-GD1 בזמנים מדויקים. על ידי הוספה או הסרה של תגי אוביקוויטין באזורים גמישים אינטרינזיים של חלבונים אלה, PfGID יכול לכוונן במהירות עד כמה PfDPL מארגן גנים ספציפיים לזכרים בגרעין וכמה חזק GD1 שומר מסרי RNA במצב מושתק. אם תזמון זה מופר, גמטוציטים זכריים ונקביים אינם מגיעים לבגרות והטפיל אינו יכול לעבור ליתוש. לקורא שאינו מומחה, המסקנה היא שטפילי המלריה נשענים על מערכת מתוחכמת של "בקרת איכות" חלבונית ורשת השתקת מסרים כדי להפוך לזיהומיים. פגיעה ב-PfGID, PfDPL, GD1 או באינטראקציות ביניהם עשויה לכן להציע דרכים חדשות להקפיא את הטפיל לפני שיגיע ליתוש ולשבור את שרשרת ההעברה.
ציטוט: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
מילות מפתח: העברת מלריה, גמטוציטים של Plasmodium falciparum, ליגאז אוביקוויטין, דיכוי תרגום RNA, גורל תאי של טפיל