Clear Sky Science · de
GID/CTLH E3-Ligase-Komplex steuert zelluläre Schicksalsprogramme für die sexuelle Entwicklung von Plasmodium falciparum
Warum diese Malaria-Studie wichtig ist
Malaria tötet weiterhin Hunderttausende von Menschen pro Jahr, und zu verhindern, dass der Parasit vom Menschen auf Mücken übergeht, ist ein zentrales Ziel zur Eindämmung der Krankheit. Diese Studie enthüllt ein verborgenes Kontrollsystem im Malariaparasiten Plasmodium falciparum, das darüber entscheidet, ob seine sexuellen Formen, die Gametozyten, richtig ausreifen und für Mücken infektiös werden. Indem sie erklärt, wie eine kleine Gruppe von Proteinen diese Entscheidung fein abstimmt, weist die Arbeit auf neue Angriffspunkte für Medikamente oder Impfstoffe hin, die die Übertragung blockieren und so zur Eindämmung von Malaria weltweit beitragen könnten.
Der lange Weg des Parasiten zur Infektiosität
Um sich zu verbreiten, muss P. falciparum einige seiner Blutstadien in spezialisierte Sexualzellen, männliche und weibliche Gametozyten, umwandeln, die sich über 10–12 Tage entwickeln. Während dieser langsamen Umgestaltung werden Form, Stoffwechsel und die Wechselwirkung mit der roten Blutzelle vollständig umgebaut. Frühere Arbeiten hatten gezeigt, wie ein Master-Schalter in der Parasiten-DNA die Entscheidung für den Eintritt in den sexuellen Weg auslöst, aber deutlich weniger war darüber bekannt, wie der Parasit anschließend die Tausenden molekularen Schritte koordiniert, die nötig sind, um voll ausgebildete, mückenbereite Gametozyten des Stadiums V zu erreichen. Die Autoren vermuteten, dass der Parasit neben dem Ein- und Ausschalten von Genen auch auf kontrollierten Proteinabbau angewiesen ist, um die Entwicklung auf Kurs zu halten.
Ein molekularer Schiedsrichter für die sexuelle Entwicklung
Die Studie konzentriert sich auf eine Proteinanlage namens GID/CTLH E3-Ligase-Komplex, hier PfGID genannt. E3-Ligasen wirken wie Markiergeräte, die kleinen Ubiquitin-Molekülen an ausgewählte Proteine anhängen, um deren Abbau oder Modifikation zu kennzeichnen. Durch Durchsuchen des Malaria-Genoms und einen Vergleich mit verwandten Organismen identifizierten die Forschenden sechs Komponenten, die sich zu einem PfGID-Komplex zusammensetzen. Sie zeigten, dass diese Proteine ein konserviertes Gerüst im Parasiten bilden und sowohl während des asexuellen Wachstums als auch während der Gametozytenentwicklung aktiv sind. Auffällig war, dass bei der Deletion einzelner PfGID-Untereinheiten der Parasit sich zwar weiterhin in roten Blutkörperchen vermehren konnte, die sexuelle Entwicklung aber etwa zur Hälfte stecken blieb. Die resultierenden Gametozyten wirkten wie in einem Zwischenstadium eingefroren und konnten Mücken überhaupt nicht infizieren, was PfGID als essenziell für die Übertragung ausweist.
Wie PfGID männliche und weibliche Schicksale lenkt
Um zu verstehen, was schiefläuft, wenn PfGID fehlt, untersuchte das Team globale RNA- und Proteomprofile der Mutantenparasiten. Sie fanden, dass Schlüsselprozesse wie RNA-Verarbeitung, Proteinsynthese und Proteinrecycling fehlreguliert waren und dass Proteine, die normalerweise in männlichen beziehungsweise weiblichen Gametozyten angereichert sind, stark gestört wurden. Insbesondere sank die Fülle vieler männlichkeitsspezifischer Proteine, während Marker reifer Gametozyten in beiden Geschlechtern reduziert waren. 
Zwei verflochtene Steuerarme: DNA-Organisation und Nachrichten-Stilllegung
PfDPL scheint vor allem die männliche Linie zu formen. Es lokalisert sich im Zellkern sich entwickelnder Gametozyten und assoziiert mit Histonen, Chromatin-Remodellierern, Kernporen und anderen Faktoren, die steuern, wie DNA verpackt und gelesen wird. Wird PfDPL entfernt, gehen Proteine verloren, die für DNA-Replikation, Zellteilung, Flagellenaufbau und Befruchtung in männlichen Gameten benötigt werden, und die männliche Exflagellation — die explosionsartige Freisetzung spermienähnlicher Formen — verschwindet nahezu. Im Unterschied dazu wirkt GD1 im Zytoplasma, wo es sich zu kleinen Granula sammelt, den sogenannten P-Bodies. Diese Strukturen fungieren als Speicher- und Silencing-Zentren für messenger-RNAs. Die Autoren zeigen, dass GD1 mit mehreren klassischen Translationsrepressoren zusammenarbeitet und Hunderte von RNA-Nachrichten bindet, darunter viele, die Schlüsselkomponenten der Gametozyten codieren. Liegt GD1 entweder zu gering oder zu hoch vor — etwa weil es gelöscht, überexprimiert oder von PfGID unzureichend abgebaut wird — gerät die Zusammensetzung der P-Bodies aus dem Gleichgewicht und Gametozyten bleiben früh in der Entwicklung stehen. 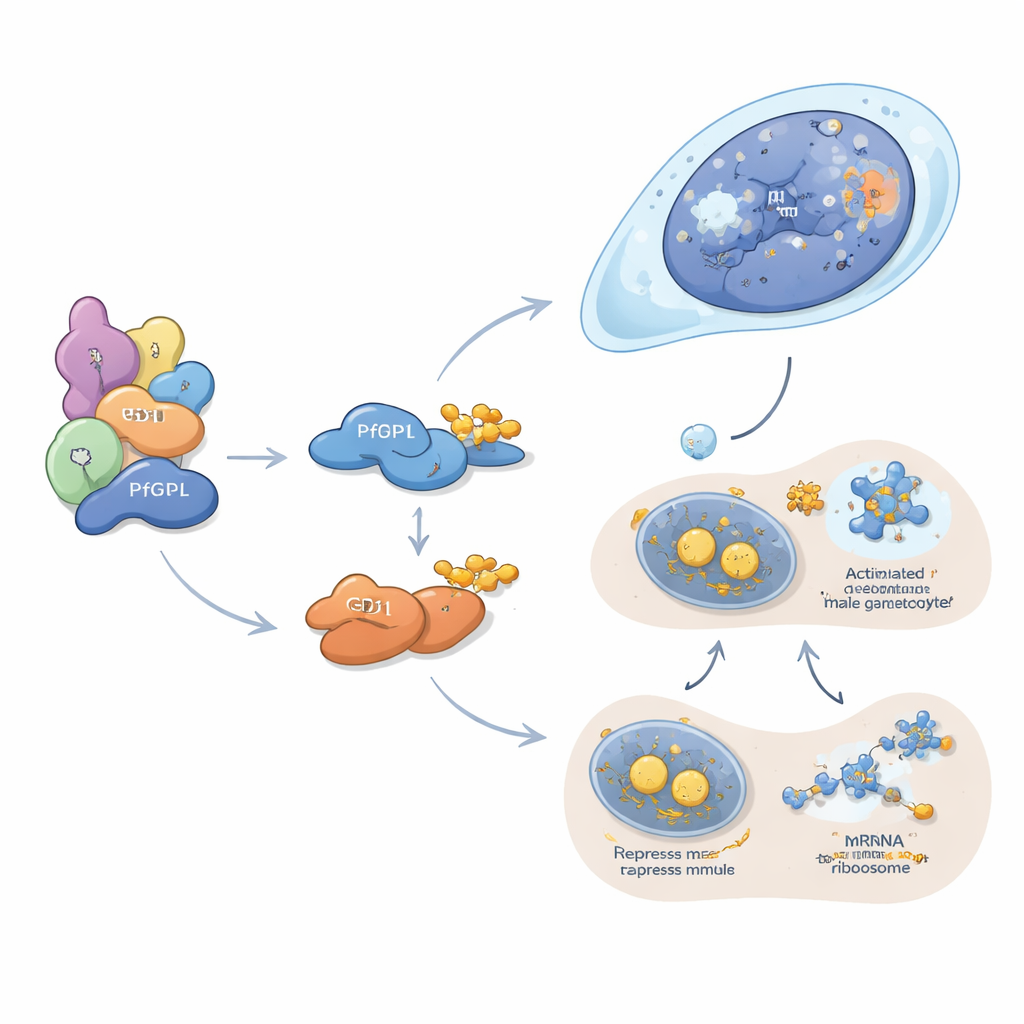
Ein fein abgestimmter Timer für die Parasitenübertragung
Die Ergebnisse stützen ein Modell, in dem der PfGID-Komplex als molekularer Schiedsrichter fungiert und Menge sowie Aktivität von PfDPL und GD1 zu präzisen Zeitpunkten justiert. Indem er Ubiquitin-Markierungen an intrinsisch flexiblen Regionen dieser Proteine anbringt oder entfernt, kann PfGID schnell regulieren, wie stark PfDPL männlichkeitsspezifische Gene im Kern organisiert und wie fest GD1 wichtige RNA-Nachrichten in einem stillen Zustand hält. Wird dieses Timing gestört, reifen männliche und weibliche Gametozyten nicht aus und der Parasit kann nicht auf die Mücke übergehen. Für den Laien lässt sich festhalten: Malariaparasiten sind auf ein ausgeklügeltes Protein-„Qualitätskontroll“- und Nachrichten-Silencing-Netzwerk angewiesen, um infektiös zu werden. Das Anvisieren von PfGID, PfDPL, GD1 oder deren Wechselwirkungen könnte daher neue Möglichkeiten bieten, den Parasit zu stoppen, bevor er die Mücke erreicht, und so die Übertragungskette zu unterbrechen.
Zitation: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Schlüsselwörter: Malaria-Übertragung, Plasmodium falciparum Gametozyten, Ubiquitin-Ligase, RNA-Translationsrepression, Parasiten-Zellschicksal