Clear Sky Science · pt
Complexo E3 ligase GID/CTLH controla programas de destino celular para o desenvolvimento sexual de Plasmodium falciparum
Por que este estudo sobre malária é importante
A malária ainda mata centenas de milhares de pessoas por ano, e impedir que o parasita passe de humanos para mosquitos é um objetivo central para acabar com a doença. Este artigo revela um sistema de controle oculto dentro do parasita da malária Plasmodium falciparum que decide se suas formas sexuais, chamadas gametócitos, maturam corretamente e se tornam infectantes para mosquitos. Ao explicar como um pequeno grupo de proteínas afina essa decisão, o estudo aponta novos alvos potenciais para drogas ou vacinas que poderiam bloquear a transmissão e ajudar a reduzir a malária no mundo.
O longo caminho do parasita até se tornar infectante
Para se espalhar, P. falciparum precisa converter algumas de suas formas na fase sanguínea em células sexuais especializadas, gametócitos masculinos e femininos, que se desenvolvem ao longo de 10–12 dias. Durante essa lenta transformação, a forma, o metabolismo e a interação do parasita com o glóbulo vermelho são completamente remodelados. Trabalhos anteriores revelaram como um interruptor mestre no DNA do parasita liga a decisão de entrar na via sexual, mas se sabia muito menos sobre como o parasita coordena os milhares de etapas moleculares necessárias para alcançar gametócitos do estágio V totalmente formados e prontos para o mosquito. Os autores suspeitaram que, além de ligar e desligar genes, o parasita também depende da destruição controlada de proteínas para manter o desenvolvimento no caminho certo.
Um árbitro molecular do desenvolvimento sexual
O estudo concentra-se em uma máquina proteica chamada complexo E3 ligase GID/CTLH, aqui denominado PfGID. As E3 ligases agem como dispositivos de marcação, anexando pequenas moléculas de ubiquitina a proteínas escolhidas para marcá-las para degradação ou ajuste. Ao vasculhar o genoma da malária e compará-lo com organismos relacionados, os pesquisadores identificaram seis componentes que se montam em um complexo PfGID. Eles mostraram que essas proteínas formam um andaime conservado dentro do parasita e estão ativas tanto durante o crescimento assexual quanto no desenvolvimento dos gametócitos. Surpreendentemente, quando qualquer uma das subunidades do PfGID foi deletada, o parasita ainda conseguia multiplicar-se nos glóbulos vermelhos, mas o desenvolvimento sexual estagnava por volta da metade do processo. Os gametócitos resultantes pareciam presos em uma forma intermediária e falhavam completamente em infectar mosquitos, revelando o PfGID como essencial para a transmissão.
Como o PfGID direciona destinos masculinos e femininos
Para entender o que dá errado quando o PfGID é perdido, a equipe examinou os padrões globais de RNA e proteína nos parasitas mutantes. Eles descobriram que processos-chave como processamento de RNA, produção proteica e reciclagem de proteínas estavam desregulados, e que proteínas normalmente enriquecidas em gametócitos masculinos e femininos foram fortemente perturbadas. Em particular, a abundância de muitas proteínas específicas de machos caiu, enquanto marcadores de gametócitos maduros foram reduzidos em ambos os sexos. 
Dois braços de controle entrelaçados: organização do DNA e silenciamento de mensagens
O PfDPL parece atuar principalmente na modelagem da linhagem masculina. Ele se localiza no núcleo dos gametócitos em desenvolvimento e associa-se a histonas, remodeladores de cromatina, poros nucleares e outros fatores que governam como o DNA é empacotado e lido. Quando o PfDPL é removido, as proteínas necessárias para replicação do DNA, divisão celular, montagem de flagelos e fertilização em gametas masculinos são fortemente reduzidas, e a exflagelação masculina — a liberação explosiva de formas semelhantes a espermatozoides — quase desaparece. Em contraste, o GD1 opera no citoplasma, onde se agrega em minúsculos grânulos conhecidos como P-bodies. Essas estruturas atuam como centros de armazenamento e silenciamento de mensageiros de RNA. Os autores mostram que o GD1 faz parceria com vários represores traduçãois clássicos e se liga a centenas de mensagens de RNA, incluindo muitas que codificam fatores-chave dos gametócitos. Quando os níveis de GD1 estão ou muito baixos ou muito altos — porque foi deletado, superexpresso ou insuficientemente degradado pelo PfGID — os componentes dos P-bodies ficam desequilibrados e os gametócitos param cedo no desenvolvimento. 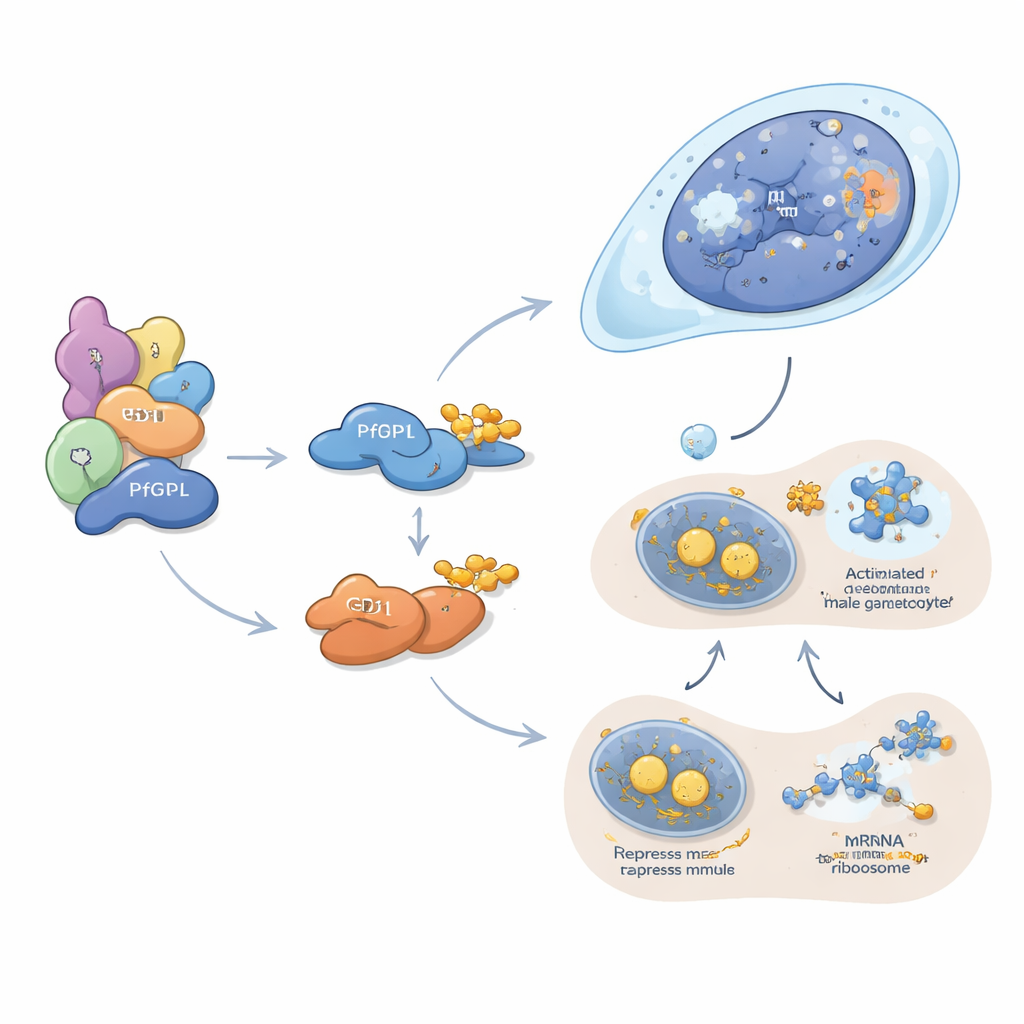
Um temporizador finamente ajustado para a transmissão do parasita
Em conjunto, os achados sustentam um modelo em que o complexo PfGID atua como um árbitro molecular, ajustando a quantidade e a atividade de PfDPL e GD1 em tempos precisos. Ao adicionar ou remover marcas de ubiquitina em regiões intrinsecamente flexíveis dessas proteínas, o PfGID pode ajustar rapidamente o quanto o PfDPL organiza genes específicos de machos no núcleo e o quão firmemente o GD1 mantém mensagens de RNA-chave em estado silenciado. Se esse temporizador for perturbado, gametócitos masculinos e femininos não conseguem maturar, e o parasita não consegue passar para o mosquito. Para um leitor leigo, a conclusão é que os parasitas da malária dependem de uma sofisticada rede de “controle de qualidade” de proteínas e de silenciamento de mensagens para se tornarem infectantes. Alvos como PfGID, PfDPL, GD1 ou suas interações poderiam, portanto, oferecer novas maneiras de congelar o parasita antes que ele chegue ao mosquito, cortando a cadeia de transmissão.
Citação: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Palavras-chave: transmissão da malária, gametócitos de Plasmodium falciparum, ligase de ubiquitina, repressão traducional de RNA, destino celular do parasita