Clear Sky Science · ar
مجمع ليغاز E3 GID/CTLH يتحكم ببرامج مصير الخلية لتطور جنسي في Plasmodium falciparum
لماذا تهم هذه الدراسة عن الملاريا
لا تزال الملاريا تقتل مئات الآلاف من الأشخاص سنوياً، وإيقاف انتقال الطفيل من البشر إلى البعوض هدف أساسي لإنهاء المرض. تكشف هذه الورقة عن نظام رقابي خفي داخل طفيلي الملاريا Plasmodium falciparum يقرر ما إذا كانت الأشكال الجنسية له، المسماة جاميتوسيتات، تنضج بشكل صحيح وتصبح معدية للبعوض. من خلال توضيح كيفية ضبط مجموعة صغيرة من البروتينات لهذا القرار بدقة، تشير الدراسة إلى أهداف جديدة محتملة لأدوية أو لقاحات يمكن أن تمنع الانتقال وتساعد على كبح الملاريا عالمياً.
الطريق الطويل للطفيل ليصبح معدياً
للانتباث، يجب على P. falciparum تحويل بعض أشكاله في مرحلة الدم إلى خلايا جنسية متخصّصة، ذكور وإناث، تطور على مدى 10–12 يوماً. خلال هذا التحول البطيء، يعاد تشكيل شكل الطفيل وطرائق استقلابه وتفاعله مع خلية الدم الحمراء بالكامل. كشفت أعمال سابقة عن مفتاح رئيسي في DNA الطفيل يشغّل قرار الدخول في المسار الجنسي، لكن كان معروفاً أقل كيف ينسّق الطفيل بعدها آلاف الخطوات الجزيئية اللازمة للوصول إلى جاميتوسيتات مكتملة وجاهزة للبعوض من المرحلة V. افترض المؤلفون أنه، بجانب تشغيل وإيقاف الجينات، يعتمد الطفيل أيضاً على تدمير البروتينات المنظم للحفاظ على سير التطور بشكل سليم.
حكم جزيئي لتطور الأشكال الجنسية
تركز الدراسة على آلة بروتينية تسمى مجمع ليغاز E3 GID/CTLH، المسماة هنا PfGID. تعمل ليغازات E3 مثل أجهزة وسم، تُلصق جزيئات يوبكويتين صغيرة بالبروتينات المختارة لوضع علامة عليها بهدف تحللها أو تعديلها. عبر مسح جينوم الملاريا ومقارنته بكائنات ذات صلة، حدّد الباحثون ستة مكوّنات تتجمع لتشكيل مجمع PfGID. أظهروا أن هذه البروتينات تشكّل هيكلاً محفوظاً داخل الطفيل وتكون نشطة طوال فترات النمو اللاجنسي وتكوّن الجاميتوسيتات. اللافت أنه عندما حُذفت أي من وحدات PfGID، ظل الطفيل قادراً على التكاثر داخل خلايا الدم الحمراء، لكن التطور الجنسي توقف في نقطة منتصف المسار تقريباً. بدت الجاميتوسيتات الناتجة عالقة في شكل وسيط وفشلت تماماً في إصابة البعوض، ما يكشف أن PfGID أساسي للانتقال.
كيف يوجّه PfGID المصائر الذكرية والأنثوية
لفهم ما يخطئ عند فقدان PfGID، فحص الفريق أنماط RNA والبروتين العالمية في الطفيليات المتحورة. وجدوا أن عمليات رئيسية مثل معالجة RNA، وإنتاج البروتين، وإعادة تدوير البروتينات كانت مضبوطة بشكل خاطئ، وأن البروتينات التي كانت عادةً غنية في جاميتوسيتات الذكور والإناث تعرّضت لاضطراب كبير. على نحو خاص، انخفضت وفرة العديد من البروتينات الخاصة بالذكور، بينما تراجعت علامات الجاميتوسيتات الناضجة في كلا الجنسين. 
ذراعان رقابيتان متشابكتان: تنظيم DNA وكبت الرسائل
يبدو أن PfDPL يعمل بشكل أساسي في تشكيل السلالة الذكرية. يتموضع في نواة الجاميتوسيتات النامية ويرتبط بالهيستونات، ومعدِّلات الكروماتين، ومسامّ النواة وعوامل أخرى تحكم كيفية تغليف DNA وقراءته. عند إزالة PfDPL، تقلّ بروتينات مطلوبة لتكرار DNA، والانقسام الخلوي، وتجميع الأسواط والخصوبة في الجاميتات الذكرية بشكل حاد، وتكاد عملية خروج الخلايا الذكرية المتحركة (exflagellation)—الإفراز الانفجاري لأشكال تشبه الحيوانات المنوية—تختفي. بالمقابل، يعمل GD1 في السيتوبلازم، حيث يتجمع في حبيبات صغيرة تعرف بأجسام P. تعمل هذه البنى كمخازن ومراكز كبت للرسائل الرسولية (mRNAs). يوضح المؤلفون أن GD1 يتعاون مع عدة كبّات ترجمة كلاسيكية ويرتبط بمئات الرسائل RNA، بما في ذلك العديد التي تشفر عوامل جاميتوسيتية رئيسية. عندما تكون مستويات GD1 منخفضة للغاية أو مرتفعة جداً—سواء بحذفه، أو إفراط التعبير عنه، أو عدم تحلله بشكل كافٍ بواسطة PfGID—تصبح مكونات أجسام P غير متوازنة ويتوقف تطور الجاميتوسيتات مبكراً. 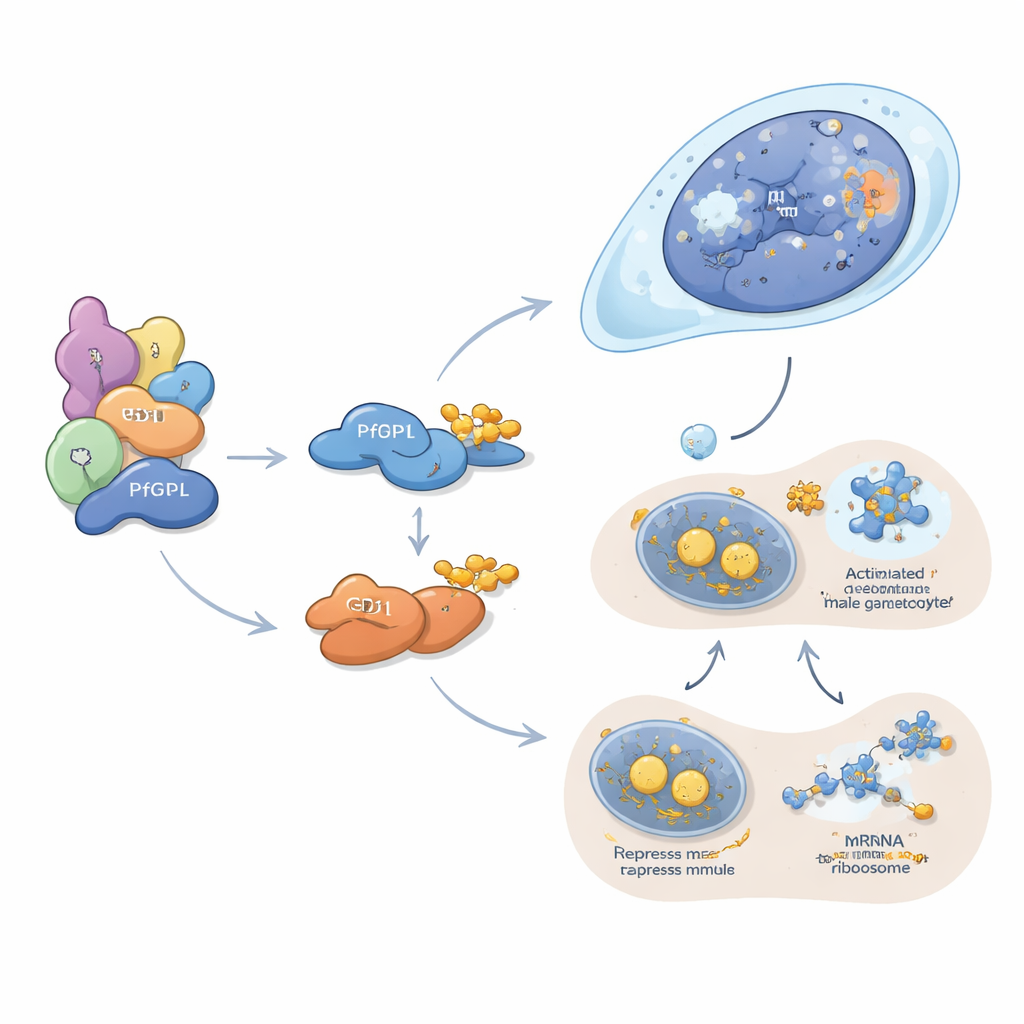
مؤقت مضبوط بدقة لانتقال الطفيل
معاً، تدعم النتائج نموذجاً مفاده أن مجمع PfGID يعمل كحكم جزيئي، يعدّل كمية ونشاط PfDPL وGD1 في أوقات دقيقة. عبر إضافة أو إزالة وسوم اليوبكويتين على مناطق مرنة جوهرياً في هذه البروتينات، يمكن لـ PfGID ضبط سرعة تنظيم PfDPL للجينات الخاصة بالذكور في النواة ومدى إحكام ارتباط GD1 بالرسائل RNA الأساسية في حالة صمت. إذا تعطّل هذا التوقيت، تفشل جاميتوسيتات الذكور والإناث في النضج، ولا يستطيع الطفيل الانتقال إلى البعوض. للمختصر غير المتخصص، الخلاصة أن طفيليات الملاريا تعتمد على شبكة متقنة من "مراقبة جودة" البروتين وقمع الرسائل لتصبح معدية. لذا قد يوفر استهداف PfGID أو PfDPL أو GD1 أو تفاعلاتها طرقاً جديدة لتجميد الطفيل قبل أن يصل إلى البعوض، ما يقطع حلقة الانتقال.
الاستشهاد: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
الكلمات المفتاحية: انتقال الملاريا, جاميتوسيتات Plasmodium falciparum, ليغاز يوبكويتين, قمع الترجمة RNA, مصير خلية الطفيل