Clear Sky Science · fr
Le complexe ubiquitine ligase GID/CTLH contrôle les programmes de destinée cellulaire pour le développement sexuel de Plasmodium falciparum
Pourquoi cette étude sur le paludisme est importante
Le paludisme tue encore des centaines de milliers de personnes chaque année, et empêcher le parasite de passer de l’homme au moustique est un objectif clé pour mettre fin à la maladie. Cet article révèle un système de contrôle caché à l’intérieur du parasite Plasmodium falciparum qui décide si ses formes sexuelles, appelées gamétocytes, mûrissent correctement et deviennent infectieuses pour les moustiques. En expliquant comment un petit groupe de protéines affine cette décision, l’étude identifie de nouvelles cibles potentielles pour des médicaments ou des vaccins capables de bloquer la transmission et d’aider à freiner le paludisme dans le monde.
La longue route du parasite pour devenir infectieux
Pour se propager, P. falciparum doit convertir certaines de ses formes sanguines en cellules sexuelles spécialisées, gamétocytes mâles et femelles, qui se développent sur 10–12 jours. Au cours de cette lente transformation, la forme, le métabolisme et l’interaction du parasite avec le globule rouge sont entièrement remodelés. Des travaux antérieurs avaient montré comment un commutateur maître dans l’ADN du parasite déclenche la décision d’entrer dans la voie sexuelle, mais on savait beaucoup moins comment le parasite coordonne ensuite les milliers d’étapes moléculaires nécessaires pour atteindre des gamétocytes de stade V pleinement formés et prêts pour le moustique. Les auteurs ont supposé que, au-delà de l’activation ou de la répression des gènes, le parasite dépend aussi d’une destruction protéique contrôlée pour maintenir le développement sur la bonne voie.
Un arbitre moléculaire du développement sexuel
L’étude se concentre sur une machinerie protéique appelée complexe E3 ligase GID/CTLH, nommé ici PfGID. Les E3 ligases fonctionnent comme des dispositifs d’étiquetage, fixant de petites molécules d’ubiquitine sur des protéines choisies pour les marquer en vue de leur dégradation ou de leur modulation. En parcourant le génome du paludisme et en le comparant à des organismes apparentés, les chercheurs ont identifié six composants qui s’assemblent en un complexe PfGID. Ils ont montré que ces protéines forment une charpente conservée au sein du parasite et sont actives tant pendant la croissance asexuée que durant le développement des gamétocytes. De manière frappante, lorsque l’une quelconque des sous-unités PfGID était supprimée, le parasite pouvait encore se multiplier dans les globules rouges, mais le développement sexuel s’arrêtait à mi-parcours. Les gamétocytes résultants semblaient bloqués dans une morphologie intermédiaire et ne pouvaient absolument pas infecter les moustiques, révélant que PfGID est essentiel pour la transmission.
Comment PfGID oriente les destins mâle et femelle
Pour comprendre ce qui se passe quand PfGID est absent, l’équipe a examiné les profils globaux d’ARN et de protéines dans les parasites mutants. Ils ont constaté que des processus clés tels que le traitement des ARN, la production de protéines et le recyclage protéique étaient déréglés, et que les protéines normalement enrichies dans les gamétocytes mâles et femelles étaient fortement perturbées. En particulier, l’abondance de nombreuses protéines spécifiques aux mâles chutait, tandis que les marqueurs de gamétocytes matures diminuaient dans les deux sexes. 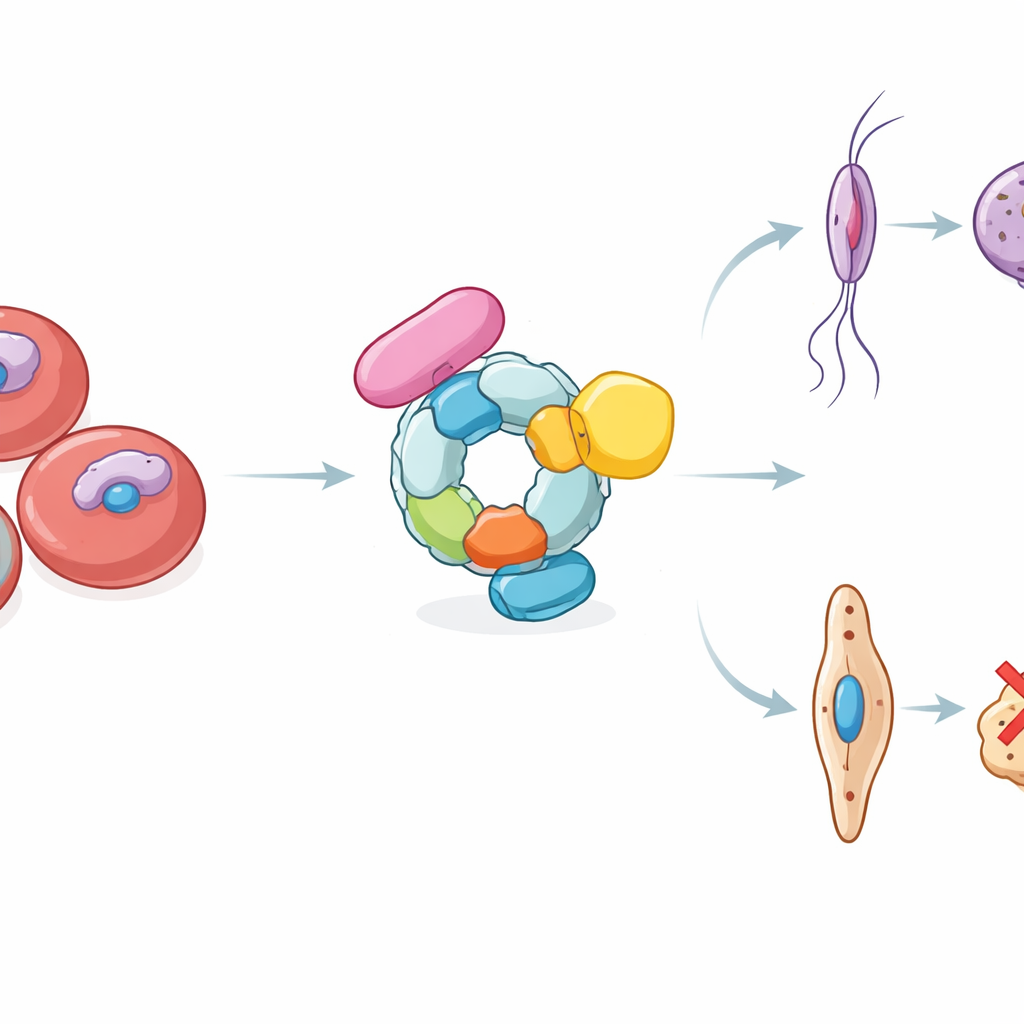
Deux bras de contrôle imbriqués : organisation de l’ADN et silencement des messages
PfDPL semble agir principalement dans la formation de la lignée mâle. Il se localise au noyau des gamétocytes en développement et s’associe aux histones, aux remodelleurs de chromatine, aux pores nucléaires et à d’autres facteurs qui gouvernent l’emballage et la lecture de l’ADN. Lorsque PfDPL est supprimé, les protéines nécessaires à la réplication de l’ADN, à la division cellulaire, au montage des flagelles et à la fécondation des gamètes mâles sont fortement réduites, et l’exflagellation mâle — la libération explosive de formes semblables à des spermatozoïdes — disparaît presque complètement. En revanche, GD1 fonctionne dans le cytoplasme, où il s’assemble en petits granules connus sous le nom de P-bodies. Ces structures servent de centres de stockage et de silencement pour les ARNm. Les auteurs montrent que GD1 s’associe à plusieurs répresseurs traductionnels classiques et lie des centaines de messages ARN, y compris beaucoup qui codent des facteurs clés des gamétocytes. Lorsque les niveaux de GD1 sont trop faibles ou trop élevés — parce qu’il est supprimé, surexprimé, ou insuffisamment dégradé par PfGID — les composants des P-bodies se déséquilibrent et les gamétocytes s’arrêtent tôt dans leur développement. 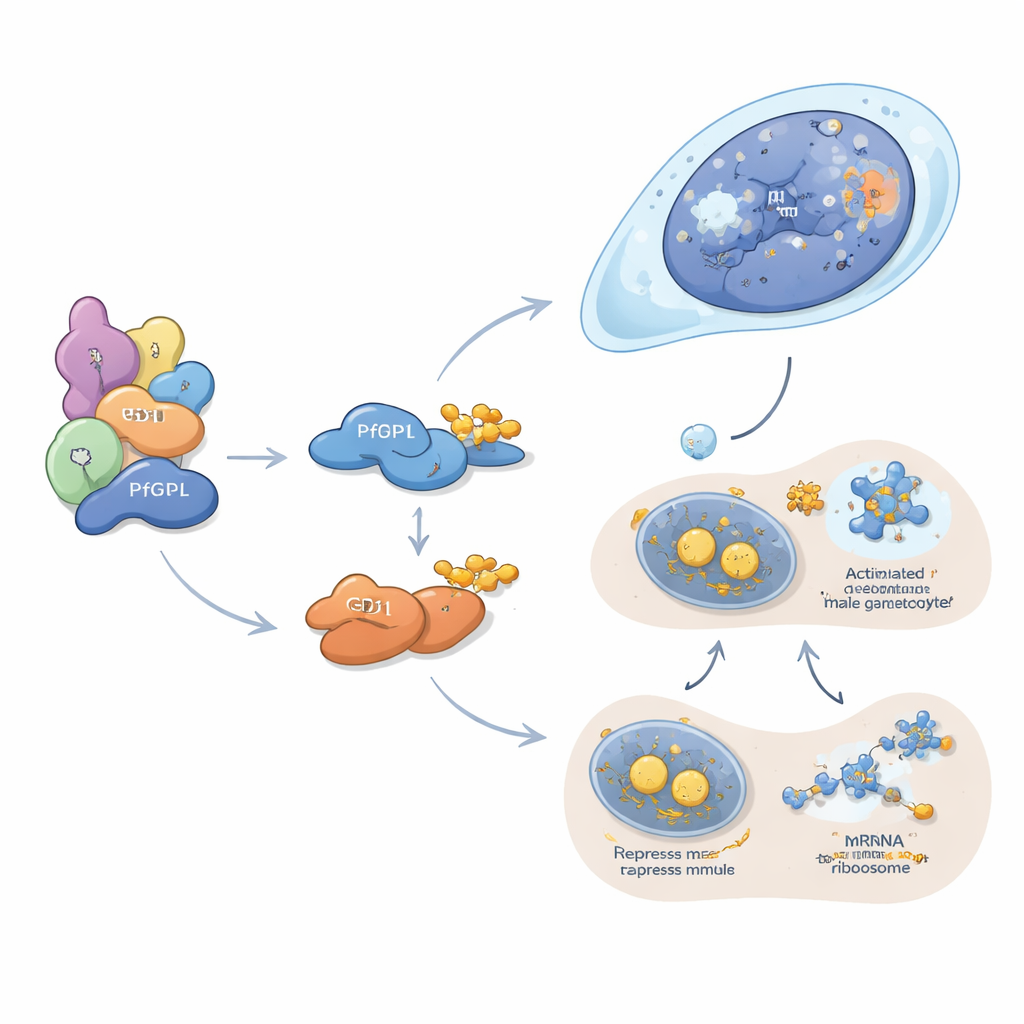
Une horloge finement réglée pour la transmission du parasite
Ensemble, les résultats soutiennent un modèle dans lequel le complexe PfGID agit comme un arbitre moléculaire, ajustant la quantité et l’activité de PfDPL et de GD1 à des moments précis. En ajoutant ou en retirant des étiquettes d’ubiquitine sur des régions intrinsèquement flexibles de ces protéines, PfGID peut ajuster rapidement l’intensité de l’organisation des gènes spécifiques aux mâles par PfDPL dans le noyau et la sévérité du maintien en silence des messages ARNm par GD1. Si ce timing est perturbé, les gamétocytes mâles et femelles ne parviennent pas à maturité et le parasite ne peut pas passer au moustique. Pour un lecteur non spécialiste, la conclusion est que les parasites du paludisme dépendent d’un réseau sophistiqué de « contrôle qualité » protéique et de silencement des messages pour devenir infectieux. Cibler PfGID, PfDPL, GD1 ou leurs interactions pourrait donc offrir de nouvelles stratégies pour bloquer le parasite avant qu’il n’atteigne le moustique, coupant ainsi la chaîne de transmission.
Citation: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Mots-clés: transmission du paludisme, gamétocytes de Plasmodium falciparum, ligase ubiquitine, répression traductionnelle de l’ARN, destinée cellulaire du parasite