Clear Sky Science · ru
Комплекс лигазы E3 GID/CTLH контролирует программы клеточной судьбы для полового развития Plasmodium falciparum
Почему это исследование малярии важно
Малярия по-прежнему уносит сотни тысяч жизней ежегодно, и прерывание перехода паразита от человека к комару — ключевая задача в борьбе с болезнью. В этой работе обнаружена скрытая система контроля внутри паразита Plasmodium falciparum, которая определяет, созревают ли его половые формы, называемые гаметоцитами, правильно и становятся ли они инфекционными для комаров. Объясняя, как небольшая группа белков точно настраивает это решение, исследование указывает на новые потенциальные мишени для лекарств или вакцин, которые могли бы блокировать передачу и помочь сдержать малярию в мире.
Долгий путь паразита к инфекционности
Для распространения P. falciparum должен превратить часть своих форм в крови в специализированные половые клетки — мужские и женские гаметоциты, которые развиваются в течение 10–12 дней. В ходе этой медленной трансформации форма, метаболизм и взаимодействие паразита с эритроцитом полностью перестраиваются. Ранее показали, как главный переключатель в ДНК паразита включает решение о вступлении в половую траекторию, но гораздо меньше было известно о том, как затем координируются тысячи молекулярных шагов, необходимых для достижения полностью сформированных, готовых к комару гаметоцитов стадии V. Авторы предположили, что помимо включения и выключения генов паразит опирается и на контролируемое разрушение белков, чтобы развитие шло по плану.
Молекулярный рефери полового развития
В центре внимания исследования — белковый аппарат, называемый комплексом лигазы E3 GID/CTLH, здесь обозначенный как PfGID. Лигазы E3 действуют как устройства для маркировки, прикрепляя маленькие молекулы убиквитина к выбранным белкам, помечая их для деградации или модификации. Просканировав геном малярийного паразита и сопоставив его с родственными организмами, исследователи выявили шесть компонентов, которые собираются в комплекс PfGID. Они показали, что эти белки формируют консервативный каркас внутри паразита и активны как в бесполом росте, так и в развитии гаметоцитов. Поразительно, но при удалении любого из субъединиц PfGID паразит всё ещё мог размножаться в эритроцитах, однако половое развитие останавливалось примерно на середине пути. Получившиеся гаметоциты выглядели застрявшими на промежуточной стадии и полностью утратили способность инфицировать комаров, что выявляет PfGID как необходимый для передачи фактор.
Как PfGID направляет мужские и женские судьбы
Чтобы понять, что идёт не так при потере PfGID, команда изучила глобальные профили РНК и белков в мутантных паразитах. Они обнаружили, что ключевые процессы, такие как обработка РНК, синтез белка и утилизация белков, оказались нарушены, и что белки, обычно обогащённые в мужских и женских гаметоцитах, сильно дезорганизованы. В частности, количество многих мужских специфических белков снизилось, тогда как маркеры зрелых гаметоцитов уменьшились в обоих полах. 
Две переплетённые ветви управления: организация ДНК и молчание сообщений
PfDPL, по-видимому, действует главным образом в формировании мужской линии. Он локализуется в ядре развивающихся гаметоцитов и ассоциируется с гистонами, ремоделлерами хроматина, ядерными порами и другими факторами, управляющими упаковкой и считыванием ДНК. При удалении PfDPL резко сокращается количество белков, необходимых для репликации ДНК, деления клеток, сборки жгутика и оплодотворения у мужских гамет, а мужская эксфлагелляция — взрывной выброс сперматозоидоподобных форм — практически исчезает. Напротив, GD1 действует в цитоплазме, где он собирается в крошечные гранулы, известные как P-бодисы. Эти структуры служат хранилищем и центрами молчания для мРНК. Авторы показывают, что GD1 взаимодействует с несколькими классическими репрессорами трансляции и связывает сотни РНК-сообщений, включая многие, кодирующие ключевые факторы гаметоцитов. Когда уровни GD1 слишком низки или слишком высоки — из‑за удаления, сверхэкспрессии или недостаточной деградации PfGID — компоненты P-бодисов теряют равновесие, и гаметоциты останавливаются на ранних стадиях развития. 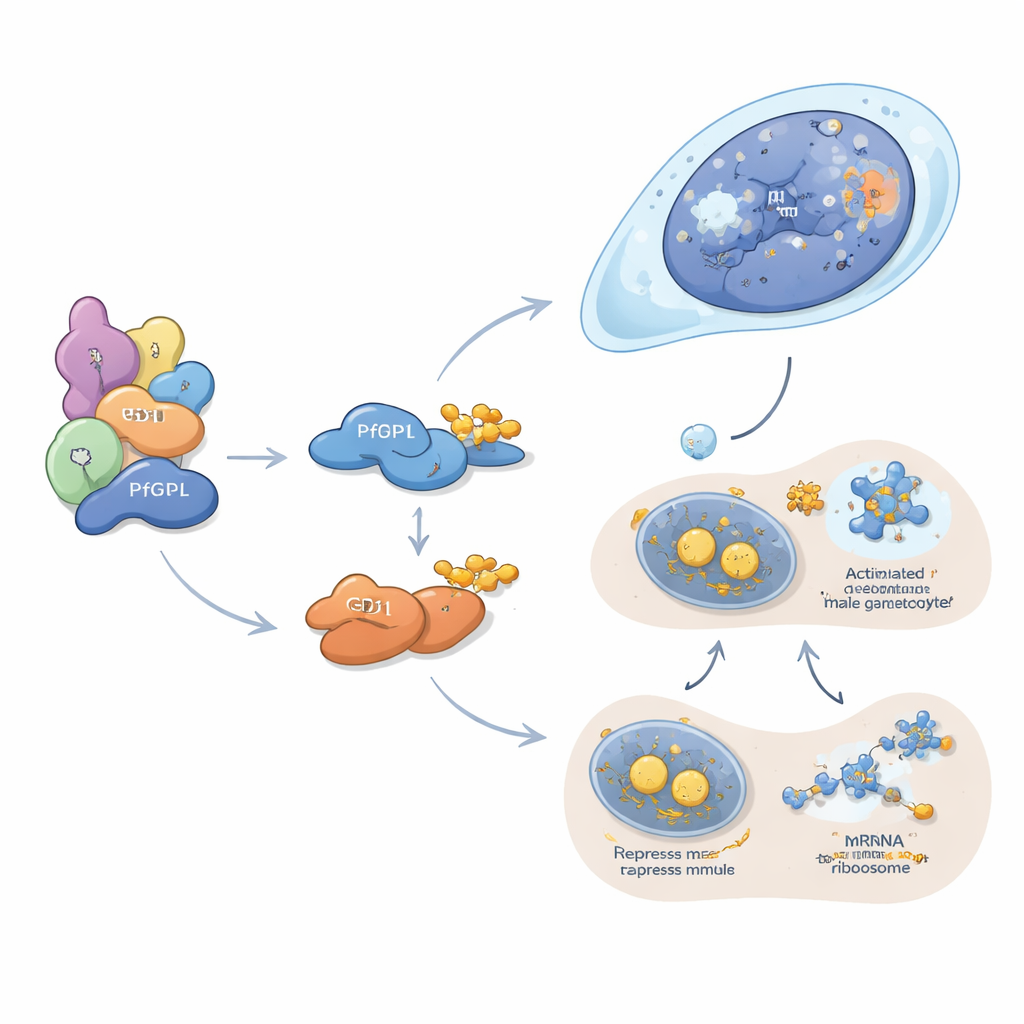
Точно настроенный таймер для передачи паразита
Вместе результаты поддерживают модель, в которой комплекс PfGID действует как молекулярный рефери, настраивая количество и активность PfDPL и GD1 в строго определённые моменты. Добавляя или снимая убиквитиновые метки на intrinsically гибких областях этих белков, PfGID может быстро регулировать, насколько сильно PfDPL организует мужеспецифические гены в ядре и насколько прочно GD1 удерживает ключевые РНК-сообщения в молчаливом состоянии. При нарушении этого тайминга мужские и женские гаметоциты не созревают, и паразит теряет способность переходить к комару. Для неспециалиста основной вывод таков: малярийные паразиты опираются на сложную сеть «контроля качества» белков и молчания сообщений, чтобы стать инфекционными. Нацеливание на PfGID, PfDPL, GD1 или их взаимодействия может поэтому предложить новые способы заморозить паразита до того, как он попадёт в комара, разрывая цепочку передачи.
Цитирование: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Ключевые слова: передача малярии, гаметоциты Plasmodium falciparum, убиквитин-лигаза, трансляционное репрессирование РНК, клеточная судьба паразита