Clear Sky Science · es
El complejo ligasa E3 GID/CTLH controla programas de destino celular para el desarrollo sexual de Plasmodium falciparum
Por qué importa este estudio sobre la malaria
La malaria sigue causando cientos de miles de muertes cada año, y evitar que el parásito pase de los humanos a los mosquitos es un objetivo clave para terminar con la enfermedad. Este artículo descubre un sistema de control oculto dentro del parásito de la malaria Plasmodium falciparum que decide si sus formas sexuales, llamadas gametocitos, maduran correctamente y se vuelven infecciosas para los mosquitos. Al explicar cómo un pequeño grupo de proteínas afina esta decisión, el estudio señala nuevos posibles blancos para fármacos o vacunas que podrían bloquear la transmisión y ayudar a reducir la malaria en todo el mundo.
El largo camino del parásito para volverse infeccioso
Para propagarse, P. falciparum debe convertir algunas de sus formas en sangre en células sexuales especializadas, gametocitos masculinos y femeninos, que se desarrollan durante 10–12 días. Durante esta lenta transformación, la forma, el metabolismo y la interacción del parásito con el glóbulo rojo se remodelan por completo. Investigaciones previas habían revelado cómo un interruptor maestro en el ADN del parásito activa la decisión de entrar en la vía sexual, pero se sabía mucho menos sobre cómo el parásito coordina después los miles de pasos moleculares necesarios para alcanzar gametocitos de estadio V plenamente formados y listos para el mosquito. Los autores sospechaban que, además de encender y apagar genes, el parásito también depende de la destrucción controlada de proteínas para mantener el desarrollo en marcha.
Un árbitro molecular para el desarrollo sexual
El estudio se centra en una maquinaria proteica llamada complejo ligasa E3 GID/CTLH, aquí denominado PfGID. Las ligasas E3 actúan como dispositivos de etiquetado, uniendo pequeñas moléculas de ubiquitina a proteínas seleccionadas para marcarlas para su degradación o ajuste. Al explorar el genoma de la malaria y comparar con organismos relacionados, los investigadores identificaron seis componentes que se ensamblan en un complejo PfGID. Mostraron que estas proteínas forman un andamiaje conservado dentro del parásito y están activas tanto durante el crecimiento asexual como durante el desarrollo de los gametocitos. De forma llamativa, cuando se eliminó cualquiera de las subunidades de PfGID, el parásito aún podía multiplicarse en los glóbulos rojos, pero el desarrollo sexual se detenía alrededor de la mitad del proceso. Los gametocitos resultantes parecían atascados en una forma intermedia y fracasaban por completo en infectar a los mosquitos, revelando que PfGID es esencial para la transmisión.
Cómo PfGID dirige los destinos masculinos y femeninos
Para entender qué falla cuando se pierde PfGID, el equipo examinó los patrones globales de ARN y proteínas en los parásitos mutantes. Encontraron que procesos clave como el procesamiento del ARN, la producción de proteínas y el reciclaje proteico estaban desregulados, y que las proteínas normalmente enriquecidas en gametocitos masculinos y femeninos se veían fuertemente perturbadas. En particular, la abundancia de muchas proteínas específicas de los machos disminuyó, mientras que los marcadores de gametocitos maduros se redujeron en ambos sexos. 
Dos brazos de control entrelazados: organización del ADN y silenciamiento de mensajes
PfDPL parece actuar principalmente en la configuración de la línea masculina. Se localiza en el núcleo de los gametocitos en desarrollo y se asocia con histonas, remodeladores de la cromatina, poros nucleares y otros factores que gobiernan cómo se empaqueta y lee el ADN. Cuando se elimina PfDPL, las proteínas necesarias para la replicación del ADN, la división celular, el ensamblaje de flagelos y la fertilización en los gametos masculinos se reducen drásticamente, y la exflagelación masculina—la liberación explosiva de formas parecidas a espermatozoides—casi desaparece. En contraste, GD1 actúa en el citoplasma, donde se agrupa en diminutos gránulos conocidos como cuerpos P. Estas estructuras actúan como depósitos y centros de silenciamiento para los ARN mensajeros. Los autores muestran que GD1 se asocia con varios represores clásicos de la traducción y se une a cientos de mensajes de ARN, incluidos muchos que codifican factores clave de los gametocitos. Cuando los niveles de GD1 son demasiado bajos o demasiado altos—porque se elimina, se sobreexpresa o no se degrada lo suficiente por PfGID—los componentes de los cuerpos P se desequilibran y los gametocitos se detienen temprano en su desarrollo. 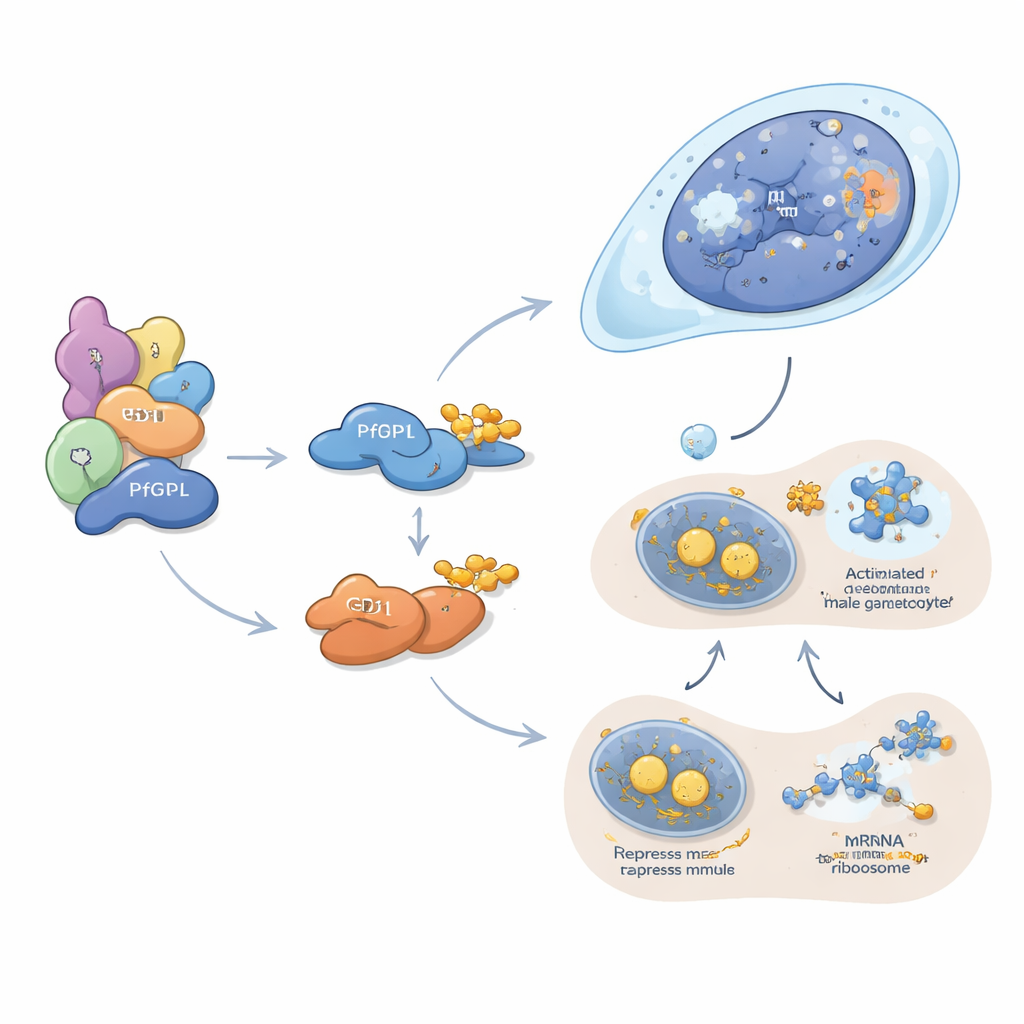
Un temporizador finamente ajustado para la transmisión del parásito
En conjunto, los hallazgos respaldan un modelo en el que el complejo PfGID actúa como un árbitro molecular, ajustando la cantidad y la actividad de PfDPL y GD1 en momentos precisos. Al añadir o quitar marcas de ubiquitina en regiones intrínsecamente flexibles de estas proteínas, PfGID puede ajustar rápidamente con qué intensidad PfDPL organiza genes específicos de los machos en el núcleo y con qué firmeza GD1 mantiene mensajes de ARN clave en un estado silencioso. Si este temporizador se altera, los gametocitos masculinos y femeninos no maduran y el parásito no puede pasar al mosquito. Para el lector general, la conclusión es que los parásitos de la malaria dependen de una sofisticada red de “control de calidad” proteico y de silenciamiento de mensajes para volverse infecciosos. Dirigirse a PfGID, PfDPL, GD1 o sus interacciones podría, por tanto, ofrecer nuevas formas de bloquear al parásito antes de que llegue al mosquito, cortando la cadena de transmisión.
Cita: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Palabras clave: transmisión de la malaria, gametocitos de Plasmodium falciparum, ligasa de ubiquitina, represión de la traducción del ARN, destino celular del parásito