Clear Sky Science · it
Il complesso ligasi E3 GID/CTLH controlla i programmi di destino cellulare per lo sviluppo sessuale di Plasmodium falciparum
Perché questo studio sulla malaria è importante
La malaria continua a uccidere centinaia di migliaia di persone ogni anno, e impedire che il parassita passi dagli esseri umani alle zanzare è un obiettivo chiave per porre fine alla malattia. Questo articolo svela un sistema di controllo nascosto all’interno del parassita della malaria Plasmodium falciparum che decide se le sue forme sessuali, chiamate gametociti, maturano correttamente e diventano infettive per le zanzare. Spiegando come un piccolo gruppo di proteine modula finemente questa decisione, lo studio indica nuovi possibili bersagli per farmaci o vaccini che potrebbero bloccare la trasmissione e contribuire a contenere la malaria a livello mondiale.
Il lungo percorso del parassita per diventare infettivo
Per diffondersi, P. falciparum deve trasformare alcune delle sue forme nel sangue in cellule sessuali specializzate, gametociti maschili e femminili, che si sviluppano in 10–12 giorni. Durante questa lenta trasformazione, la forma del parassita, il suo metabolismo e l’interazione con il globulo rosso vengono completamente rimodellati. Lavori precedenti avevano mostrato come un interruttore maestro nel DNA del parassita attivi la decisione di entrare nella via sessuale, ma si sapeva molto meno su come il parassita coordini poi le migliaia di passaggi molecolari necessari a ottenere gametociti di stadio V completi e pronti per la zanzara. Gli autori sospettavano che, oltre ad accendere e spegnere geni, il parassita si affidi anche a una distruzione proteica controllata per mantenere lo sviluppo sulla giusta traiettoria.
Un arbitro molecolare per lo sviluppo sessuale
Lo studio si concentra su una macchina proteica chiamata complesso ligasi E3 GID/CTLH, qui denominata PfGID. Le ligasi E3 funzionano come dispositivi di marcatura, attaccando piccole molecole di ubiquitina a proteine scelte per segnarle alla degradazione o alla regolazione. Scansionando il genoma della malaria e confrontandolo con organismi correlati, i ricercatori hanno identificato sei componenti che si assemblano in un complesso PfGID. Hanno mostrato che queste proteine formano uno scheletro conservato all’interno del parassita e sono attive sia durante la crescita asessuale sia durante lo sviluppo dei gametociti. Sorprendentemente, quando uno qualsiasi dei subunità PfGID veniva eliminato, il parassita poteva ancora moltiplicarsi nei globuli rossi, ma lo sviluppo sessuale si arrestava intorno alla metà del processo. I gametociti risultanti apparivano bloccati in una forma intermedia e non riuscivano affatto a infettare le zanzare, rivelando PfGID come essenziale per la trasmissione.
Come PfGID indirizza i destini maschili e femminili
Per capire cosa andasse storto in assenza di PfGID, il team ha esaminato i profili globali di RNA e proteine nei parassiti mutanti. Hanno osservato che processi chiave come l’elaborazione dell’RNA, la produzione proteica e il riciclo delle proteine erano disregolati, e che le proteine normalmente arricchite nei gametociti maschili e femminili risultavano fortemente alterate. In particolare, l’abbondanza di molte proteine specifiche dei maschi diminuiva, mentre i marker dei gametociti maturi erano ridotti in entrambi i sessi. 
Due bracci di controllo intrecciati: organizzazione del DNA e silenziamento dei messaggi
PfDPL sembra operare principalmente nel plasmare la linea maschile. Si localizza nel nucleo dei gametociti in sviluppo e si associa a istoni, rimodellatori della cromatina, pori nucleari e altri fattori che governano il modo in cui il DNA è impacchettato e letto. Quando PfDPL viene rimosso, le proteine necessarie per la replicazione del DNA, la divisione cellulare, l’assemblaggio degli organelli flagellari e la fecondazione nei gameti maschili risultano fortemente ridotte, e l’esflagellazione maschile—il rilascio esplosivo di forme simili a spermatozoi—quasi scompare. Al contrario, GD1 opera nel citoplasma, dove si raggruppa in minuscole strutture chiamate P-body. Queste strutture fungono da depositi e centri di silenziamento per gli mRNA. Gli autori mostrano che GD1 si associa a diversi repressori tradizionali della traduzione e lega centinaia di messaggi RNA, inclusi molti che codificano fattori chiave dei gametociti. Quando i livelli di GD1 sono troppo bassi o troppo alti—perché viene eliminato, sovraespresso o degradato in modo insufficiente da PfGID—i componenti dei P-body diventano sbilanciati e i gametociti si arrestano precocemente nello sviluppo. 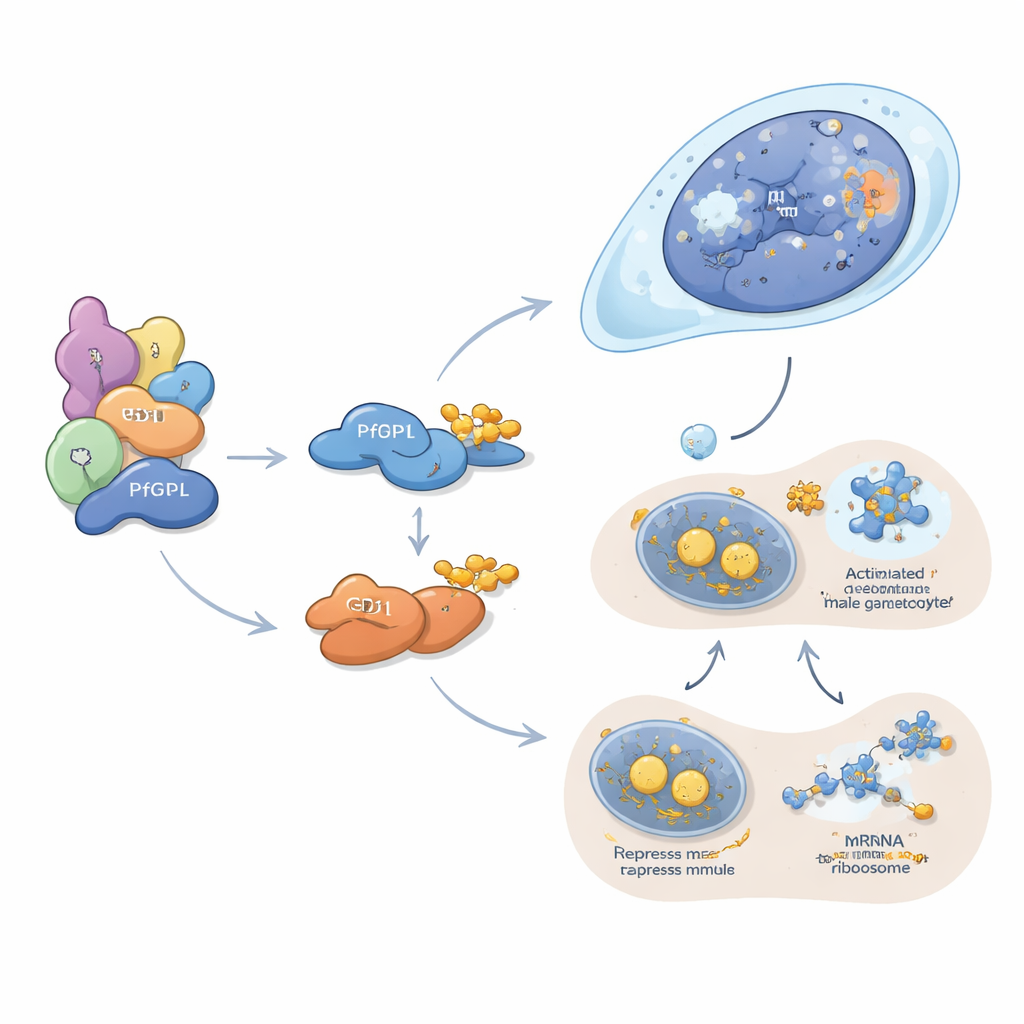
Un timer finemente regolato per la trasmissione del parassita
Nel complesso, i risultati supportano un modello in cui il complesso PfGID agisce come un arbitro molecolare, modulando quantità e attività di PfDPL e GD1 in momenti precisi. Aggiungendo o rimuovendo marchi di ubiquitina su regioni intrinsecamente flessibili di queste proteine, PfGID può adattare rapidamente quanto PfDPL organizza i geni specifici dei maschi nel nucleo e quanto saldamente GD1 mantiene certi messaggi RNA in uno stato silente. Se questo timing è disturbato, i gametociti maschili e femminili non maturano e il parassita non può passare alla zanzara. Per il lettore non specialistico, la conclusione è che i parassiti della malaria dipendono da una sofisticata rete di “controllo qualità” proteico e di silenziamento dei messaggi per diventare infettivi. Mirare a PfGID, PfDPL, GD1 o alle loro interazioni potrebbe dunque offrire nuovi modi per bloccare il parassita prima che raggiunga la zanzara, interrompendo la catena di trasmissione.
Citazione: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Parole chiave: trasmissione della malaria, gametociti di Plasmodium falciparum, ligasi dell’ubiquitina, repressione traduzionale dell’RNA, destino cellulare del parassita