Clear Sky Science · pl
Kompleks ligazy E3 GID/CTLH kontroluje programy losu komórkowego dla rozwoju płciowego Plasmodium falciparum
Dlaczego to badanie malarii ma znaczenie
Malaria nadal zabija setki tysięcy ludzi rocznie, a powstrzymanie przenoszenia pasożyta z człowieka na komara jest kluczowym celem w walce z chorobą. Artykuł ujawnia ukryty system kontroli wewnątrz pasożyta Plasmodium falciparum, który decyduje, czy jego formy płciowe, zwane gametocytami, dojrzewają prawidłowo i stają się zakaźne dla komarów. Wyjaśniając, jak niewielka grupa białek precyzyjnie dostraja tę decyzję, badanie wskazuje nowe cele dla leków lub szczepionek, które mogłyby zablokować transmisję i pomóc zahamować malarię na świecie.
Długa droga pasożyta do stania się zakaźnym
Aby się rozprzestrzeniać, P. falciparum musi przekształcić część swoich postaci krwinkowych w wyspecjalizowane komórki płciowe, gametocyty męskie i żeńskie, które rozwijają się przez 10–12 dni. W trakcie tej powolnej transformacji kształt pasożyta, jego metabolizm i sposób interakcji z krwinką są całkowicie przebudowywane. Wcześniejsze prace ujawniły, jak główny przełącznik w genomie pasożyta uruchamia decyzję o wejściu na ścieżkę płciową, ale wiadomo znacznie mniej o tym, jak pasożyt koordynuje tysiące molekularnych kroków potrzebnych, by osiągnąć w pełni uformowane, gotowe dla komara gametocyty stadium V. Autorzy podejrzewali, że poza włączaniem i wyłączaniem genów pasożyt polega również na kontrolowanym niszczeniu białek, aby utrzymać rozwój na właściwej drodze.
Molekularny sędzia rozwoju płciowego
Badanie koncentruje się na maszynie białkowej zwanej kompleksem ligazy E3 GID/CTLH, tutaj określanym jako PfGID. Ligazy E3 działają jak urządzenia tagujące, przyłączając małe cząsteczki ubiquityny do wybranych białek, oznaczając je do degradacji lub modyfikacji. Przeszukując genom malarii i porównując go z pokrewnymi organizmami, naukowcy zidentyfikowali sześć składników, które łączą się w kompleks PfGID. Wykazali, że te białka tworzą zachowany rusztowanie wewnątrz pasożyta i są aktywne zarówno podczas wzrostu bezpłciowego, jak i rozwoju gametocytów. Co istotne, gdy usunięto którykolwiek ze podjednostek PfGID, pasożyt nadal mógł się rozmnażać w krwinkach, ale rozwój płciowy zatrzymywał się mniej więcej w połowie drogi. Powstałe gametocyty wyglądały na utknione na etapie pośrednim i całkowicie nie infekowały komarów, co ujawniło PfGID jako niezbędny dla transmisji.
Jak PfGID kieruje losami męskimi i żeńskimi
Aby zrozumieć, co idzie nie tak po utracie PfGID, zespół przeanalizował globalne wzorce RNA i białek w mutantach pasożyta. Stwierdzono, że kluczowe procesy, takie jak przetwarzanie RNA, produkcja białek i recykling białek, były zaburzone, a białka zwykle wzbogacone w gametocytach męskich i żeńskich były silnie zmienione. W szczególności obfitość wielu białek specyficznych dla płci męskiej spadła, podczas gdy markery dojrzałych gametocytów zostały zredukowane w obu płciach. 
Dwa splecione ramiona kontroli: organizacja DNA i wyciszanie przekazów
PfDPL wydaje się działać głównie przy kształtowaniu linii męskiej. Lokalizuje się w jądrze rozwijających się gametocytów i łączy się z histonami, remodelerami chromatyny, porami jądrowymi oraz innymi czynnikami kontrolującymi opakowanie i odczyt DNA. Po usunięciu PfDPL białka potrzebne do replikacji DNA, podziału komórkowego, składania wici i zapłodnienia w gametach męskich są wyraźnie zredukowane, a eksflagelacja męska — gwałtowne uwolnienie form przypominających plemniki — niemal zanika. W przeciwieństwie do tego GD1 działa w cytoplazmie, gdzie grupuje się w małe grudki znane jako ciała P. Struktury te pełnią funkcję magazynów i centrów wyciszania dla mRNA. Autorzy pokazują, że GD1 współpracuje z kilkoma klasycznymi represorami translacji i wiąże setki komunikatów RNA, w tym wiele kodujących kluczowe czynniki gametocytarne. Gdy poziomy GD1 są zbyt niskie lub zbyt wysokie — z powodu delecji, nadekspresji lub niewystarczającej degradacji przez PfGID — składniki ciał P ulegają rozchwianiu, a gametocyty zatrzymują się we wczesnym stadium rozwoju. 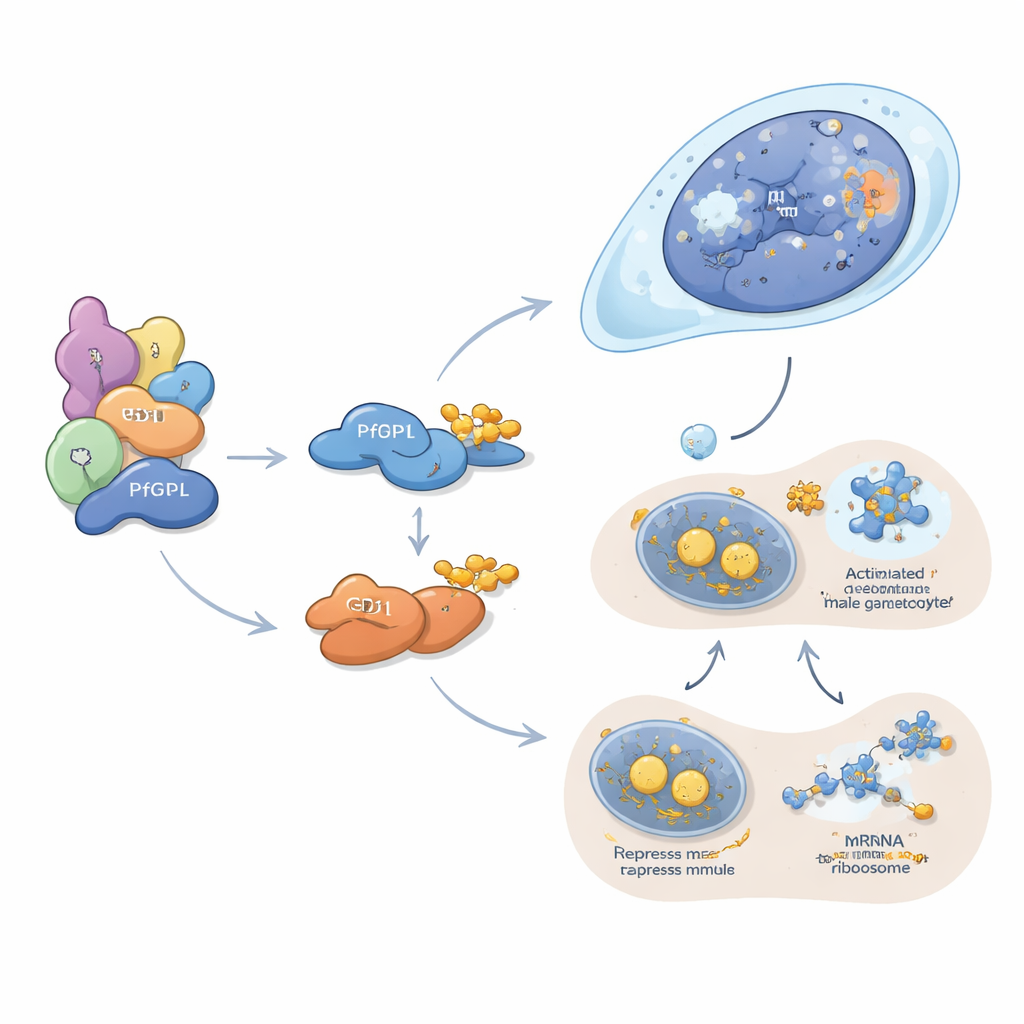
Precyzyjnie dostrojony zegar transmisji pasożyta
Wyniki wspierają model, w którym kompleks PfGID działa jako molekularny sędzia, regulując ilość i aktywność PfDPL oraz GD1 w precyzyjnych momentach. Poprzez dodawanie lub usuwanie znaczników ubiquityny na wewnętrznie elastycznych regionach tych białek PfGID może szybko dostosować, jak silnie PfDPL organizuje geny specyficzne dla płci męskiej w jądrze oraz jak ściśle GD1 utrzymuje kluczowe komunikaty RNA w stanie uśpienia. Jeśli to timing zostanie zaburzony, gametocyty męskie i żeńskie nie dojrzewają i pasożyt nie może przenieść się na komara. Dla czytelnika popularnonaukowego wniosek jest taki, że pasożyty malarii polegają na wyrafinowanej sieci kontroli jakości białek i wyciszania przekazów, by stać się zakaźnymi. Celowanie w PfGID, PfDPL, GD1 lub ich interakcje mogłoby więc dać nowe sposoby zamrożenia pasożyta, zanim kiedykolwiek dotrze do komara, przerywając łańcuch transmisji.
Cytowanie: Marapana, D.S., Lopaticki, S., Balan, B. et al. GID/CTLH E3 ligase complex control cell fate programs for sexual development of Plasmodium falciparum. Nat Commun 17, 3497 (2026). https://doi.org/10.1038/s41467-026-69183-9
Słowa kluczowe: transmisja malarii, gametocyty Plasmodium falciparum, ligaza ubiquityny, tłumieniе translacji RNA, los komórkowy pasożyta