Clear Sky Science · zh
用EGOLD解码染色质环境在CRISPR脱靶效应中的作用
为何微小的DNA变动会产生重大副作用
CRISPR基因编辑曾带来通过在细胞内精确改变DNA来治愈多种遗传性疾病的希望。但同样能修复错误基因的工具,也可能意外改变基因组的其他部分,产生“脱靶”变异。本研究引入了一种在人体细胞中直接绘制这些非预期编辑的新方法,并揭示了DNA在细胞内折叠的松紧程度在决定脱靶发生位置上起到关键作用。
超越DNA字母本身的视角
大多数关于CRISPR安全性的研究都集中在DNA序列本身:哪些由A、C、G、T组成的字符串最容易被切割或改变。然而在活细胞中,DNA缠绕在蛋白质上并被折叠成更开放或更封闭的状态,这种景观被称为染色质。开放区域更容易被细胞机器访问,而封闭区域更受屏蔽。作者怀疑这种局部的DNA包装会悄悄引导CRISPR工具犯错的地点,但现有测试没有覆盖足够多的真实基因组位点来深入研究这一效应。
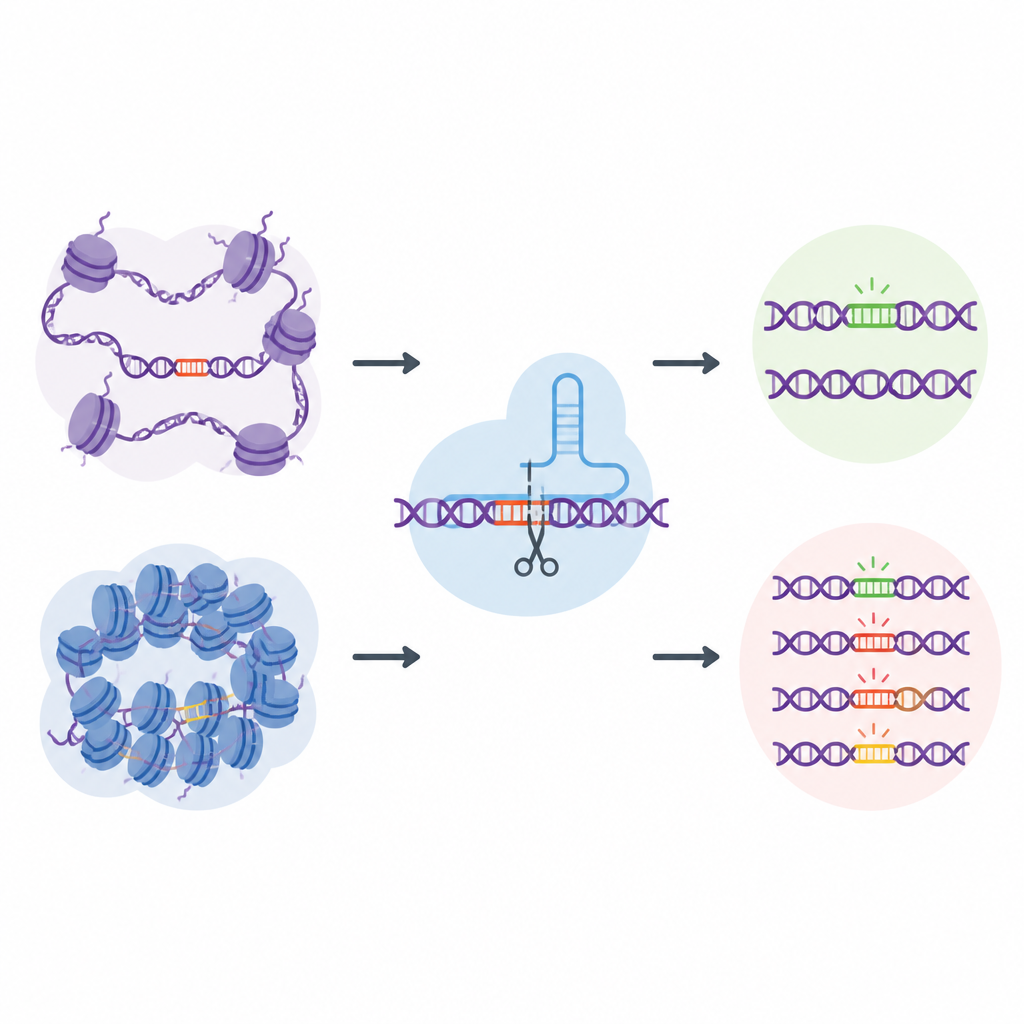
一种全基因组“天然”脱靶位点库
为了解决这一难题,研究者创建了EGOLD,全称为内源性全基因组脱靶库检测(Endogenous Genome-wide Off-target Library Detection)。他们没有构建人工DNA库,而是利用人类基因组中天然存在的重复或高度相似序列。研究者挑选出一些特殊的靶位点,其中单个CRISPR导向RNA与成千上万其他位置高度匹配,这些位置拥有相同的序列但位于非常不同的染色质环境中。通过编辑一个选定位点然后读取整个基因组,EGOLD可以比较这些长得很像的位点中哪些被编辑、哪些保持不变,同时它们的底层DNA字母保持一致。
开放的DNA更易受到误编辑
利用EGOLD,团队测试了17种基于CRISPR的编辑器,包括标准的切割DNA的Cas9蛋白和无需切割双链即可改变单个碱基的新型碱基编辑器。在超过两百万个检测到的脱靶事件中,清晰的模式显现:位于开放染色质的位点比相同序列但埋在封闭、致密区域的位点更容易被编辑。开放DNA的信号,例如对切割酶的可及性以及附近蛋白上的活性化学标记,与脱靶活性呈正相关。相反,与紧密包装或化学沉默的DNA相关的特征则倾向于对抗不良变更。
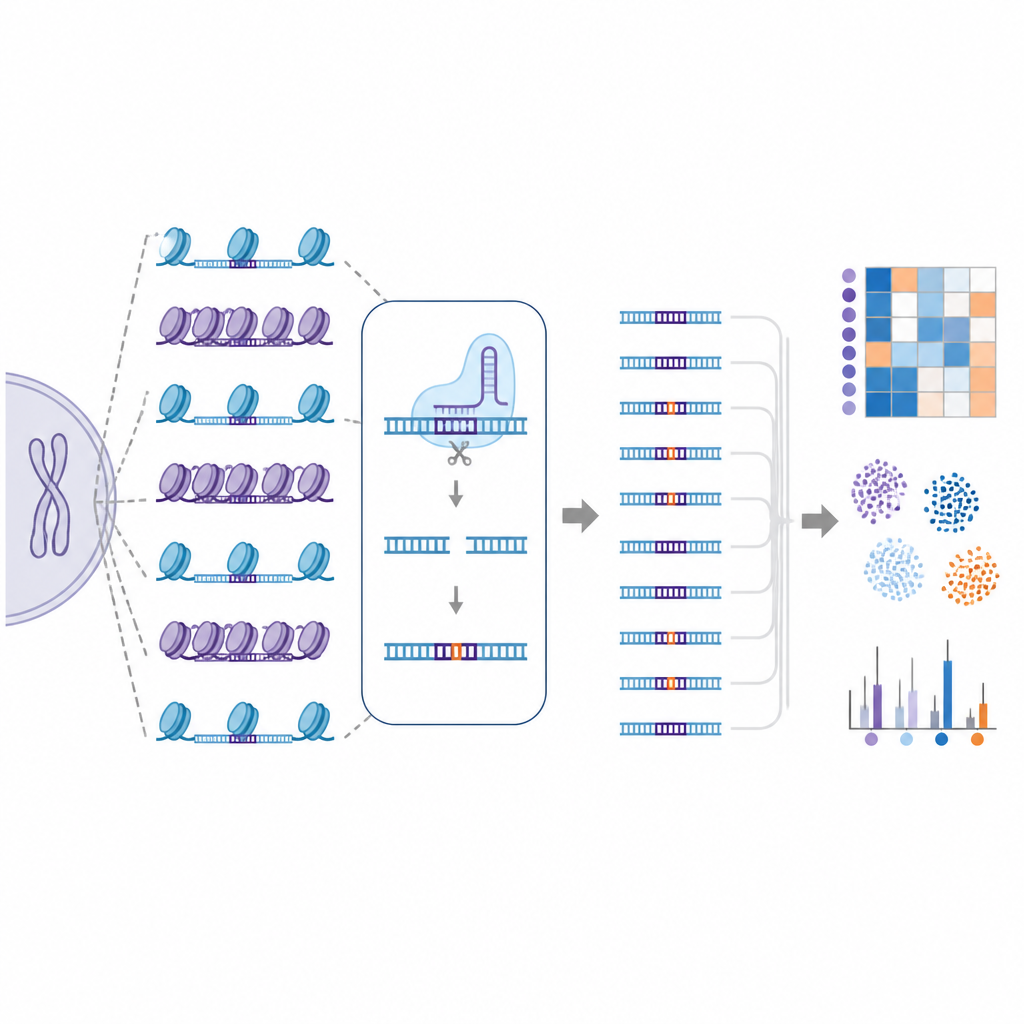
并非所有编辑器和细胞都表现相同
研究还比较了不同Cas9变体,这些变体经过工程改造以在识别上更为精确或更具灵活性。一个名为SuperFiCas9的变体在保持对其目标位点良好活性的同时产生相对较少的脱靶变化,尤其在作为碱基编辑器时表现突出。那些能容忍更多序列差异或识别规则更宽松的版本则显示出更高的脱靶率。即使使用相同的编辑器和导向RNA,不同的人类细胞类型也表现出不同的脱靶模式,突出显示了细胞特异性的染色质景观如何塑造编辑结果。
教计算机预测高风险位点
由于EGOLD生成了如此大规模且详细的脱靶地图,作者用这些数据训练了机器学习模型。这些计算模型输入每个潜在位点的序列信息和局部染色质特征,学会高精度地区分被编辑与未被编辑的位置。当将染色质信息加入基于序列的特征后,预测性能得到提升,强调了DNA包装不仅是一个次要细节,而是脱靶风险的关键组成部分。
对更安全基因编辑的意义
对关注基因治疗进展的人来说,这项工作表明CRISPR出错的位置不仅由DNA拼写决定,还受该DNA在细胞内如何折叠与标记的影响。EGOLD提供了一种在真实基因组中直接绘制这些风险的实用方法,并能构建将染色质环境纳入考虑的更智能预测工具。从长远看,这种方法可帮助研究者选择更安全的编辑策略、设计更优的导向序列并挑选更合适的编辑器版本,从而让改变生命的DNA修复伴随更少的非预期变更。
引用: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
关键词: CRISPR脱靶, 染色质环境, 碱基编辑, 基因组安全, 机器学习