Clear Sky Science · ar
فك شفرة دور سياق الكروماتين في الآثار الجانبية للتحرير الجيني بواسطة CRISPR باستخدام EGOLD
لماذا يمكن للتعديلات الصغيرة في الحمض النووي أن تُحدث آثارًا جانبية كبيرة
أثار تحرير الجينات باستخدام CRISPR آمالًا في علاج العديد من الأمراض الوراثية عن طريق تغيير الحمض النووي داخل خلايانا بدقة. لكن الأدوات نفسها التي قد تصلح جينًا معطوبًا قد تغيّر أيضًا أجزاء أخرى من الجينوم عن غير قصد، مكوِّنة تغييرات "خارج الهدف". تقدّم هذه الدراسة طريقة جديدة لرسم خرائط تلك التعديلات غير المقصودة مباشرة في خلايا بشرية وتكشف أن مدى إحكام تغليف الحمض النووي داخل الخلية يلعب دورًا رئيسيًا في الأماكن التي تحدث فيها التغييرات خارج الهدف.
النظر إلى ما وراء حروف الحمض النووي
تركّز معظم الجهود لفهم سلامة CRISPR على تسلسل الحمض النووي نفسه: أي سلاسل من A وC وG وT أكثر عرضة للقص أو التغيير. ومع ذلك، يكون الحمض النووي في الخلايا الحية ملفوفًا حول بروتينات ومطويًا في حالات أكثر انفتاحًا أو انغلاقًا، وهو منظر يُعرف بالكروماتين. المناطق المفتوحة أسهل لوصول الآلات الخلوية إليها، بينما تكون المناطق المغلقة أكثر حماية. اشتبه المؤلفون أن هذا التغليف المحلي للحمض النووي قد يوجّه بهدوء الأماكن التي ترتكب فيها أدوات CRISPR أخطاءها، لكن الاختبارات القائمة لم تلتقط مواقع جينومية حقيقية كافية لدراسة هذا التأثير بعمق.
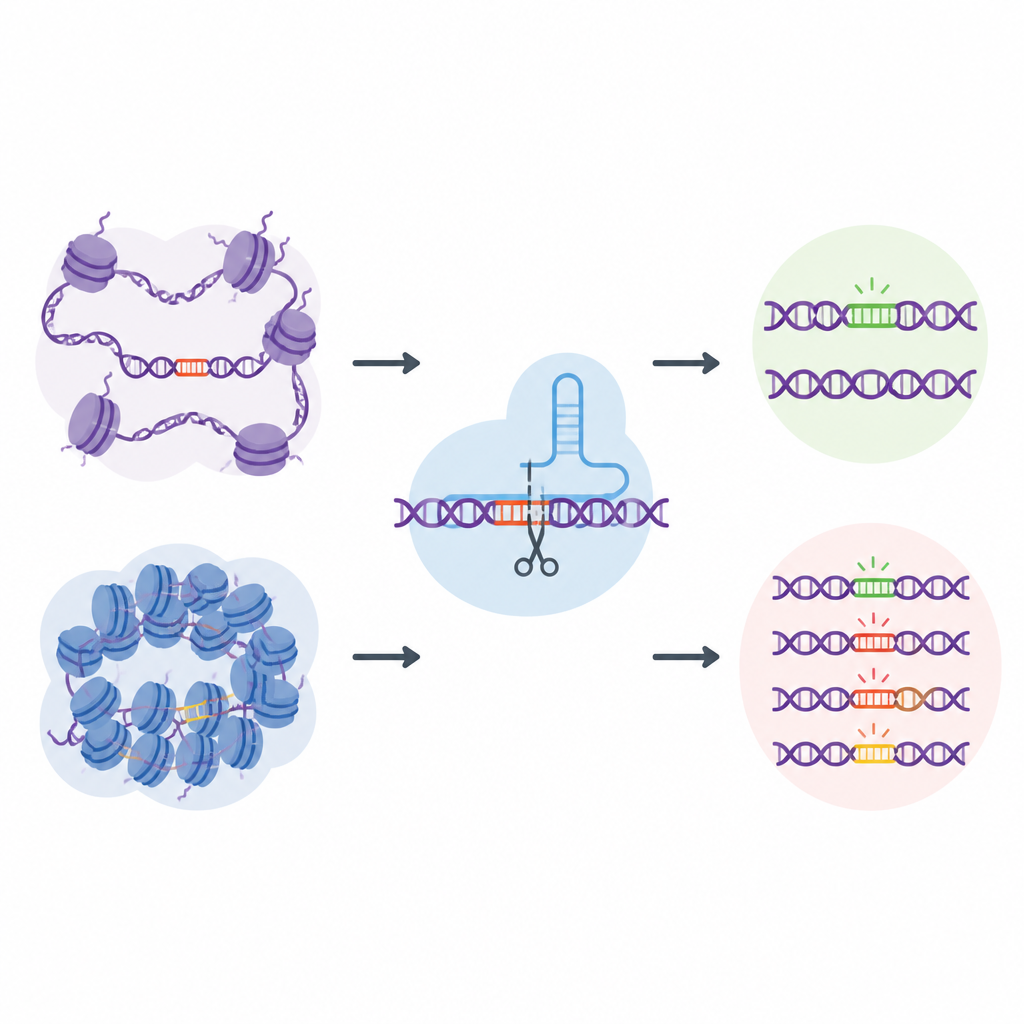
مكتبة طبيعية خارج الهدف شاملة للجينوم
لمعالجة هذا التحدي، أنشأ الباحثون EGOLD، وهو اختصار لـ Endogenous Genome-wide Off-target Library Detection. بدلاً من بناء مكتبات DNA اصطناعية، استغلّوا التسلسلات المتكررة أو المتشابهة جدًا المنتشرة بالفعل في الجينوم البشري. اختاروا مواقع مستهدفة خاصة حيث يتطابق مرشد CRISPR RNA واحد عن كثب مع آلاف المواقع الأخرى التي تشترك في نفس التسلسل لكنها تقع في بيئات كروماتين مختلفة للغاية. عن طريق تعديل موقع مختار واحد ثم قراءة الجينوم بأكمله، تُمكّن EGOLD من مقارنة أيٍّ من هذه المواقع المتشابهة عُدل وأيّها بقي غير مُعدَّل، بينما تبقى حروف الحمض النووي الأساسية متطابقة.
الحمض النووي المكشوف أكثر عرضة للتعديلات الطائشة
باستخدام EGOLD، اختبر الفريق 17 محررًا قائمًا على CRISPR، بما في ذلك بروتينات Cas9 القاطعة التقليدية والمحررات القاعدية الأحدث التي تغيّر حرفًا واحدًا دون قطع كلا شريطي الحمض النووي. عبر أكثر من مليوني حدث خارج هدف مُكتشف، ظهر نمط واضح: كانت المواقع الموجودة في كروماتين مفتوح أكثر عرضة للّمس من نفس التسلسل المدفون في مناطق مغلقة وكثيفة. كانت إشارات الحمض النووي المفتوح، مثل قابلية الوصول لإنزيمات القص والعلامات الكيميائية النشطة على البروتينات المجاورة، مرتبطة إيجابيًا بنشاط خارج الهدف. بالمقابل، كانت الميزات المرتبطة بالحمض النووي المكدّس بإحكام أو المُخمَّد كيميائيًا تميل إلى الحماية من التغييرات غير المرغوب فيها.
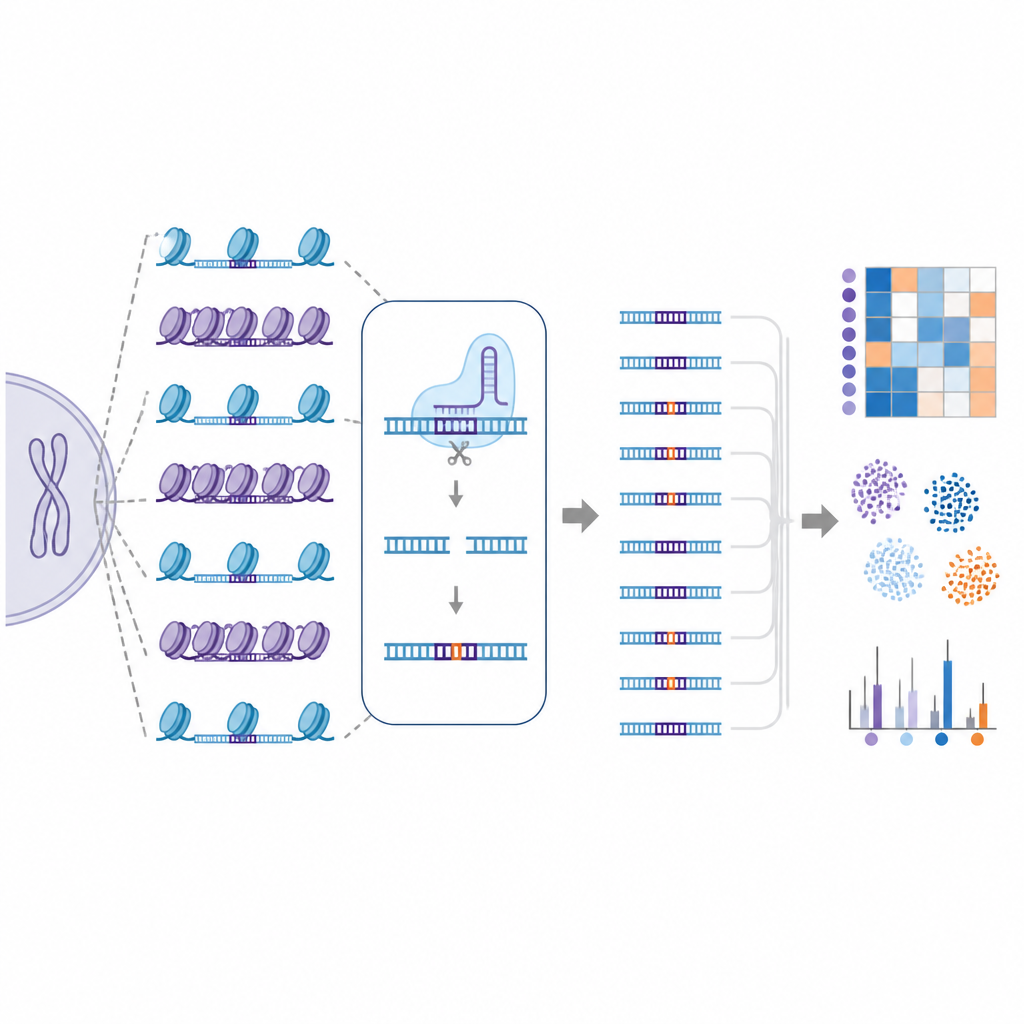
ليست كل المحررات أو الخلايا متشابهة
قارنَت الدراسة أيضًا بين متغيرات Cas9 المصممة إما لتكون أكثر دقة أو أكثر مرونة في ما تعترف به. برز متغير واحد اسمه SuperFiCas9 لاحتفاظه بنشاط جيد عند الهدف المقصود مع إنتاجه لعدد قليل نسبيًا من التغييرات خارج الهدف، لا سيما عند دمجه في محررات قاعدية. أبانت النسخ الأخرى التي تتحمّل اختلافات تسلسلية أكثر أو قواعد اعتراف أكثر تساهلًا معدلات خارج هدف أعلى بكثير. وحتى عند استخدام نفس المحرر ومرشد RNA، أظهرت أنواع خلايا بشرية مختلفة أنماطًا متباينة من الأحداث خارج الهدف، مما يبرز كيف أن مشاهد الكروماتين الخاصة بكل خلية تشكّل نتائج التحرير.
تعليم الحواسيب توقع المواقع عالية المخاطر
بما أن EGOLD تولّد خرائط خارج هدف كبيرة ومفصّلة، استخدم المؤلفون هذه البيانات لتدريب نماذج تعلم آلي. تمّ تزويد هذه النماذج الحاسوبية بمعلومات التسلسل وميزات الكروماتين المحلية لكل موقع محتمل، وتعلمت التمييز بدقّةٍ عالية بين المواقع المعدلة وغير المعدلة. عندما أضيفت معلومات الكروماتين إلى ميزات التسلسل، تحسّن أداء التنبؤ، ما يؤكد أن تغليف الحمض النووي ليس مجرد تفصيل ثانوي بل جزء أساسي من خطر حدوث تأثيرات خارج الهدف.
ماذا يعني هذا لتحرير جيني أكثر أمانًا
بالنسبة للمتابعين لتقدّم العلاج الجيني، تُظهر هذه الدراسة أن أماكن الخطأ في CRISPR تتشكّل ليس فقط بتهجئة الحمض النووي بل أيضًا بطريقة طيّ ووسم هذا الحمض داخل الخلايا. توفّر EGOLD وسيلة عملية لرسم هذه المخاطر مباشرة في جينومات حقيقية وبناء أدوات تنبؤ أذكى تأخذ سياق الكروماتين في الحسبان. على المدى الطويل، قد تساعد هذه المقاربة الباحثين على اختيار استراتيجيات تحرير أكثر أمانًا، وتصميم مرشدين أفضل، واختيار نسخ محرر أنسب بحيث تأتي الإصلاحات الجينية المغيِّرة للحياة مع عدد أقل من التغييرات غير المقصودة في أماكن أخرى.
الاستشهاد: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
الكلمات المفتاحية: تأثيرات خارج الهدف لـ CRISPR, سياق الكروماتين, التحرير القاعدي, سلامة الجينوم, تعلم الآلة