Clear Sky Science · it
Decodificare il ruolo del contesto cromatinico negli effetti off-target dell’editing CRISPR con EGOLD
Perché piccole modifiche al DNA possono avere grandi effetti collaterali
L’editing genetico con CRISPR ha acceso la speranza di curare molte malattie genetiche modificando con precisione il DNA all’interno delle nostre cellule. Ma gli stessi strumenti che possono correggere un gene difettoso possono anche alterare accidentalmente altre parti del genoma, creando cambiamenti “off-target”. Questo studio presenta un nuovo metodo per mappare quegli interventi non intenzionali direttamente in cellule umane e rivela che il grado di compattamento del DNA all’interno della cellula gioca un ruolo importante nel determinare dove si verificano gli off-target.
Oltre le lettere del DNA
La maggior parte degli sforzi per comprendere la sicurezza di CRISPR si concentra sulla sequenza del DNA: quali stringhe di A, C, G e T sono più propense a essere tagliate o modificate. Tuttavia, nel contesto cellulare il DNA è avvolto attorno a proteine e ripiegato in stati più aperti o più chiusi, un paesaggio noto come cromatina. Le regioni aperte sono più facilmente raggiungibili dalle macchine cellulari, mentre le regioni chiuse sono più protette. Gli autori sospettavano che questo confezionamento locale del DNA potesse indirizzare silenziosamente dove gli strumenti CRISPR commettono errori, ma i test esistenti non catturavano un numero sufficiente di siti genomici reali per studiare questo effetto in profondità.
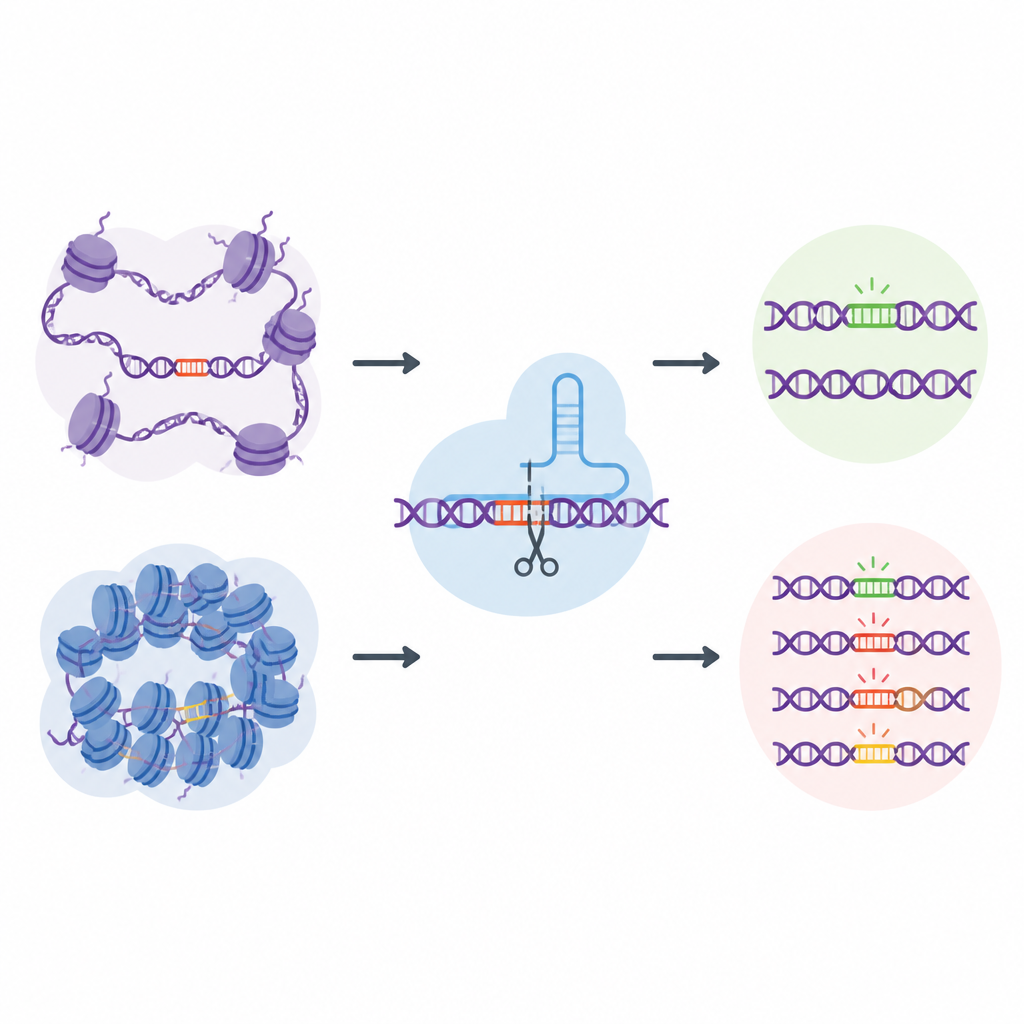
Una libreria off-target “naturale” su scala genomica
Per affrontare questa sfida, i ricercatori hanno creato EGOLD, acronimo di Endogenous Genome-wide Off-target Library Detection. Invece di costruire librerie di DNA artificiali, hanno sfruttato sequenze ripetute o molto simili già disseminate nel genoma umano. Hanno selezionato siti bersaglio particolari in cui una singola guida CRISPR corrisponde strettamente a migliaia di altre posizioni che condividono la stessa sequenza ma si trovano in ambienti cromatinici molto diversi. Modificando un sito scelto e poi sequenziando l’intero genoma, EGOLD può confrontare quali di questi molti siti simili vengono modificati e quali restano intatti, pur avendo lettere di DNA sottostanti identiche.
Il DNA aperto è più vulnerabile alle modifiche accidentali
Con EGOLD, il team ha testato 17 editor basati su CRISPR, inclusi i classici enzimi Cas9 che tagliano il DNA e i più recenti editor di basi che cambiano singole lettere senza rompere entrambi i filamenti. Su oltre due milioni di eventi off-target rilevati è emerso un quadro chiaro: i siti in cromatina aperta erano molto più propensi a essere modificati rispetto alla stessa sequenza se sepolta in regioni chiuse e compatte. Segnali di DNA aperto, come l’accessibilità agli enzimi di taglio e marchi chimici attivi sulle proteine vicine, si associavano positivamente all’attività off-target. Al contrario, caratteristiche legate a DNA fortemente impaccato o chimicamente silenziato tendevano a proteggere contro cambiamenti indesiderati.
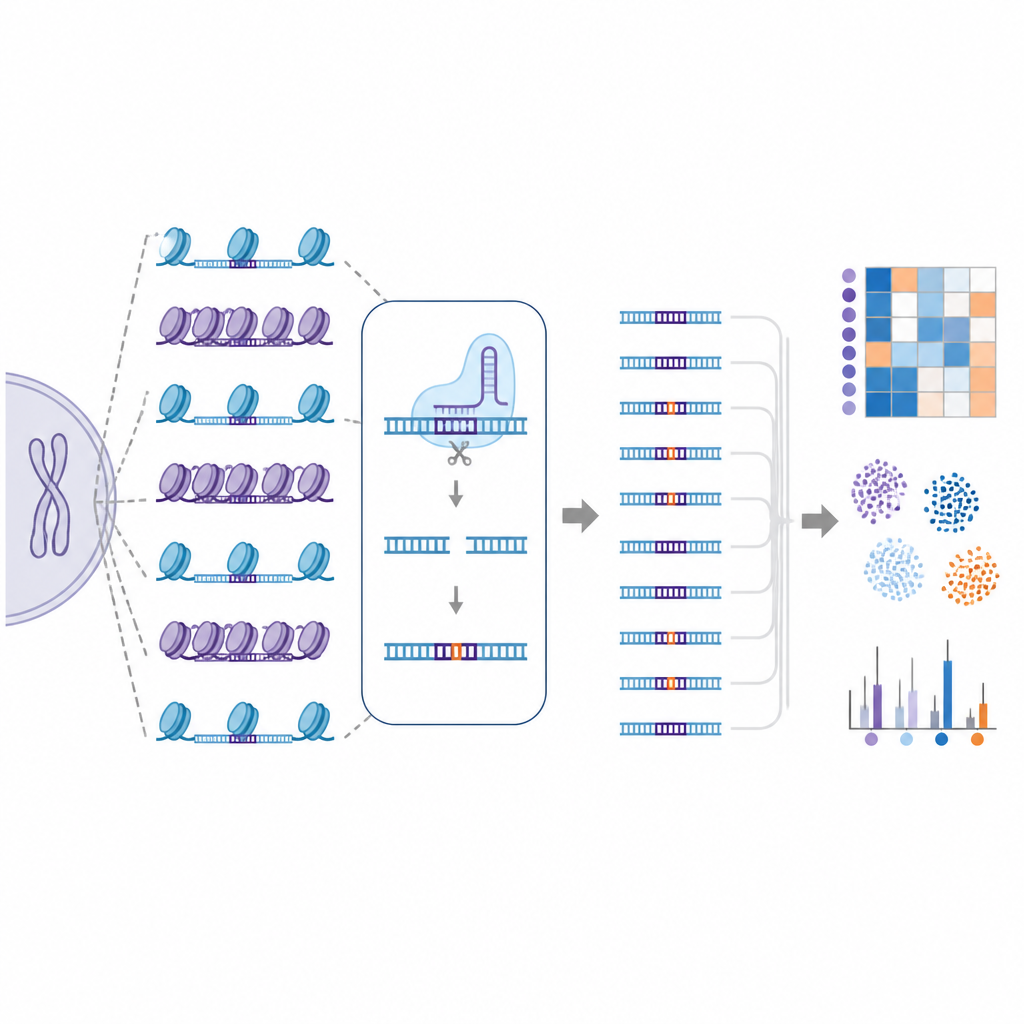
Non tutti gli editor e le cellule si comportano allo stesso modo
Lo studio ha anche confrontato varianti di Cas9 ingegnerizzate per essere più accurate o più permissive nel riconoscere sequenze. Una variante chiamata SuperFiCas9 si è distinta per mantenere una buona attività sul bersaglio previsto producendo relativamente pochi off-target, soprattutto quando integrata in editor di basi. Altre versioni in grado di tollerare più differenze di sequenza o regole di riconoscimento più rilassate mostravano tassi di off-target molto più alti. Anche usando lo stesso editor e la stessa guida, diversi tipi di cellule umane hanno mostrato pattern off-target differenti, sottolineando come i paesaggi cromatinici specifici delle cellule influenzino gli esiti dell’editing.
Addestrare i computer a prevedere i siti a rischio
Poiché EGOLD produce mappe off-target così ampie e dettagliate, gli autori hanno usato questi dati per addestrare modelli di machine learning. Questi modelli informatici hanno ricevuto sia informazioni di sequenza sia caratteristiche cromatiniche locali per ciascun sito potenziale e hanno imparato a distinguere le posizioni modificate da quelle non modificate con altissima accuratezza. Quando alle caratteristiche basate sulla sequenza è stata aggiunta l’informazione sulla cromatina, le prestazioni predittive sono migliorate, evidenziando che il confezionamento del DNA non è un dettaglio marginale ma una componente chiave del rischio off-target.
Cosa significa per un editing genetico più sicuro
Per chi segue i progressi della terapia genica, questo lavoro mostra che dove CRISPR fallisce è determinato non solo dall’ortografia del DNA ma anche da come quel DNA è ripiegato e marcato all’interno delle cellule. EGOLD fornisce un modo pratico per mappare direttamente questi rischi nei genomi reali e per costruire strumenti predittivi più intelligenti che tengano conto del contesto cromatinico. Nel lungo periodo, questo approccio potrebbe aiutare i ricercatori a scegliere strategie di editing più sicure, progettare guide migliori e selezionare versioni di editor più adatte, in modo che correzioni del DNA che cambiano la vita comportino meno modifiche indesiderate altrove.
Citazione: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
Parole chiave: Off-target CRISPR, contesto cromatinico, editing di basi, sicurezza del genoma, apprendimento automatico