Clear Sky Science · pl
Odkodowanie roli kontekstu chromatyny w efektach pozabrefowych edycji genów CRISPR za pomocą EGOLD
Dlaczego drobne zmiany w DNA mogą mieć poważne skutki uboczne
Edycja genów za pomocą CRISPR wzbudziła nadzieje na wyleczenie wielu chorób genetycznych dzięki precyzyjnej zmianie DNA w naszych komórkach. Jednak te same narzędzia, które potrafią naprawić wadliwy gen, mogą też przypadkowo modyfikować inne fragmenty genomu, tworząc tzw. zmiany pozabrefowe. W badaniu tym przedstawiono nową metodę mapowania takich niezamierzonych edycji bezpośrednio w komórkach ludzkich i ujawniono, że stopień upakowania DNA w komórce odgrywa istotną rolę w określaniu miejsc, gdzie pojawiają się te niepożądane zmiany.
Patrząc poza litery DNA
Większość prób zrozumienia bezpieczeństwa CRISPR koncentruje się na samej sekwencji DNA: które sekwencje A, C, G i T są najbardziej podatne na przecięcie lub zmianę. Tymczasem DNA w żywych komórkach owinięte jest wokół białek i złożone w stany bardziej otwarte lub zamknięte — krajobraz zwany chromatyną. Regiony otwarte są łatwiej dostępne dla maszynerii komórkowej, podczas gdy regiony zamknięte są bardziej osłonięte. Autorzy przypuszczali, że lokalne pakowanie DNA może dyskretnie kierować miejscami, gdzie narzędzia CRISPR popełniają błędy, lecz istniejące testy nie obejmowały wystarczająco wielu rzeczywistych miejsc genomowych, by dokładnie zbadać ten efekt.
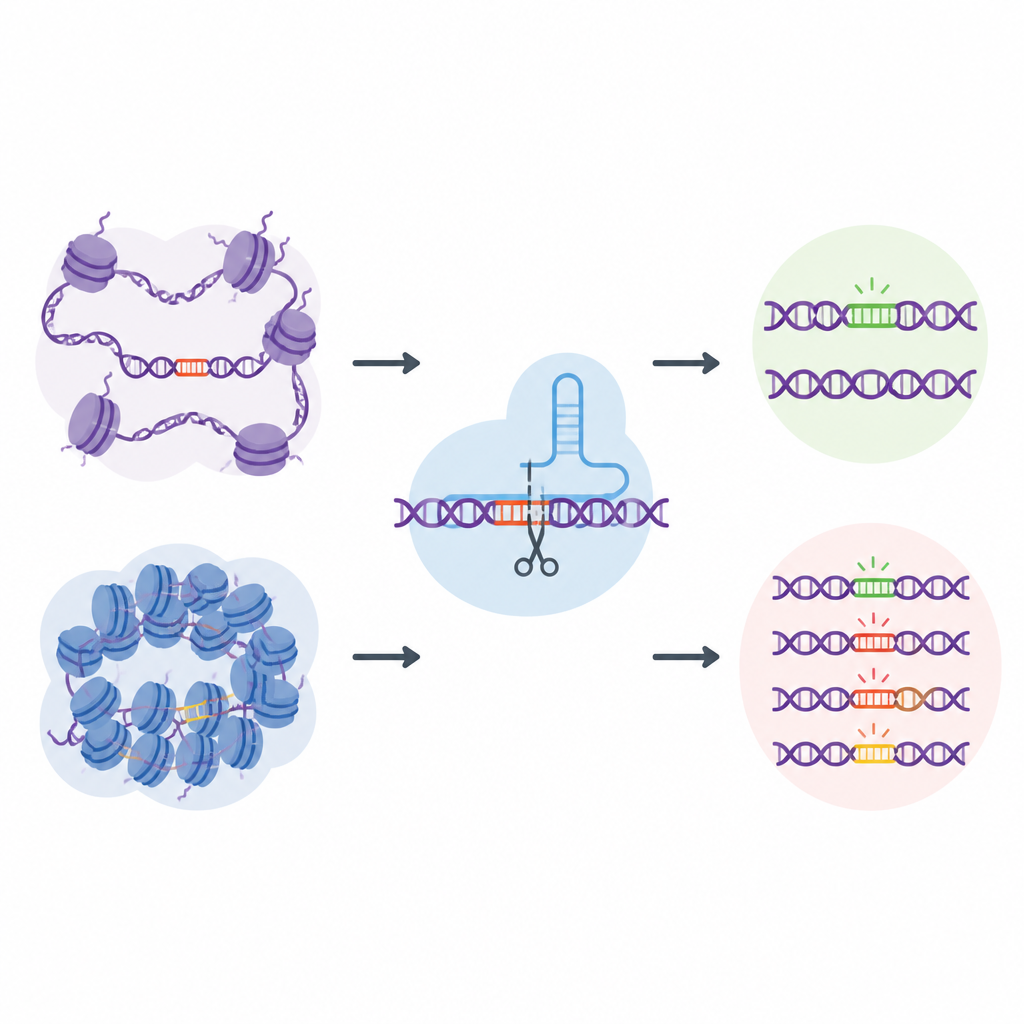
Genomowa „naturalna” biblioteka miejsc pozacelowych
Aby sprostać temu wyzwaniu, badacze stworzyli EGOLD, czyli Endogenous Genome-wide Off-target Library Detection. Zamiast budować sztuczne biblioteki DNA, skorzystali z powtarzających się lub bardzo podobnych sekwencji już rozrzuconych po całym ludzkim genomie. Wybrali specjalne cele, gdzie pojedynczy przewodnik RNA CRISPR bardzo dobrze pasuje do tysięcy innych lokalizacji, które mają tę samą sekwencję, ale znajdują się w różnych środowiskach chromatynowych. Poprzez edycję jednego wybranego miejsca i późniejsze odczytanie całego genomu, EGOLD może porównać, które z tych wielu podobnych miejsc zostały zedytowane, a które pozostały nietknięte, przy niezmiennej sekwencji liter DNA.
Otwarte DNA jest bardziej podatne na przypadkowe edycje
Stosując EGOLD, zespół przetestował 17 edytorów opartych na CRISPR, w tym standardowe białka Cas9 przecinające DNA oraz nowsze edytory zasad, które zmieniają pojedyncze litery bez przecinania obu nici DNA. W ponad dwóch milionach wykrytych zdarzeń pozacelowych wyłonił się wyraźny wzorzec: miejsca w otwartej chromatynie były znacznie bardziej narażone na edycję niż ta sama sekwencja ukryta w zamkniętych, skompaktowanych regionach. Sygnaly otwartego DNA, takie jak dostępność dla enzymów tnących DNA oraz aktywne chemiczne modyfikacje pobliskich białek, korelowały dodatnio z aktywnością pozacelową. Natomiast cechy związane z ciasno upakowanym lub chemicznie wyciszonym DNA zwykle chroniły przed niepożądanymi zmianami.
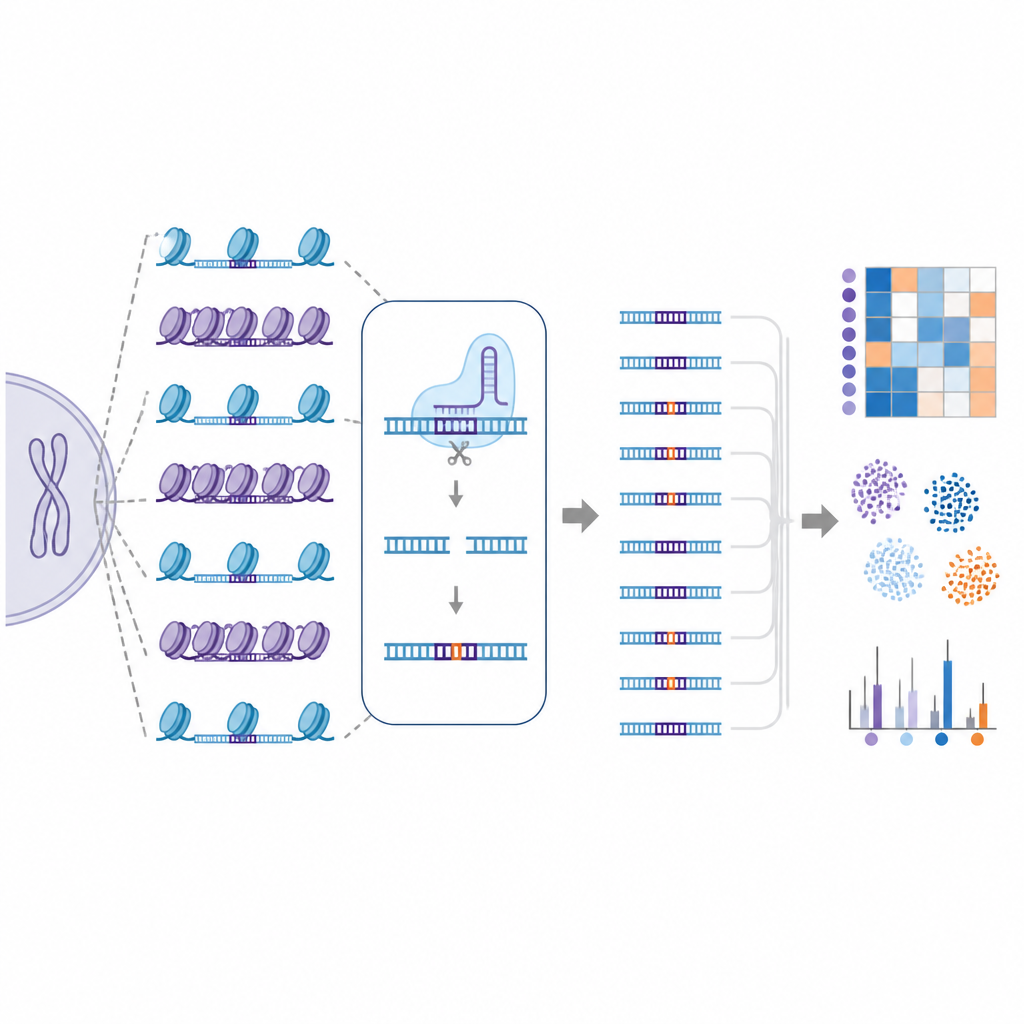
Nie wszystkie edytory i typy komórek zachowują się jednakowo
Badanie porównało również różne warianty Cas9 zaprojektowane tak, aby były albo bardziej precyzyjne, albo bardziej elastyczne w rozpoznawaniu sekwencji. Jeden wariant nazwany SuperFiCas9 wyróżniał się utrzymywaniem dobrej aktywności na zamierzonym celu przy stosunkowo niewielkiej liczbie zmian pozacelowych, zwłaszcza gdy zastosowano go w edytorach zasad. Inne wersje, które tolerowały większe różnice w sekwencji lub miały luźniejsze zasady rozpoznawania, wykazywały znacznie wyższe wskaźniki pozacelowe. Nawet przy użyciu tego samego edytora i przewodnika RNA różne typy ludzkich komórek pokazywały odmienne wzorce pozacelowe, podkreślając, jak komórkowo-specyficzne krajobrazy chromatyny kształtują wyniki edycji.
Nauczanie komputerów przewidywania ryzykownych miejsc
Ponieważ EGOLD generuje tak duże, szczegółowe mapy pozacelowe, autorzy wykorzystali te dane do trenowania modeli uczenia maszynowego. Modele te otrzymywały zarówno informacje o sekwencji, jak i lokalne cechy chromatyny dla każdego potencjalnego miejsca i nauczyły się rozróżniać zedytowane od niezedytowanych lokalizacji z bardzo wysoką dokładnością. Gdy do cech opartych na sekwencji dodano informacje o chromatynie, skuteczność predykcji wzrosła, co podkreśla, że pakowanie DNA nie jest jedynie bocznym szczegółem, lecz kluczowym elementem ryzyka pozacelowego.
Co to znaczy dla bezpieczniejszej edycji genów
Dla osób śledzących postęp terapii genowych, praca ta pokazuje, że miejsca, w których CRISPR się myli, są kształtowane nie tylko przez zapis DNA, ale także przez to, jak DNA jest złożone i oznaczone w komórkach. EGOLD dostarcza praktycznego sposobu na bezpośrednie mapowanie tych ryzyk w rzeczywistych genomach oraz na budowanie lepszych narzędzi predykcyjnych uwzględniających kontekst chromatyny. W dłuższej perspektywie podejście to może pomóc badaczom wybierać bezpieczniejsze strategie edycji, projektować lepsze przewodniki i dobierać bardziej odpowiednie warianty edytorów, tak by znaczące naprawy DNA wiązały się z mniejszą liczbą niezamierzonych zmian w innych miejscach.
Cytowanie: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
Słowa kluczowe: pozacele CRISPR, kontekst chromatyny, edycja zasad, bezpieczeństwo genomu, uczenie maszynowe