Clear Sky Science · de
Entschlüsselung der Rolle des Chromatin-Kontexts bei Off-Target-Effekten der CRISPR-Geneditierung mit EGOLD
Warum winzige DNA-Änderungen große Nebenwirkungen haben können
Die CRISPR-Geneditierung weckt Hoffnungen, viele genetische Erkrankungen zu heilen, indem sie DNA in unseren Zellen präzise verändert. Dieselben Werkzeuge, die ein fehlerhaftes Gen reparieren können, können jedoch auch versehentlich andere Stellen im Genom verändern und so "Off-Target"-Veränderungen erzeugen. Diese Studie stellt eine neue Methode vor, um solche unbeabsichtigten Edits direkt in menschlichen Zellen zu kartieren, und zeigt, dass die Dichte, mit der DNA innerhalb der Zelle verpackt ist, eine wichtige Rolle dabei spielt, wo Off-Target-Veränderungen auftreten.
Über die DNA-Buchstaben hinausblicken
Die meisten Bemühungen, CRISPR-Sicherheit zu verstehen, konzentrieren sich auf die DNA-Sequenz selbst: Welche Abfolgen von A, C, G und T werden am ehesten geschnitten oder verändert? In lebenden Zellen ist die DNA jedoch um Proteine gewickelt und zu offeneren oder geschlosseneren Zuständen gefaltet — eine Landschaft, die als Chromatin bekannt ist. Offene Regionen sind leichter für zelluläre Maschinen zugänglich, während geschlossene Regionen stärker abgeschirmt sind. Die Autorinnen und Autoren vermuteten, dass diese lokale DNA-Verpackung stillschweigend steuern könnte, wo CRISPR-Werkzeuge Fehler machen. Bestehende Tests erfassten jedoch nicht genügend echte genomische Stellen, um diesen Effekt gründlich zu untersuchen.
Eine genomweite „natürliche“ Off-Target-Bibliothek
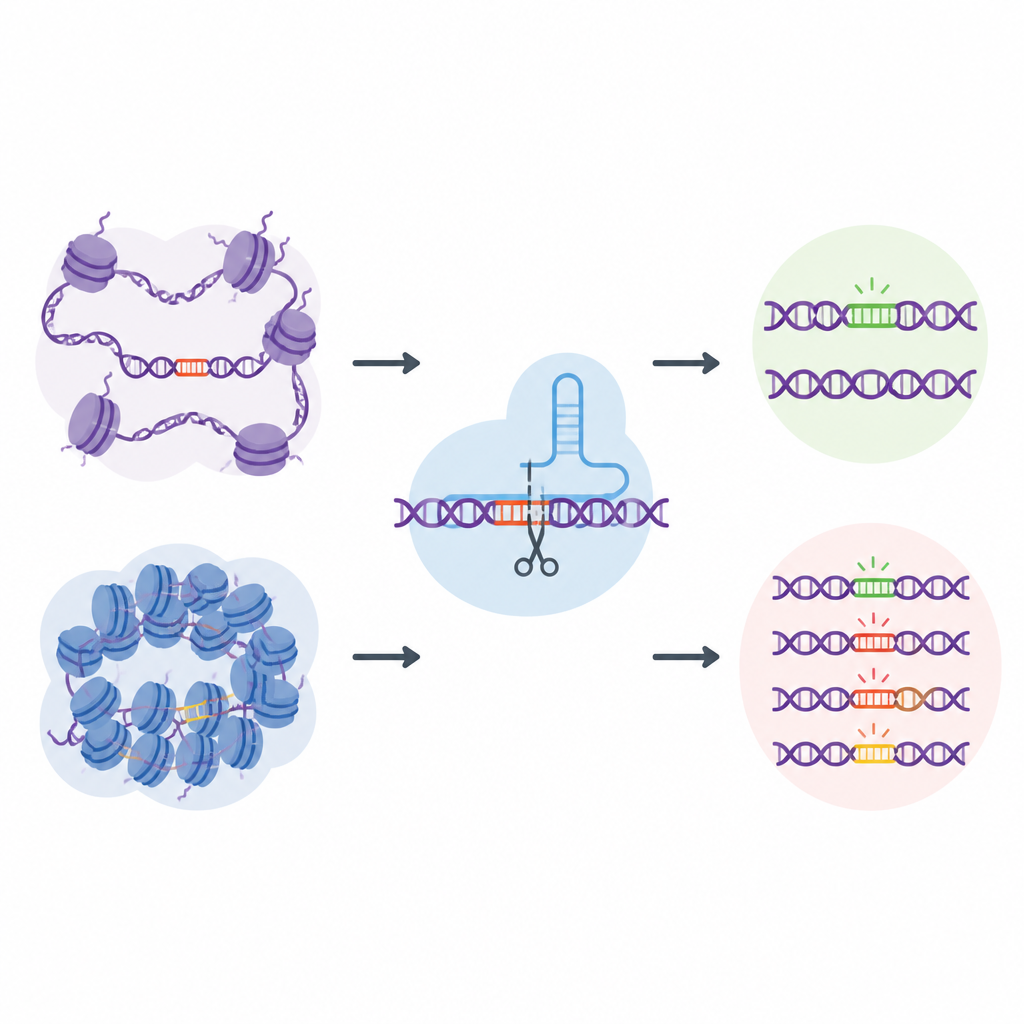
Um diese Herausforderung anzugehen, entwickelten die Forschenden EGOLD, kurz für Endogenous Genome-wide Off-target Library Detection. Statt künstliche DNA-Bibliotheken zu bauen, nutzten sie wiederkehrende oder sehr ähnliche Sequenzen, die bereits im menschlichen Genom verteilt sind. Sie wählten spezielle Zielstellen aus, an denen eine einzelne CRISPR-Guide-RNA tausendfach ähnlich passende Orte findet, die dieselbe Sequenz teilen, aber in sehr unterschiedlichen Chromatin-Umgebungen liegen. Indem sie eine gewählte Stelle editieren und dann das gesamte Genom auslesen, kann EGOLD vergleichen, welche dieser vielen ähnlichen Stellen verändert und welche unberührt bleiben — wobei die zugrunde liegenden DNA-Buchstaben identisch bleiben.
Offene DNA ist anfälliger für versehentliche Edits
Mit EGOLD testete das Team 17 CRISPR-basierte Editoren, darunter klassische Cas9-Proteine, die DNA schneiden, sowie neuere Baseneditoren, die einzelne Buchstaben ändern, ohne beide DNA-Stränge zu schneiden. Über mehr als zwei Millionen detektierte Off-Target-Ereignisse zeigte sich ein klares Muster: Stellen in offenem Chromatin wurden viel häufiger editiert als dieselbe Sequenz, die in geschlossenen, kompakteren Regionen eingebettet war. Kennzeichen offener DNA, wie Zugänglichkeit für schneidende Enzyme und aktive chemische Markierungen an benachbarten Proteinen, korrelierten positiv mit Off-Target-Aktivität. Dagegen schützten Merkmale, die mit dicht gepackter oder chemisch stillgelegter DNA verbunden sind, tendenziell vor unerwünschten Veränderungen.
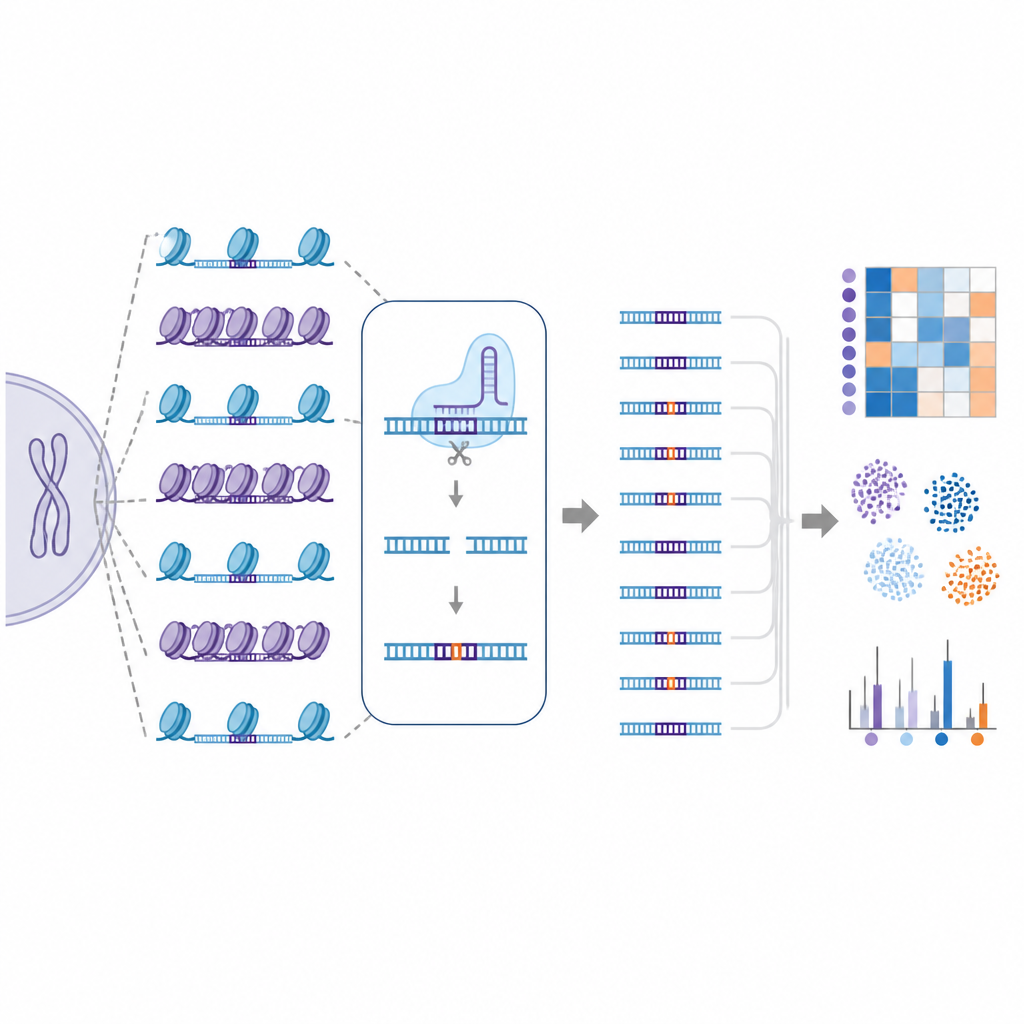
Nicht alle Editoren und Zelltypen verhalten sich gleich
Die Studie verglich außerdem verschiedene Cas9-Varianten, die entweder auf Genauigkeit getrimmt oder in ihrer Erkennungsflexibilität verändert wurden. Eine Variante namens SuperFiCas9 fiel dadurch auf, dass sie gute Aktivität am beabsichtigten Ziel beibehielt, aber vergleichsweise wenige Off-Target-Veränderungen verursachte — besonders, wenn sie in Baseneditoren eingebaut war. Andere Versionen, die mehr Sequenzabweichungen tolerierten oder lockerere Erkennungsregeln hatten, zeigten deutlich höhere Off-Target-Raten. Selbst bei demselben Editor und derselben Guide-RNA zeigten verschiedene menschliche Zelltypen unterschiedliche Off-Target-Muster, was unterstreicht, wie zelltypspezifische Chromatin-Landschaften Editierergebnisse prägen.
Computern beibringen, riskante Stellen vorherzusagen
Weil EGOLD so große, detaillierte Off-Target-Karten erzeugt, nutzten die Autorinnen und Autoren diese Daten, um maschinelle Lernmodelle zu trainieren. Diese Modelle wurden sowohl mit Sequenzinformationen als auch mit lokalen Chromatin-Merkmalen für jede potenzielle Stelle gefüttert und lernten, editierte von uneditierten Positionen mit sehr hoher Genauigkeit zu unterscheiden. Sobald Chromatin-Informationen zu sequenzbasierten Merkmalen hinzugefügt wurden, verbesserte sich die Vorhersageleistung — ein Hinweis darauf, dass DNA-Verpackung nicht nur ein Randdetail ist, sondern ein zentraler Faktor des Off-Target-Risikos.
Was das für sicherere Geneditierung bedeutet
Für alle, die die Entwicklung der Gentherapie verfolgen, zeigt diese Arbeit, dass die Orte, an denen CRISPR Fehler macht, nicht nur durch die DNA-Schreibweise bestimmt werden, sondern auch durch die Art und Weise, wie diese DNA in Zellen gefaltet und markiert ist. EGOLD liefert eine praktikable Methode, diese Risiken direkt in echten Genomen zu erfassen und bessere Vorhersagemodelle zu entwickeln, die den Chromatin-Kontext berücksichtigen. Langfristig könnte dieser Ansatz Forschenden helfen, sicherere Editierstrategien zu wählen, bessere Guides zu entwerfen und geeignetere Editor-Versionen auszuwählen, sodass lebensverändernde DNA-Korrekturen mit weniger unbeabsichtigten Veränderungen an anderen Stellen einhergehen.
Zitation: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
Schlüsselwörter: CRISPR Off-Targets, Chromatin-Kontext, Baseneditierung, Genomsicherheit, Maschinelles Lernen