Clear Sky Science · fr
Décoder le rôle du contexte chromatinien dans les effets hors cible de l'édition génique CRISPR avec EGOLD
Pourquoi de minuscules retouches d'ADN peuvent avoir de gros effets secondaires
L'édition génique par CRISPR a suscité l'espoir de guérir de nombreuses maladies génétiques en modifiant précisément l'ADN à l'intérieur de nos cellules. Mais les mêmes outils qui peuvent réparer un gène défaillant peuvent aussi modifier accidentellement d'autres parties du génome, créant des altérations « hors cible ». Cette étude présente une nouvelle méthode pour cartographier ces éditions non désirées directement dans des cellules humaines et révèle que la manière dont l'ADN est compacté dans la cellule joue un rôle majeur dans l'endroit où surviennent ces modifications hors cible.
Regarder au-delà des lettres de l'ADN
La plupart des efforts pour comprendre la sécurité de CRISPR se concentrent sur la séquence d'ADN elle-même : quelles suites de A, C, G et T sont les plus susceptibles d'être coupées ou modifiées. Pourtant, l'ADN dans les cellules vivantes est enroulé autour de protéines et replié en états plus ouverts ou plus fermés, un paysage appelé chromatine. Les régions ouvertes sont plus accessibles aux machineries cellulaires, tandis que les régions fermées sont davantage protégées. Les auteurs ont supposé que cet emballage local de l'ADN pouvait discrètement guider les erreurs des outils CRISPR, mais les tests existants ne capturent pas assez de sites génomiques réels pour étudier cet effet en profondeur.
Une bibliothèque « naturelle » hors cible à l'échelle du génome
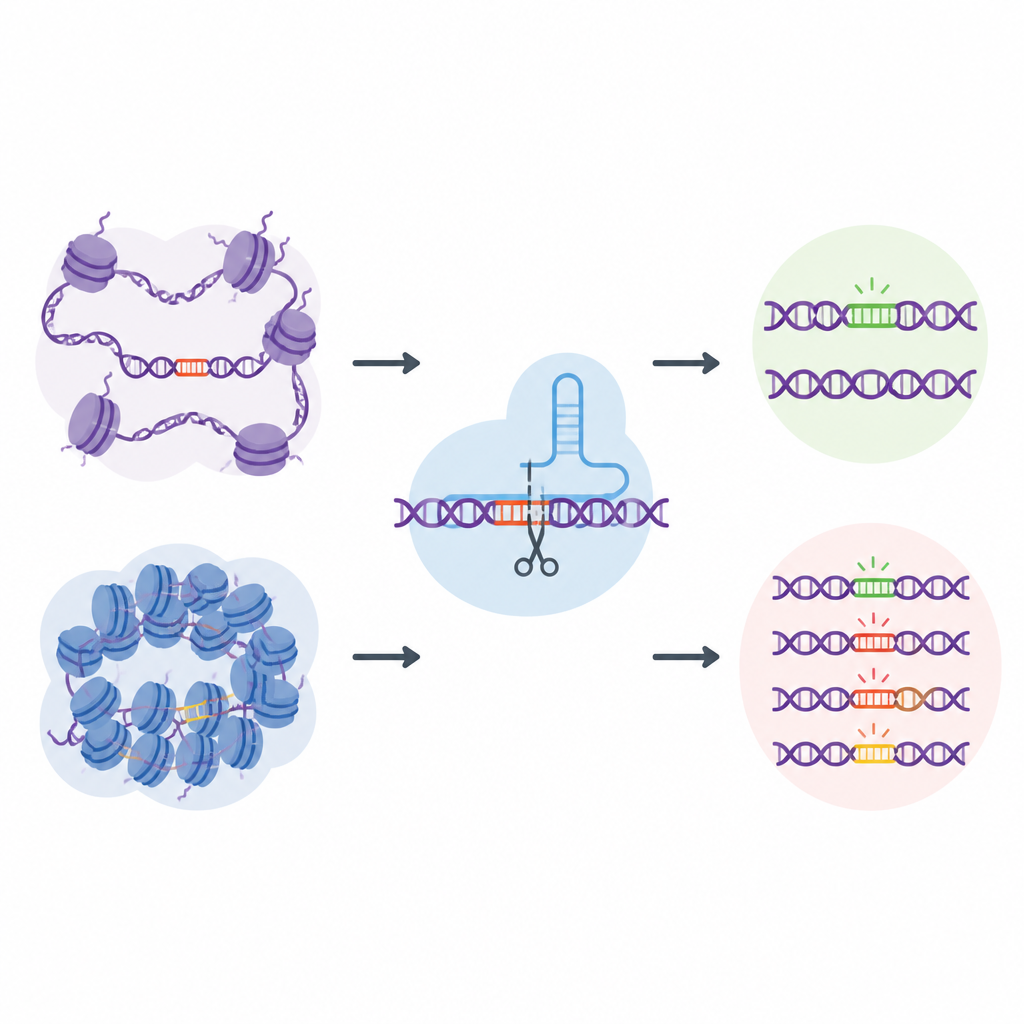
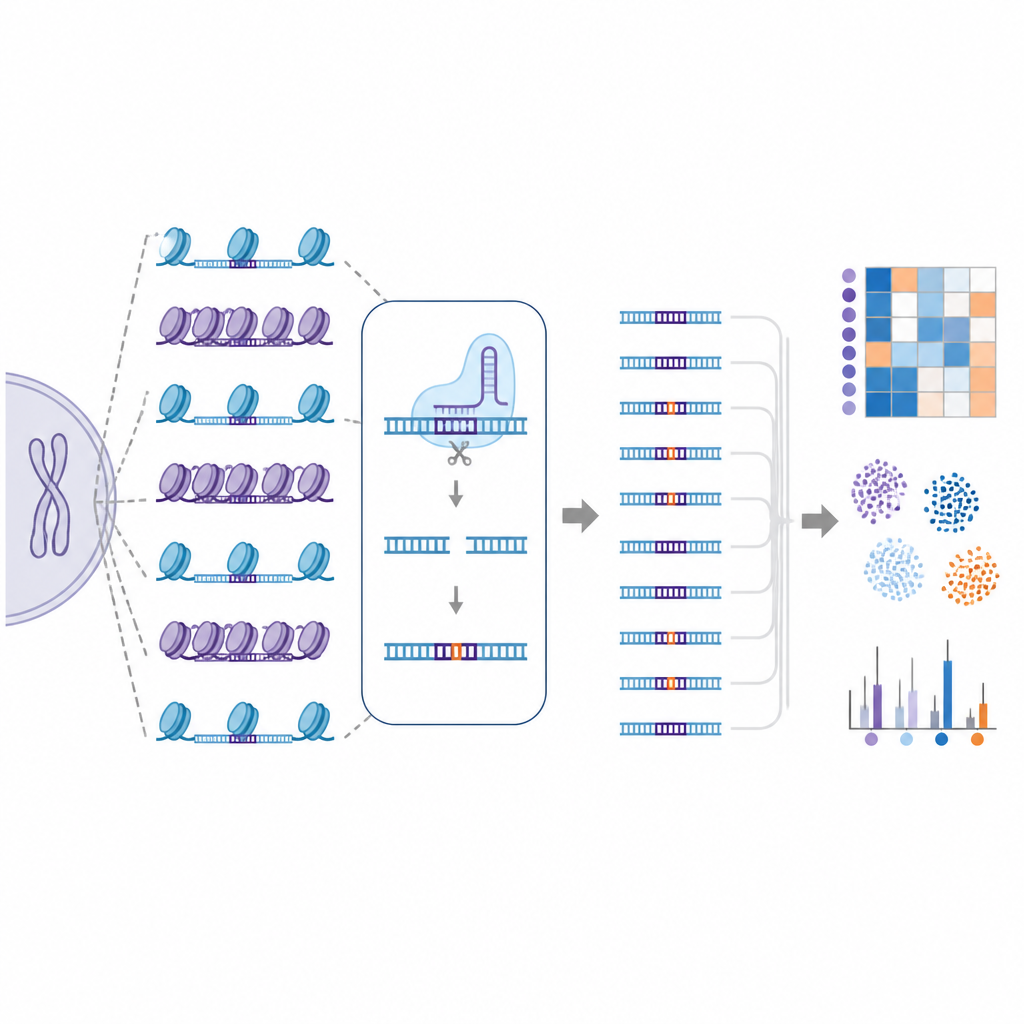
Pour relever ce défi, les chercheurs ont créé EGOLD, abréviation de Endogenous Genome-wide Off-target Library Detection. Plutôt que de construire des bibliothèques d'ADN artificielles, ils ont tiré parti de séquences répétées ou très similaires déjà disséminées dans le génome humain. Ils ont choisi des sites cibles spéciaux où un ARN guide CRISPR correspond de près à des milliers d'autres emplacements qui partagent la même séquence mais se trouvent dans des environnements chromatiniens très différents. En éditant un site choisi puis en lisant l'ensemble du génome, EGOLD peut comparer lesquels de ces nombreux sites semblables sont modifiés et lesquels restent intacts, tout en conservant des lettres d'ADN identiques.
L'ADN ouvert est plus vulnérable aux modifications errantes
Avec EGOLD, l'équipe a testé 17 éditeurs basés sur CRISPR, y compris les protéines Cas9 classiques qui coupent l'ADN et de nouveaux éditeurs de bases qui modifient une seule lettre sans couper les deux brins. Sur plus de deux millions d'événements hors cible détectés, un schéma clair est apparu : les sites en chromatine ouverte étaient beaucoup plus susceptibles d'être édités que la même séquence enfouie dans des régions fermées et compactes. Les signaux d'ADN ouvert, comme l'accessibilité aux enzymes de coupure et les marques chimiques actives sur les protéines voisines, étaient positivement liés à l'activité hors cible. En revanche, les caractéristiques associées à un ADN fortement compacté ou chimiquement silencieux avaient tendance à protéger contre les modifications indésirables.
Tous les éditeurs et toutes les cellules ne se comportent pas de la même façon
L'étude a également comparé différents variants de Cas9 conçus pour être soit plus précis soit plus flexibles dans leur reconnaissance. Un variant appelé SuperFiCas9 s'est distingué en conservant une bonne activité sur sa cible prévue tout en produisant relativement peu de changements hors cible, surtout lorsqu'il était intégré dans des éditeurs de bases. D'autres versions capables de tolérer davantage de différences de séquence ou des règles de reconnaissance plus lâches présentaient des taux hors cible bien plus élevés. Même lorsque le même éditeur et le même ARN guide étaient utilisés, différents types cellulaires humains montraient des profils hors cible différents, soulignant comment les paysages chromatiniens propres à chaque cellule influencent les résultats d'édition.
Apprendre aux ordinateurs à prédire les sites à risque
Parce qu'EGOLD génère des cartes hors cible aussi larges et détaillées, les auteurs ont utilisé ces données pour entraîner des modèles d'apprentissage automatique. Ces modèles informatiques ont reçu à la fois des informations de séquence et des caractéristiques chromatiniques locales pour chaque site potentiel et ont appris à distinguer les emplacements édités des non édités avec une très grande précision. Lorsque l'information sur la chromatine était ajoutée aux caractéristiques basées sur la séquence, les performances de prédiction s'amélioraient, soulignant que l'emballage de l'ADN n'est pas un détail accessoire mais une composante clé du risque hors cible.
Ce que cela signifie pour une édition génique plus sûre
Pour ceux qui suivent les progrès de la thérapie génique, ce travail montre que les erreurs de CRISPR sont déterminées non seulement par l'orthographe de l'ADN mais aussi par la façon dont cet ADN est replié et marqué à l'intérieur des cellules. EGOLD offre un moyen pratique de cartographier ces risques directement dans des génomes réels et de construire des outils de prédiction plus intelligents qui tiennent compte du contexte chromatinien. À long terme, cette approche pourrait aider les chercheurs à choisir des stratégies d'édition plus sûres, concevoir de meilleurs guides et sélectionner des versions d'éditeurs plus appropriées afin que des corrections d'ADN potentiellement salvatrices s'accompagnent de moins de modifications non désirées ailleurs.
Citation: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
Mots-clés: effets hors cible de CRISPR, contexte chromatinien, édition de bases, sûreté du génome, apprentissage automatique