Clear Sky Science · es
Descifrando el papel del contexto de la cromatina en los efectos fuera de objetivo de la edición génica CRISPR con EGOLD
Por qué pequeños ajustes del ADN pueden tener grandes efectos secundarios
La edición génica con CRISPR ha despertado la esperanza de curar muchas enfermedades genéticas al cambiar con precisión el ADN dentro de nuestras células. Pero las mismas herramientas que pueden corregir un gen defectuoso también pueden alterar por accidente otras partes del genoma, generando cambios “fuera de objetivo”. Este estudio presenta una nueva manera de mapear esas ediciones no intencionadas directamente en células humanas y revela que la forma en que el ADN está compactado dentro de la célula desempeña un papel principal en dónde ocurren dichos cambios fuera de objetivo.
Mirando más allá de las letras del ADN
La mayoría de los esfuerzos por entender la seguridad de CRISPR se centran en la secuencia de ADN: qué cadenas de A, C, G y T son más propensas a ser cortadas o modificadas. Sin embargo, el ADN en las células vivas está envuelto alrededor de proteínas y plegado en estados más abiertos o cerrados, un paisaje conocido como cromatina. Las regiones abiertas son más accesibles para las maquinarias celulares, mientras que las cerradas están más protegidas. Los autores sospechaban que este empaquetamiento local del ADN podría dirigir silenciosamente dónde las herramientas CRISPR cometen errores, pero las pruebas existentes no capturaban suficientes sitios genómicos reales para estudiar este efecto en profundidad.
Una biblioteca “natural” de off-targets a escala genómica
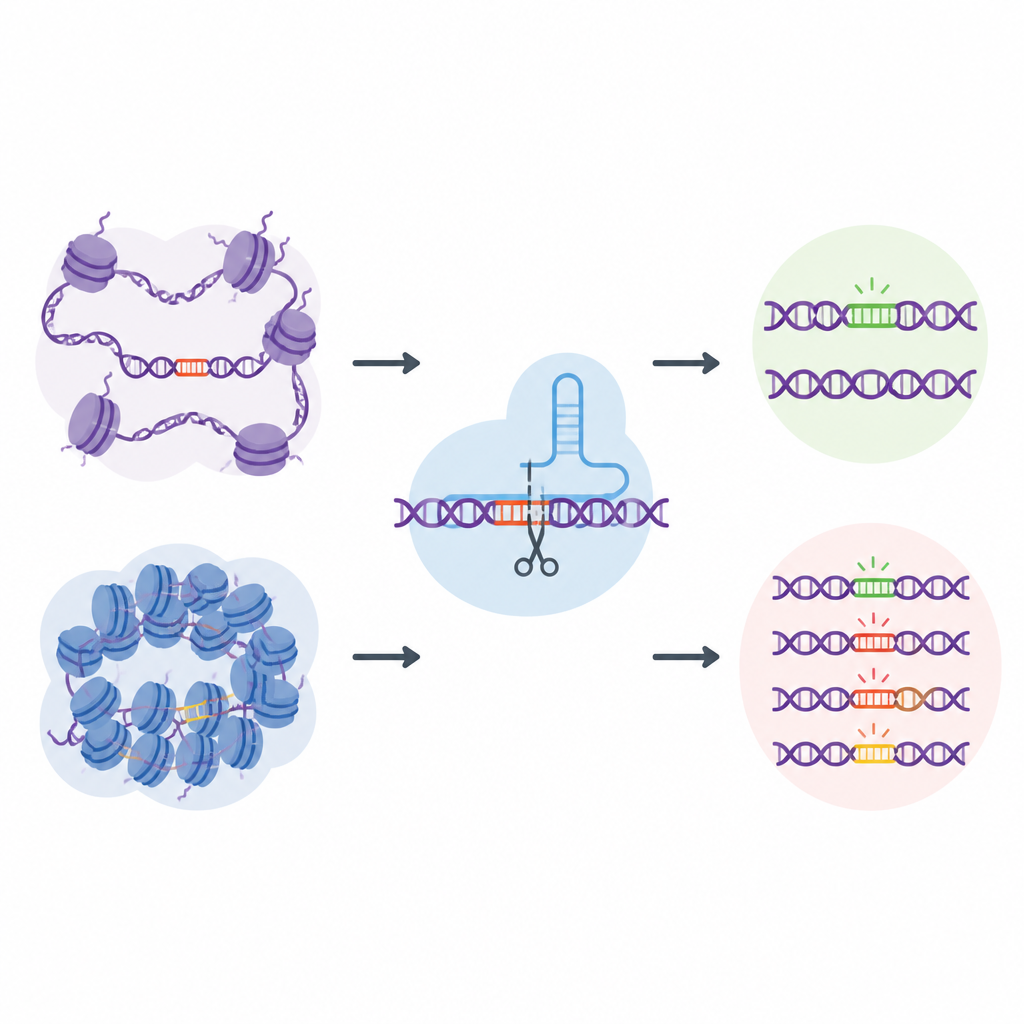
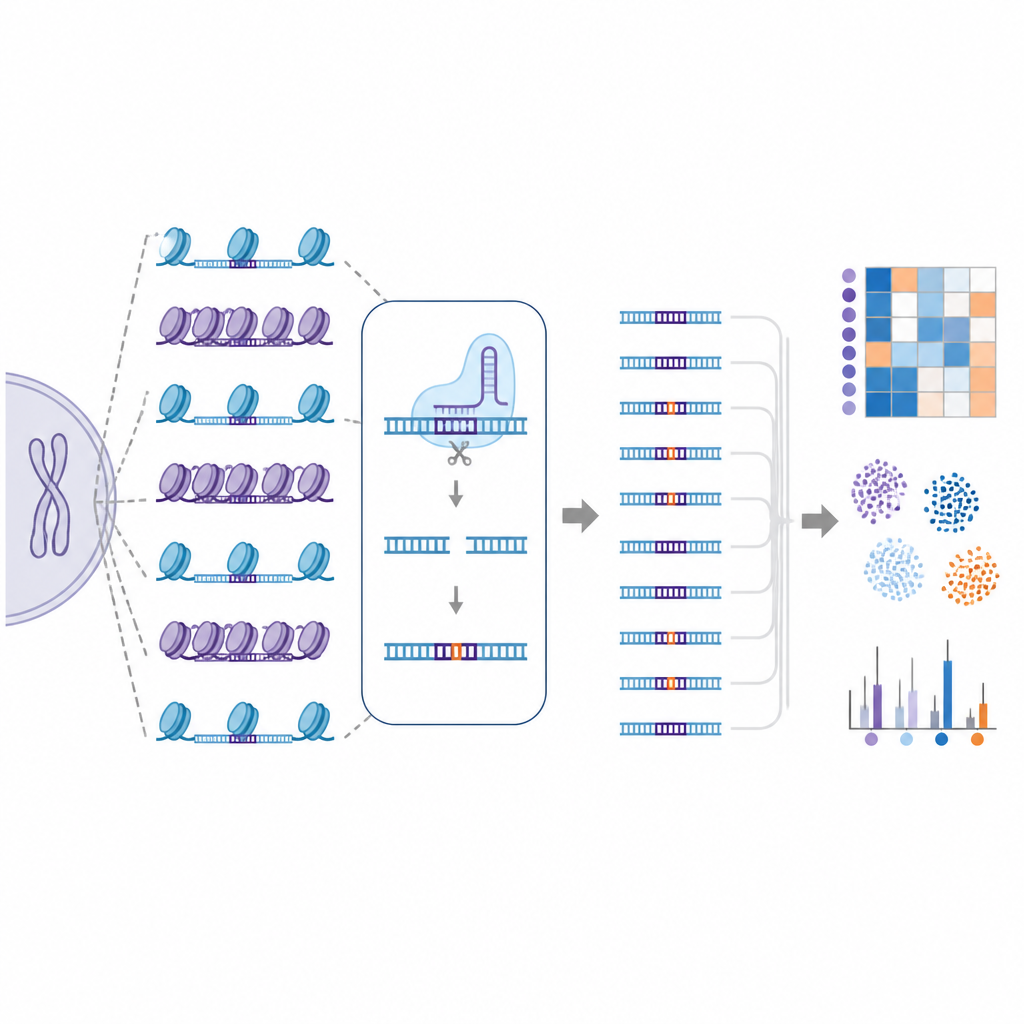
Para abordar este desafío, los investigadores crearon EGOLD, siglas en inglés de Endogenous Genome-wide Off-target Library Detection. En lugar de construir bibliotecas de ADN artificiales, aprovecharon secuencias repetidas o muy similares ya dispersas por el genoma humano. Eligieron sitios diana especiales donde una sola guía de CRISPR coincide estrechamente con miles de otras ubicaciones que comparten la misma secuencia pero se encuentran en entornos de cromatina muy diferentes. Al editar un sitio elegido y luego leer todo el genoma, EGOLD puede comparar cuáles de estos muchos sitios similares son editados y cuáles quedan intactos, todo ello mientras sus letras de ADN subyacentes permanecen idénticas.
El ADN abierto es más vulnerable a ediciones errantes
Usando EGOLD, el equipo probó 17 editores basados en CRISPR, incluidos proteínas Cas9 estándar que cortan el ADN y editores de bases más recientes que cambian letras individuales sin cortar ambas hebras. A través de más de dos millones de eventos fuera de objetivo detectados, apareció un patrón claro: los sitios en cromatina abierta eran mucho más propensos a ser editados que la misma secuencia enterrada en regiones cerradas y compactas. Señales de ADN abierto, como la accesibilidad a enzimas que cortan el ADN y marcas químicas activas en proteínas cercanas, se asociaron positivamente con la actividad fuera de objetivo. En contraste, características vinculadas al ADN fuertemente empaquetado o químicamente silenciado tendían a proteger contra cambios no deseados.
No todos los editores y células se comportan igual
El estudio también comparó diferentes variantes de Cas9 diseñadas para ser más precisas o más flexibles en lo que reconocen. Una variante llamada SuperFiCas9 destacó por mantener buena actividad en su objetivo previsto mientras producía relativamente pocos cambios fuera de objetivo, especialmente cuando se incorporaba en editores de bases. Otras versiones que toleraban más diferencias de secuencia o normas de reconocimiento más relajadas mostraron tasas de off-target mucho más altas. Incluso usando el mismo editor y la misma guía, distintos tipos de células humanas mostraron patrones de off-target diferentes, lo que subraya cómo los paisajes cromatínicos específicos de cada célula moldean los resultados de la edición.
Enseñar a las máquinas a predecir sitios de riesgo
Puesto que EGOLD genera mapas de off-target tan grandes y detallados, los autores usaron estos datos para entrenar modelos de aprendizaje automático. Estos modelos informáticos recibieron tanto información de la secuencia como características locales de la cromatina para cada sitio potencial y aprendieron a distinguir ubicaciones editadas de no editadas con muy alta precisión. Cuando se añadió información de cromatina a las características basadas en la secuencia, el rendimiento de la predicción mejoró, subrayando que el empaquetamiento del ADN no es un detalle secundario sino una pieza clave del riesgo fuera de objetivo.
Qué significa esto para una edición génica más segura
Para quienes siguen el progreso de la terapia génica, este trabajo muestra que dónde CRISPR falla está determinado no solo por la ortografía del ADN sino también por cómo ese ADN está plegado y marcado dentro de las células. EGOLD proporciona una forma práctica de trazar esos riesgos directamente en genomas reales y de construir herramientas de predicción más inteligentes que tengan en cuenta el contexto de la cromatina. A la larga, este enfoque podría ayudar a los investigadores a elegir estrategias de edición más seguras, diseñar mejores guías y seleccionar versiones de editores más adecuadas, de modo que las correcciones de ADN que cambian vidas vengan acompañadas de menos cambios no intencionados en otras partes.
Cita: Feng, H., Zheng, J., Li, N. et al. Decoding the role of chromatin context in the off-target effects of CRISPR gene editing with EGOLD. Cell Discov 12, 32 (2026). https://doi.org/10.1038/s41421-026-00889-2
Palabras clave: Off-targets de CRISPR, contexto de la cromatina, edición de bases, seguridad genómica, aprendizaje automático