Clear Sky Science · zh
A20通过促进occludin降解增强胃癌细胞的迁移和转移
为何重要
胃癌,即胃部恶性肿瘤,是世界上致死率较高的肿瘤之一,主要原因在于它常在被发现前就已扩散。本研究揭示了一个与炎症相关的单一蛋白A20如何帮助胃癌细胞从邻近细胞中脱离并迁移到远处器官。通过阐明这一隐蔽的逃逸通路,这项工作指出了未来医生可能减缓或阻断胃癌转移的新途径。
位于癌症与炎症交汇处的蛋白
临床上早已知道,诸如长期感染等造成的慢性胃部炎症会增加胃癌风险。A20通常是一种有助于抑制炎性信号的蛋白,但在若干癌症中它表现得更像促进肿瘤生长的因子。研究者首先询问人体胃肿瘤中的A20水平是否与癌症的侵袭性有关。对122例患者的肿瘤样本分析显示,A20水平高的肿瘤更具侵袭性,更容易转移到淋巴结和远处部位,且与较差的生存率相关。这些临床数据提示A20并非单纯旁观者,可能积极推动胃癌的恶化。
A20如何帮助癌细胞解除黏附
要发生转移,癌细胞必须放松通常把相邻细胞牢固连接在一起的紧密结合。许多组织中这些结合的关键成分是一种名为occludin的蛋白,它有助于形成紧密连接,像分子拉链齿一样把细胞连接起来。在体外培养的胃癌细胞系中,研究者证明提高A20水平会使细胞更易扩散并迁移更快,而降低A20则有相反效果。他们注意到当A20升高时,细胞表面的occludin丢失并转移到细胞内部。单独沉默occludin就足以增加癌细胞的运动,表明失去这一“拉链”是允许细胞游走的关键步骤。
通过内部降解关闭细胞“拉链”
团队接着探究A20使occludin消失的机制。细胞不断回收表面蛋白,通过小囊将它们内吞,然后或被再利用或被销毁。研究发现A20加速了occludin从细胞表面进入这些内吞囊泡并进而进入类似细胞回收中心的消化室的过程。阻断蛋白酶体的蛋白降解并不能挽救occludin,但阻断内吞或阻断称为溶酶体的酸性囊泡则能。处于这些阻断条件下,即使A20丰富,癌细胞的迁移也减少。综上,这些实验表明A20通过促进occludin的内化和溶酶体降解来削弱细胞间屏障,从而鼓励癌细胞扩散。
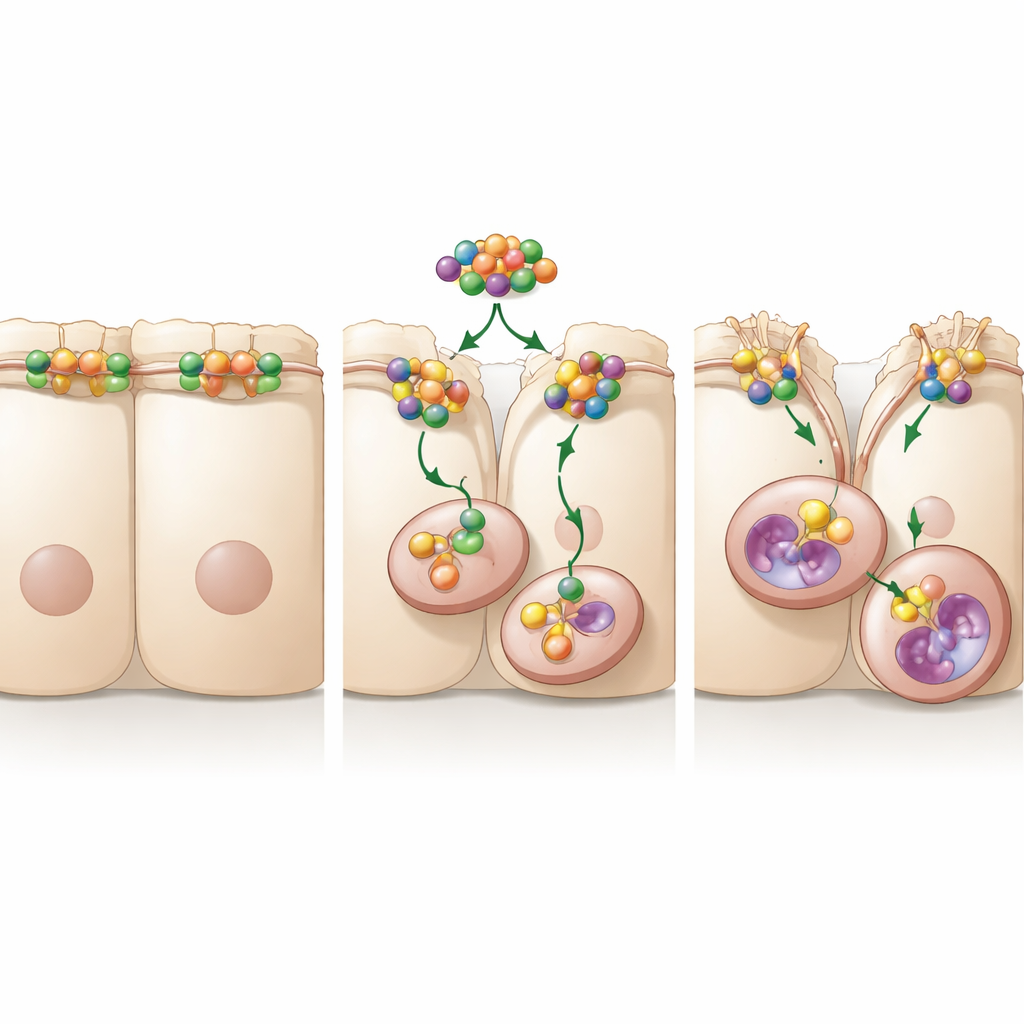
稳定运动开关的信号传递接力
深入研究时,研究者寻找可能让A20控制细胞运动的伙伴。他们发现A20与RhoA结合,RhoA是一种众所周知可重塑细胞内部骨架并松弛细胞间连接的小分子开关。当A20存在时,RhoA的含量和活性更高,下游促使细胞纤维变强的信号也延长。减少或化学抑制RhoA时,occludin水平上升,细胞迁移减慢,即便A20高亦如此。研究锁定了A20的一个特定区域——OTU结构域,表明其必不可少:当该区域发生突变,A20不能再稳定RhoA,不能维持将occludin内吞的信号,也不能增强细胞运动。这表明A20作为RhoA的保护者,防止其被标记销毁,从而保持运动机制处于开启状态。
对未来治疗的意义
简而言之,这项工作表明A20通过保护一个运动开关(RhoA)并触发关键“拉链”蛋白(occludin)的内部降解,帮助胃癌细胞逃逸。A20含量较高的肿瘤更容易深入侵袭和转移,患此类肿瘤的患者预后更差。通过描绘出A20–RhoA–occludin通路,研究突出了若干潜在干预点,例如干扰A20的OTU结构域、降低RhoA活性或阻止occludin被导向溶酶体的药物。尽管此类治疗尚不可用,且需要在不损害A20正常调控炎症功能的前提下慎重权衡,但这些发现为减缓或阻止胃癌致命转移的研究提供了更清晰的靶点。
引用: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
关键词: 胃癌, 转移, 细胞连接, 炎症, RhoA信号