Clear Sky Science · pl
A20 zwiększa migrację i przerzuty komórek raka żołądka przez promowanie degradacji okludyny
Dlaczego to ważne
Rak żołądka jest jednym z najgroźniejszych nowotworów na świecie, głównie dlatego, że często rozprzestrzenia się zanim zostanie wykryty. Badanie to ujawnia, jak pojedynczy białkowy czynnik związany z zapaleniem, zwany A20, pomaga komórkom raka żołądka odrywać się od sąsiednich komórek i przemieszczać do odległych narządów. Odkrycie tej ukrytej drogi ucieczki wskazuje nowe możliwości, które w przyszłości mogłyby pozwolić lekarzom spowolnić lub zablokować rozsiew raka żołądka.
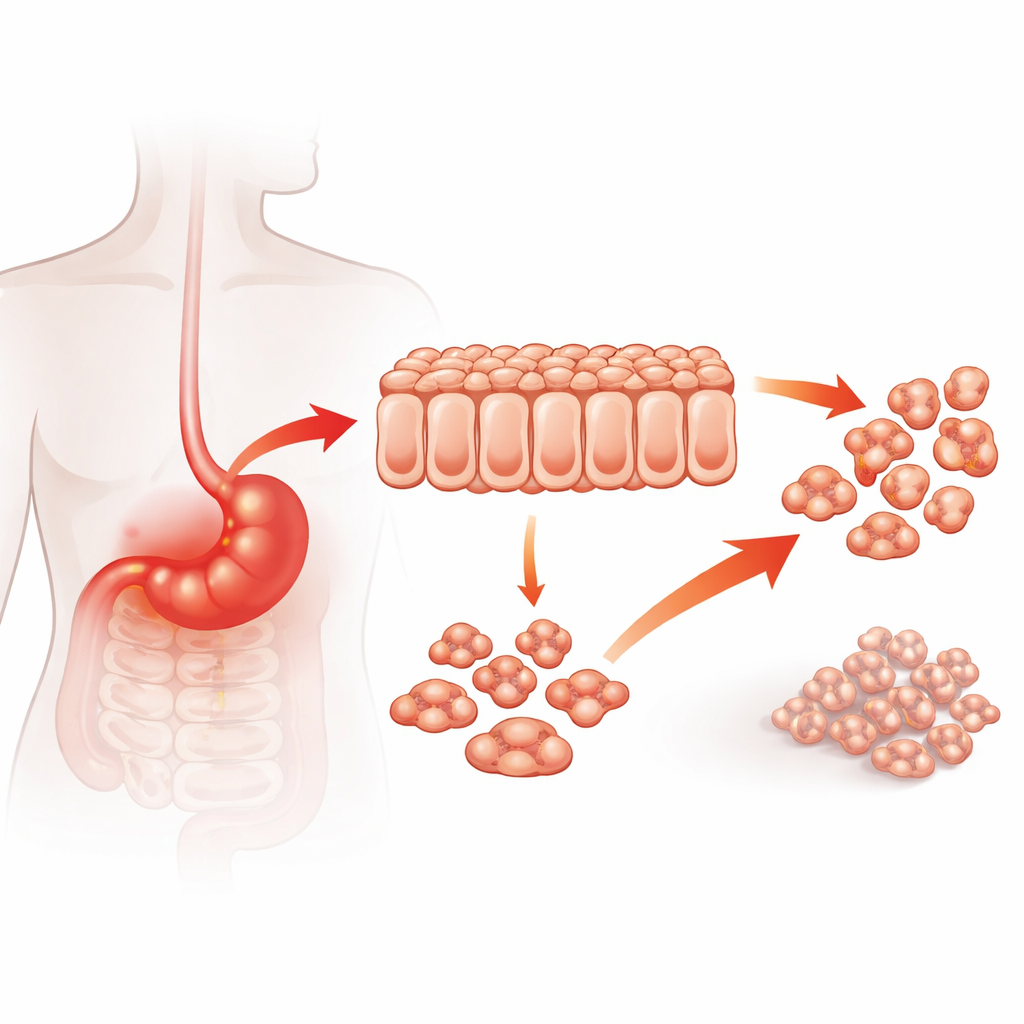
Białko na skrzyżowaniu raka i zapalenia
Lekarze od dawna wiedzą, że przewlekłe zapalenie w żołądku, np. wywołane długotrwałą infekcją, zwiększa ryzyko raka żołądka. A20 to białko, które zwykle pomaga kontrolować sygnały zapalne, ale w kilku nowotworach zachowuje się jak promotor wzrostu guza. Autorzy zaczęli od pytania, czy poziomy A20 w ludzkich guzach żołądka korelują z agresywnością nowotworu. Analiza próbek guzów od 122 pacjentów wykazała, że nowotwory o wysokim poziomie A20 były bardziej inwazyjne, częściej zajmowały węzły chłonne i odległe miejsca oraz wiązały się z gorszym przeżyciem. Dane kliniczne sugerują więc, że A20 nie jest tylko biernym obserwatorem, lecz może aktywnie napędzać pogarszanie się raka żołądka.
Jak A20 pomaga komórkom nowotworowym zerwać więzi
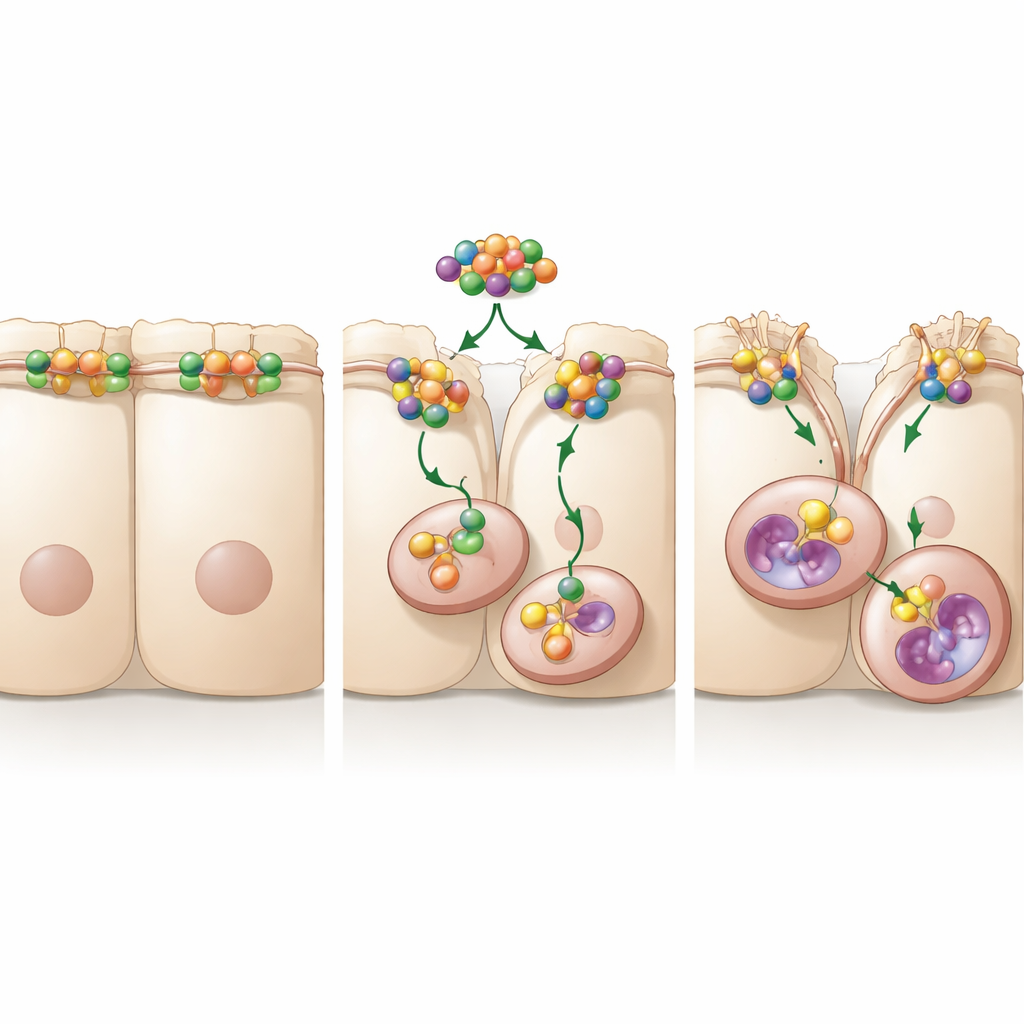
Aby komórki nowotworowe mogły dać przerzuty, muszą poluzować ciasne połączenia, które normalnie trzymają sąsiednie komórki razem. Kluczowym składnikiem tych połączeń w wielu tkankach jest białko okludyna, które pomaga tworzyć połączenia zwane tight junctions, działające jak zęby zamka molekularnego między komórkami. W liniach komórkowych raka żołądka hodowanych w laboratorium badacze pokazali, że zwiększenie poziomu A20 sprawia, iż komórki się rozprzestrzeniają i szybciej migrują, natomiast zmniejszenie A20 daje efekt odwrotny. Zaobserwowali, że przy wysokim A20 okludyna z powierzchni komórki zanika i przemieszcza się do wnętrza komórki. Uciszenie okludyny samo w sobie wystarczyło, by zwiększyć ruchliwość komórek nowotworowych, co wskazuje, że utrata tego „zamka” jest kluczowym krokiem umożliwiającym wędrówkę komórek.
Przygaszanie komórkowego „zamka” przez wewnętrzne rozdrabnianie
Zespół następnie zbadał, jak A20 powoduje znikanie okludyny. Komórki nieustannie recyklingują swoje białka powierzchniowe, wpuklając je do wnętrza w małych kieszonkach i kierując je albo do ponownego użycia, albo do zniszczenia. Badanie wykazało, że A20 przyspiesza drogę okludyny z powierzchni komórki do tych wewnętrznych kieszonek, a następnie do lizosomów — kompartmentów trawiących białka, pełniących rolę komórkowych centrów recyklingu. Zablokowanie maszynerii rozkładającej białka w proteasomie nie przywróciło okludyny, natomiast zahamowanie endocytozy lub lizosomalnych kwaśnych pęcherzyków tak. W warunkach tych blokad komórki nowotworowe migrowały mniej, nawet przy wysokim A20. Razem eksperymenty te pokazują, że A20 sprzyja szerzeniu się raka, promując internalizację i lizosomalną degradację okludyny, osłabiając barierę między komórkami.
Przekaźnik sygnałowy stabilizujący włącznik ruchliwości
Idąc głębiej, badacze szukali partnerów, którzy umożliwialiby A20 kontrolę ruchu komórek. Odkryli, że A20 wiąże się z RhoA, małym molekularnym włącznikiem znanym z przekształcania wewnętrznego rusztowania komórkowego i rozluźniania połączeń między komórkami. Gdy A20 był obecny, poziomy i aktywność RhoA były wyższe, a sygnały prowadzące do utwardzania włókien komórkowych były wydłużone. Gdy RhoA został zredukowany lub chemicznie zablokowany, poziomy okludyny wracały do normy, a migracja komórek spowalniała, nawet przy wysokim A20. Badanie wskazało konkretny region A20, zwany domeną OTU, jako niezbędny: gdy ten region był zmutowany, A20 nie mogło już stabilizować RhoA, nie utrzymywało sygnałów potrzebnych do wciągania okludyny i nie zwiększało ruchliwości komórek. To sugeruje, że A20 działa jak strażnik RhoA, chroniąc go przed oznaczaniem do usunięcia i utrzymując maszynerię ruchu w stanie aktywnym.
Co to może znaczyć dla przyszłych terapii
W skrócie, praca ta pokazuje, że A20 pomaga komórkom raka żołądka uciekać, chroniąc włącznik ruchliwości (RhoA) i wywołując wewnętrzne rozdrabnianie kluczowego komórkowego zamka (okludyny). Guzy z wyższym poziomem A20 mają większą zdolność do głębokiej inwazji i rozsiewu, a pacjenci z takimi guzami mają gorsze rokowania. Mapując szlak A20–RhoA–okludyna, badanie wskazuje kilka potencjalnych punktów interwencji, takich jak leki zaburzające domenę OTU A20, zmniejszające aktywność RhoA lub zapobiegające kierowaniu okludyny do lizosomów. Chociaż takie terapie nie są jeszcze dostępne i wymagałyby ostrożnego wyważenia z normalnymi rolami A20 w kontroli zapalenia, wyniki dostarczają jaśniejszego celu dla działań mających na celu spowolnienie lub zapobieganie śmiertelnemu rozsiewowi raka żołądka.
Cytowanie: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Słowa kluczowe: rak żołądka, przerzuty, łączenia komórkowe, zapalanie, szlak sygnałowy RhoA