Clear Sky Science · de
A20 fördert Migration und Metastasierung von Magenkrebszellen durch Förderung des Abbaus von Occludin
Warum das wichtig ist
Magenkrebs, also Krebs des Magens, gehört zu den weltweit tödlichsten Tumoren, vor allem weil er oft schon gestreut hat, bevor er entdeckt wird. Diese Studie enthüllt, wie ein einzelnes, mit Entzündung verknüpftes Protein namens A20 Krebszellen im Magen dabei unterstützt, sich von ihren Nachbarn zu lösen und in entfernte Organe zu wandern. Indem sie diese versteckte Fluchtroute aufdeckt, zeigt die Arbeit mögliche neue Ansätze auf, mit denen Ärztinnen und Ärzte eines Tages das Fortschreiten oder die Ausbreitung von Magenkrebs verlangsamen oder blockieren könnten.
Ein Protein an der Schnittstelle von Krebs und Entzündung
Bereits länger ist bekannt, dass chronische Entzündungen im Magen, etwa durch langjährige Infektionen, das Risiko für Magenkrebs erhöhen. A20 ist ein Protein, das normalerweise hilft, entzündliche Signale zu dämpfen, sich in mehreren Krebsarten jedoch eher wie ein Förderelement des Tumorwachstums verhält. Die Autorinnen und Autoren fragten zunächst, ob die A20-Spiegel in menschlichen Magen-Tumoren mit der Aggressivität des Krebses zusammenhängen. Bei der Analyse von Tumorproben von 122 Patientinnen und Patienten fanden sie, dass Tumoren mit hohen A20-Werten invasiver waren, häufiger Lymphknoten und Fernmetastasen zeigten und mit einer schlechteren Überlebensrate verbunden waren. Diese klinischen Daten legen nahe, dass A20 nicht nur ein beiläufiger Begleiter ist, sondern aktiv die Verschlechterung von Magenkrebs vorantreiben kann.
Wie A20 Krebszellen hilft, ihre Verbindungen zu lösen
Den zellulären „Reißverschluss“ durch interne Zerstückelung abschalten
Als Nächstes untersuchte das Team, wie A20 dazu führt, dass Occludin verschwindet. Zellen recyceln ihre Oberflächenproteine ständig, indem sie sie in kleinen Einstülpungen nach innen ziehen und sie entweder wiederverwenden oder zur Zerstörung weiterleiten. Die Studie ergab, dass A20 die Reise von Occludin von der Zelloberfläche in diese inneren Einstülpungen und weiter in verdauungsähnliche Kompartimente, vergleichbar mit zellulären Recyclingzentren, beschleunigt. Das Blockieren der proteasomalen Proteinabbau-Maschinerie rettete Occludin nicht, wohl aber das Hemmen der Endozytose oder der sauren Vesikel, der Lysosomen. Unter diesen Blockierbedingungen migrierten die Krebszellen weniger, selbst wenn A20 reichlich vorhanden war. Zusammen zeigen diese Experimente, dass A20 die Ausbreitung von Krebs fördert, indem es die Internalisation und lysosomale Zerstörung von Occludin begünstigt und damit die Barriere zwischen Zellen schwächt.
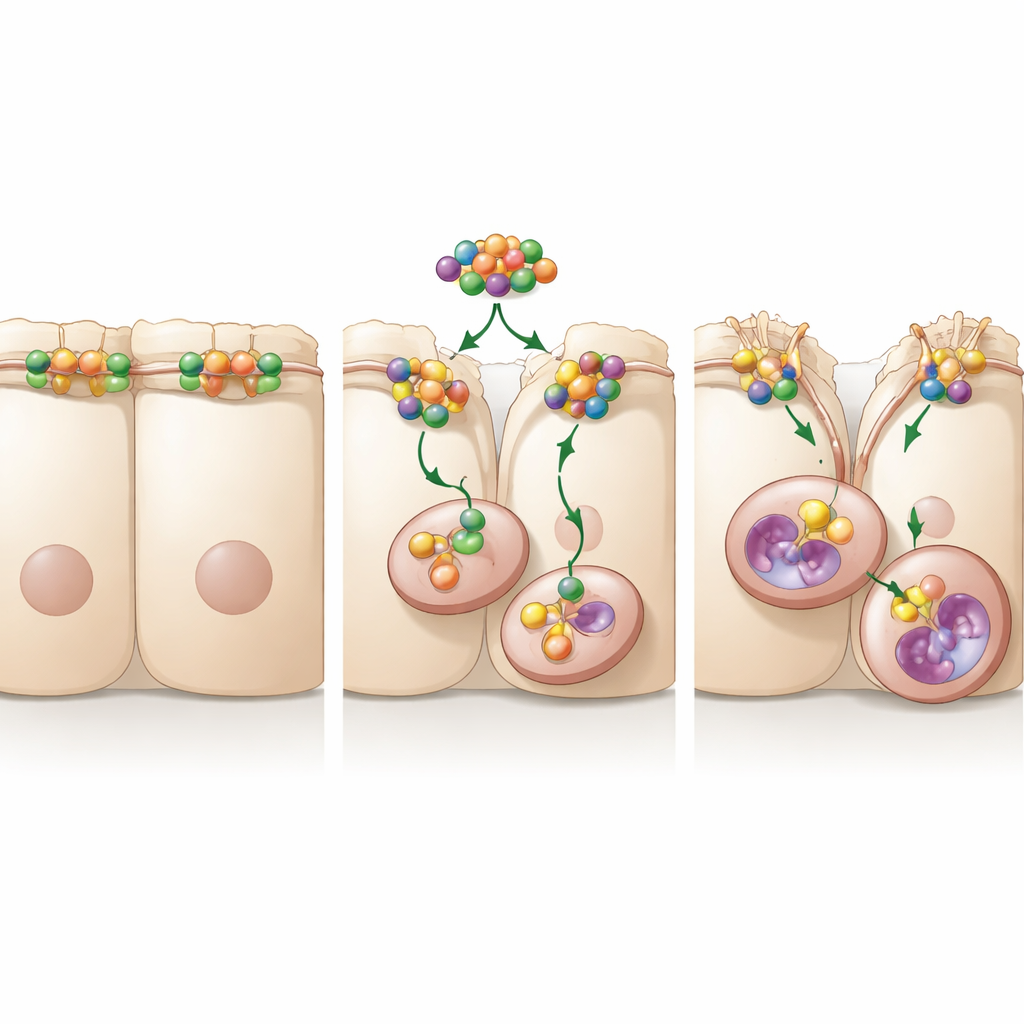
Eine Signalweiterleitung, die einen Beweglichkeitsschalter stabilisiert
Tiefergehend suchten die Forschenden nach Partnern, die A20 ermöglichen könnten, die Zellbewegung zu steuern. Sie entdeckten, dass A20 an RhoA bindet, einen kleinen molekularen Schalter, der das innere Gerüst der Zelle umgestaltet und die Verbindungen zwischen Zellen lockert. In Gegenwart von A20 waren RhoA-Spiegel und -Aktivität erhöht, und nachgeschaltete Signale, die die zellulären Fasern versteifen, dauerten länger an. Wurde RhoA reduziert oder chemisch blockiert, stiegen die Occludin-Werte wieder an und die Zellmigration verlangsamte sich, selbst wenn A20 hoch war. Die Studie identifizierte eine bestimmte Region von A20, das OTU-Domäne genannt wird, als wesentlich: Bei Mutation dieser Region konnte A20 RhoA nicht mehr stabilisieren, die für die Einziehung von Occludin erforderliche Signalgebung nicht aufrechterhalten und die Zellbewegung nicht fördern. Dies deutet darauf hin, dass A20 als Schutzpatron von RhoA wirkt, indem es dessen Markierung für den Abbau verhindert und so die Beweglichkeitsmaschinerie eingeschaltet lässt.
Was das für zukünftige Therapien bedeuten könnte
Vereinfacht gesagt zeigt diese Arbeit, dass A20 Magenkrebszellen beim Entkommen hilft, indem es einen Beweglichkeitsschalter (RhoA) schützt und die interne Zerstückelung eines wichtigen zellulären Reißverschlusses (Occludin) auslöst. Tumoren mit höherem A20 sind eher tief infiltrierend und metastasierend, und Patientinnen und Patienten mit solchen Tumoren haben schlechtere Aussichten. Durch die Kartierung dieses A20–RhoA–Occludin-Wegs hebt die Studie mehrere potenzielle Eingriffspunkte hervor, etwa Wirkstoffe, die A20s OTU-Domäne stören, RhoA-Aktivität reduzieren oder verhindern, dass Occludin zu Lysosomen weitergeleitet wird. Solche Therapien sind zwar noch nicht verfügbar und müssten sorgfältig gegen die normalen entzündungsregulierenden Funktionen von A20 abgewogen werden, doch die Ergebnisse liefern klarere Ziele für Bestrebungen, das tödliche Fortschreiten von Magenkrebs zu verlangsamen oder zu verhindern.
Zitation: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Schlüsselwörter: Magenkrebs, Metastasierung, Zellverbindungen, Entzündung, RhoA-Signalgebung