Clear Sky Science · it
A20 aumenta la migrazione e le metastasi delle cellule del cancro gastrico promuovendo la degradazione di occludina
Perché è importante
Il cancro gastrico, o tumore dello stomaco, è tra i tumori più letali al mondo in gran parte perché spesso si diffonde prima di essere diagnosticato. Questo studio rivela come una singola proteina legata all’infiammazione, chiamata A20, aiuti le cellule del cancro gastrico a staccarsi dai loro vicini e a viaggiare verso organi distanti. Svelando questa via di fuga nascosta, il lavoro indica nuovi possibili approcci che in futuro potrebbero rallentare o bloccare la diffusione del cancro gastrico.
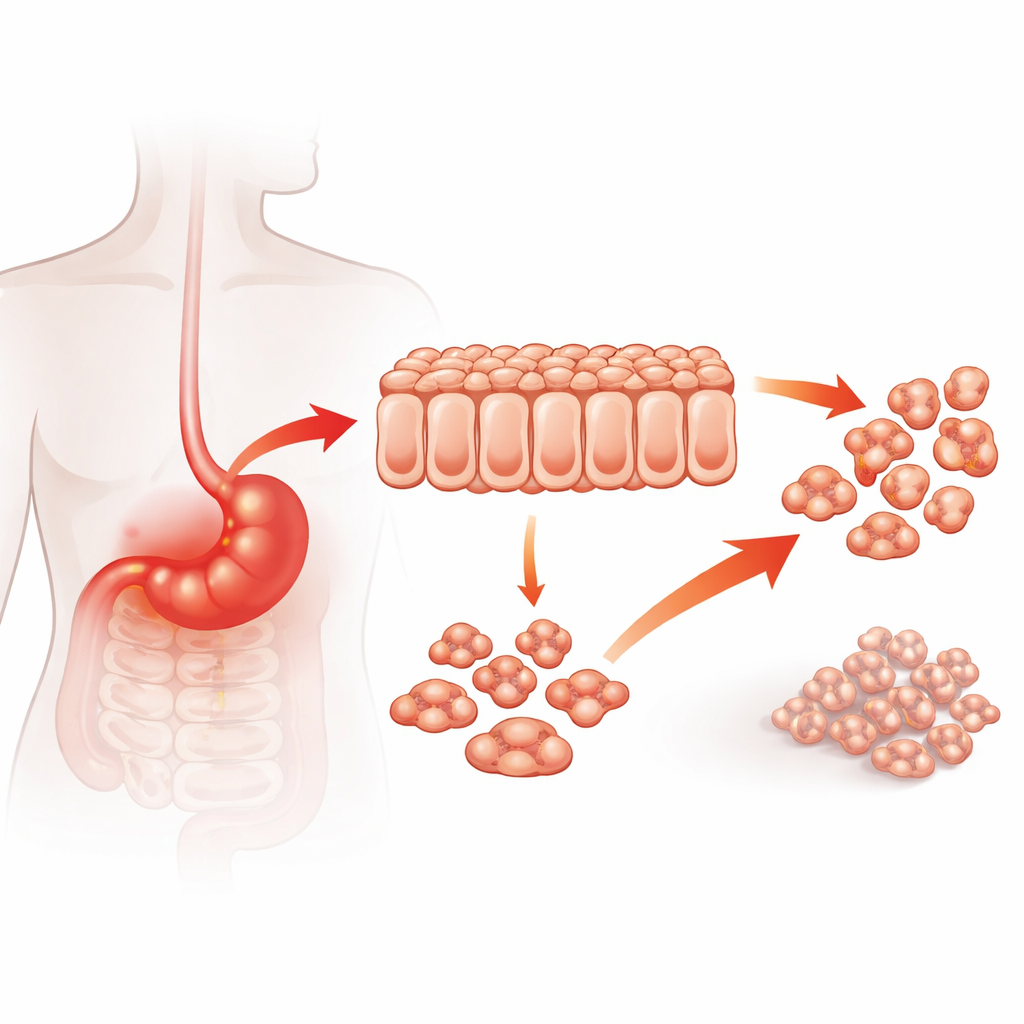
Una proteina all’incrocio tra cancro e infiammazione
Da tempo i medici sanno che l’infiammazione cronica dello stomaco, ad esempio quella causata da un’infezione prolungata, aumenta il rischio di cancro gastrico. A20 è una proteina che normalmente contribuisce a regolare i segnali infiammatori, ma in diversi tumori si comporta più come un promotore della crescita tumorale. Gli autori hanno iniziato chiedendosi se i livelli di A20 nei tumori gastrici umani fossero collegati all’aggressività del cancro. Analizzando campioni tumorali di 122 pazienti, hanno osservato che i tumori con alti livelli di A20 erano più invasivi, più propensi ad aver metastatizzato in linfonodi e sedi distanti e associati a una sopravvivenza peggiore. Questi dati clinici suggeriscono che A20 non è solo un osservatore, ma può attivamente favorire il peggioramento del cancro gastrico.
Come A20 aiuta le cellule tumorali a sciogliere i legami
Per metastatizzare, le cellule tumorali devono allentare i legami stretti che normalmente tengono insieme le cellule vicine. Un componente chiave di questi legami in molti tessuti è una proteina chiamata occludina, che contribuisce a formare le giunzioni strette, simili ai denti di una cerniera molecolare tra le cellule. In linee cellulari di cancro gastrico coltivate in laboratorio, i ricercatori hanno mostrato che aumentare i livelli di A20 ha reso le cellule più disperse e più mobili, mentre ridurre A20 ha avuto l’effetto opposto. Hanno notato che quando A20 era elevata, l’occludina alla superficie cellulare veniva persa e spostata nell’interno della cellula. Silenziare solo l’occludina è stato sufficiente ad aumentare il movimento delle cellule tumorali, indicando che la perdita di questa “cerniera” è un passaggio cruciale che permette alle cellule di allontanarsi.
Spegnere la “cerniera” cellulare attraverso la degradazione interna
Il gruppo ha poi indagato come A20 faccia scomparire l’occludina. Le cellule riciclano costantemente le proteine di superficie prelevandole in tasche interne e inviandole o al riutilizzo o alla distruzione. Lo studio ha rilevato che A20 accelera il percorso dell’occludina dalla superficie cellulare verso queste tasche interne e poi verso compartimenti digestivi simili a centri di riciclaggio della cellula. Bloccare la macchina di degradazione proteica del proteasoma non ha salvato l’occludina, mentre bloccare l’endocitosi o i sacchi acidi noti come lisosomi lo ha fatto. In presenza di questi blocchi, le cellule tumorali migravano meno, anche quando A20 era abbondante. Nel loro insieme, questi esperimenti mostrano che A20 favorisce la diffusione tumorale promuovendo l’internalizzazione e la degradazione lisosomiale dell’occludina, indebolendo la barriera tra le cellule.
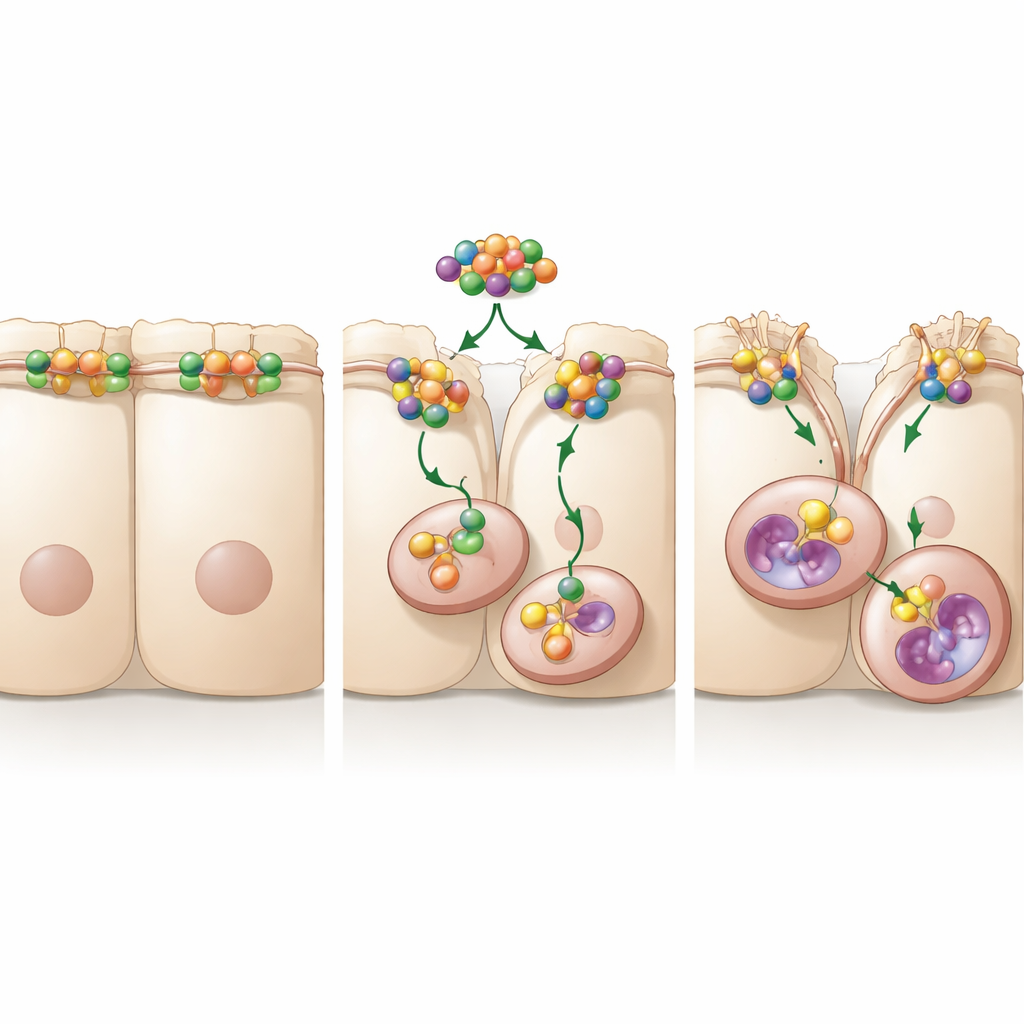
Una catena di segnalazione che stabilizza l’interruttore di motilità
Approfondendo, i ricercatori hanno cercato partner che potessero permettere ad A20 di controllare il movimento cellulare. Hanno scoperto che A20 si lega a RhoA, un piccolo interruttore molecolare noto per rimodellare lo scheletro interno della cellula e per allentare le giunzioni tra le cellule. Quando A20 era presente, i livelli e l’attività di RhoA aumentavano, e i segnali a valle che irrigidiscono le fibre cellulari duravano più a lungo. Quando RhoA veniva ridotto o bloccato chimicamente, i livelli di occludina risalivano e la migrazione cellulare rallentava, anche se A20 era elevata. Lo studio ha individuato una regione specifica di A20, chiamata dominio OTU, come essenziale: quando questa regione era mutata, A20 non riusciva più a stabilizzare RhoA, non poteva sostenere la segnalazione necessaria per internalizzare l’occludina e non aumentava la motilità cellulare. Ciò indica che A20 agisce come un guardiano di RhoA, proteggendolo dal venire taggato per la degradazione e mantenendo così attivata la macchina della motilità.
Cosa potrebbe significare per i trattamenti futuri
In termini semplici, questo lavoro mostra che A20 aiuta le cellule del cancro gastrico a sfuggire proteggendo un interruttore di motilità (RhoA) e innescando la degradazione interna di una cerniera cellulare chiave (occludina). I tumori con più A20 hanno maggiori probabilità di invadere profondamente e diffondersi, e i pazienti con questi tumori hanno esiti peggiori nel tempo. Mappando la via A20–RhoA–occludina, lo studio evidenzia diversi possibili punti di intervento, come farmaci che ostacolino il dominio OTU di A20, riducano l’attività di RhoA o impediscano che l’occludina venga diretta ai lisosomi. Sebbene tali terapie non siano ancora disponibili e richiederebbero un bilanciamento accurato rispetto ai ruoli normali di A20 nel controllo dell’infiammazione, i risultati forniscono un bersaglio più chiaro per gli sforzi volti a rallentare o prevenire la pericolosa diffusione del cancro gastrico.
Citazione: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Parole chiave: cancro gastrico, metastasi, giunzioni cellulari, infiammazione, segnalazione RhoA