Clear Sky Science · sv
A20 förstärker migrationen och metastaseringen av magsäckscancer genom att främja nedbrytning av occludin
Varför detta är viktigt
Magcancer, eller cancer i magen, är en av världens dödligaste tumörer framför allt eftersom den ofta sprider sig innan den upptäcks. Denna studie avslöjar hur ett enskilt inflammationskopplat protein, kallat A20, hjälper magcancerceller att släppa taget om sina grannar och resa till avlägsna organ. Genom att belysa denna dolda flyktrutt pekar arbetet på nya sätt som läkare i framtiden kan använda för att sakta ner eller blockera spridningen av magcancer.
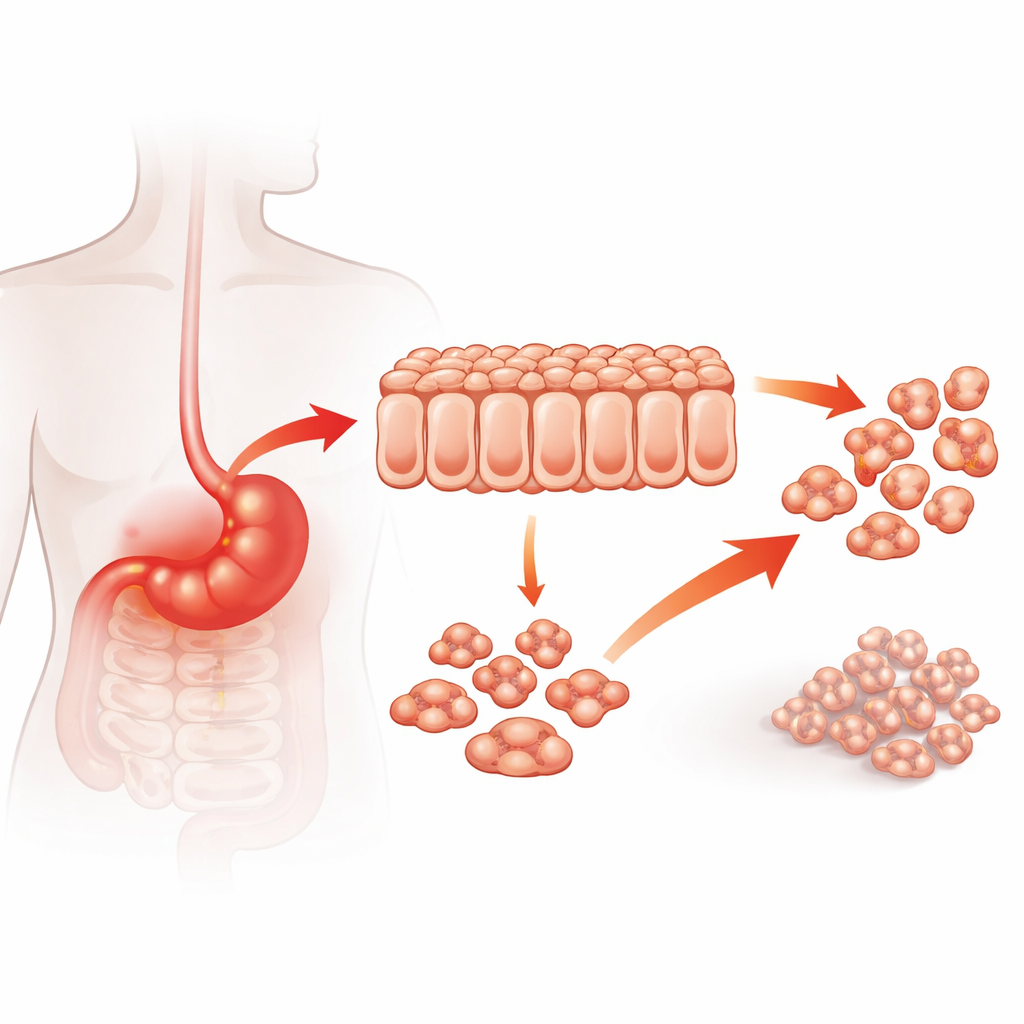
Ett protein i skärningspunkten mellan cancer och inflammation
Läkare har länge vetat att kronisk inflammation i magen, till exempel som orsakas av långvarig infektion, ökar risken för magcancer. A20 är ett protein som normalt hjälper till att hålla inflammatoriska signaler i schack, men i flera cancerformer beter det sig mer som en främjare av tumörtillväxt. Författarna började med att undersöka om A20‑nivåer i mänskliga magtumörer är kopplade till hur aggressiv cancern är. Genom att analysera tumörprover från 122 patienter fann de att tumörer med höga A20‑nivåer var mer invasiva, mer benägna att ha spridit sig till lymfkörtlar och avlägsna platser, och var associerade med sämre överlevnad. Dessa kliniska data tyder på att A20 inte bara är en åskådarprotein utan kan aktivt driva en försämring av magcancer.
Hur A20 hjälper cancerceller att släppa sina bindningar
För att cancerceller ska metastasera måste de luckra upp de täta bindningar som normalt håller intilliggande celler ihop. En nyckelkomponent i dessa bindningar i många vävnader är ett protein kallat occludin, som hjälper till att bilda täta junctions som fungerar som molekylära blixtlås mellan celler. I magcancercellinjer odlade i labbet visade forskarna att ökad A20‑nivå fick cellerna att sprida ut sig och migrera snabbare, medan minskad A20 hade motsatt effekt. De noterade att när A20 var hög försvann occludin från cellens yta och försköts in i cellens inre. Att tysta occludin ensam räckte för att öka cancercellernas rörelseförmåga, vilket visar att förlusten av detta ”blixtlås” är ett avgörande steg för att celler ska kunna vandra.
Att stänga av det cellulära ”blixtlåset” genom intern nedbrytning
Gruppen frågade sedan hur A20 får occludin att försvinna. Celler återvinner ständigt sina yta‑proteiner genom att dra in dem i små fickor och skicka dem antingen för återanvändning eller för nedbrytning. Studien fann att A20 påskyndar occludins resa från cellytan in i dessa interna fickor och vidare till matsmältningskompartiment liknande cellens återvinningscentraler. Att blockera cellens protein‑nedbrytningsmaskineri i proteasomen räddade inte occludin, men att blockera endocytos eller de sura säckarna som kallas lysosomer gjorde det. Under dessa blockeringstillstånd migrerade cancerceller mindre, även när A20 var rikligt förekommande. Tillsammans visar dessa experiment att A20 uppmuntrar cancerspridning genom att främja internalisering och lysosomal nedbrytning av occludin, vilket försvagar barriären mellan celler.
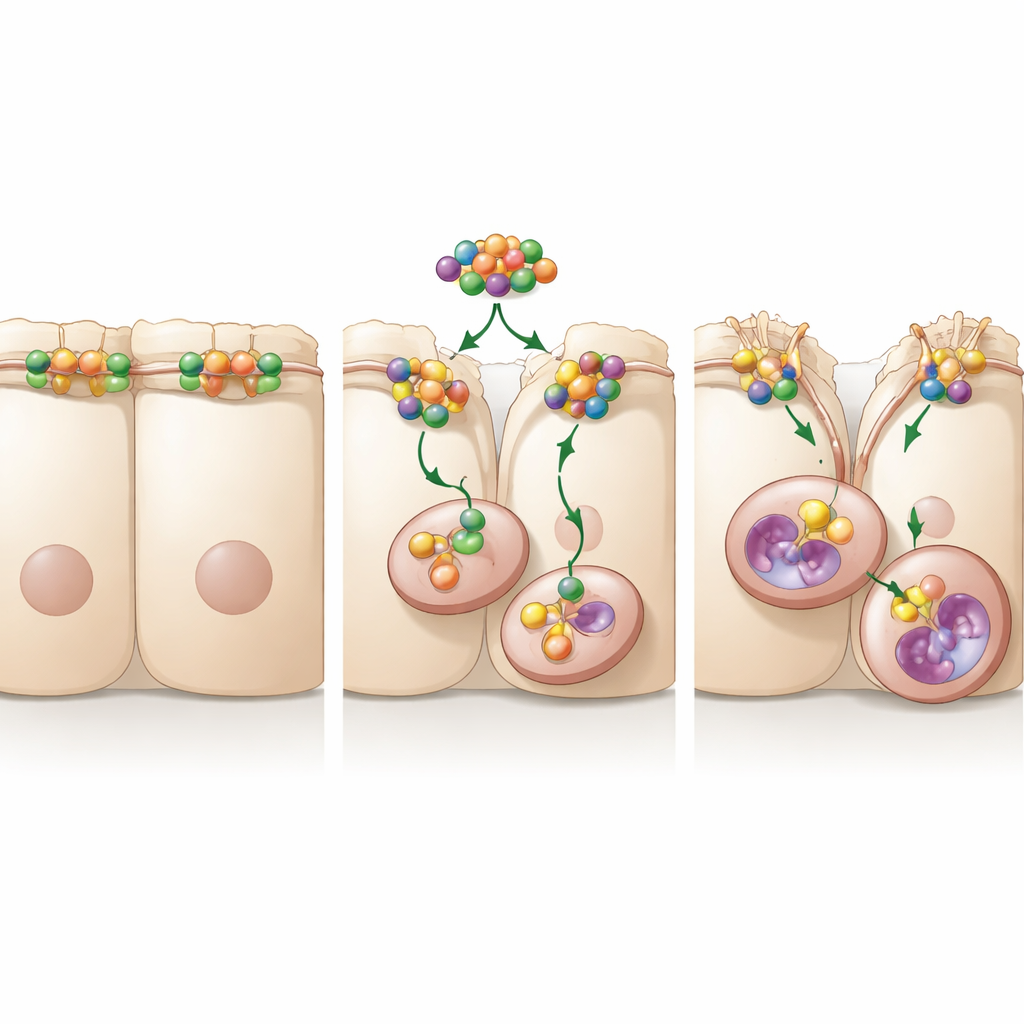
En signalväg som stabiliserar en rörelseomkopplare
För att gå djupare letade forskarna efter partners som kan tillåta A20 att reglera cellrörelse. De upptäckte att A20 binder till RhoA, en liten molekylär omkopplare som är känd för att omforma cellens inre skelett och för att luckra upp junctions mellan celler. När A20 var närvarande var RhoA‑nivåerna och dess aktivitet högre, och nedströms signaler som förstyvar cellulära fibrer var mer långvariga. När RhoA minskades eller kemiskt blockerades återgick occludin‑nivåerna och cellmigrationen saktade in, även om A20 var hög. Studien pekade ut en specifik region av A20, kallad OTU‑domänen, som avgörande: när denna region muterades kunde A20 inte längre stabilisera RhoA, kunde inte upprätthålla den signalering som behövs för att dra in occludin, och kunde inte förstärka cellrörelse. Detta visar att A20 fungerar som en väktare för RhoA, skyddar det från att märkas för nedbrytning och håller därmed rörlighetsmaskineriet påslaget.
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt visar detta arbete att A20 hjälper magcancerceller att fly genom att skydda en rörelseomkopplare (RhoA) och utlösa intern nedbrytning av ett viktigt cellulärt blixtlås (occludin). Tumörer med mer A20 har större benägenhet att invadera djupt och sprida sig, och patienter med sådana tumörer får det sämre över tid. Genom att kartlägga denna A20–RhoA–occludin‑väg lyfter studien fram flera potentiella interventionspunkter, såsom läkemedel som stör A20:s OTU‑region, minskar RhoA‑aktivitet eller förhindrar att occludin skickas till lysosomer. Även om sådana behandlingar ännu inte finns och skulle behöva balanseras noga mot A20:s normala roller i inflammationskontroll, ger fynden en tydligare måltavla för ansträngningar att sakta eller förhindra den dödliga spridningen av magcancer.
Citering: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Nyckelord: magcancer, metastasering, cellförbindelser, inflammation, RhoA‑signalering