Clear Sky Science · fr
A20 favorise la migration et les métastases des cellules du cancer gastrique en promouvant la dégradation de l’occludine
Pourquoi c’est important
Le cancer gastrique, ou cancer de l’estomac, fait partie des tumeurs les plus meurtrières au monde en grande partie parce qu’il se propage souvent avant d’être détecté. Cette étude révèle comment une seule protéine liée à l’inflammation, appelée A20, aide les cellules du cancer de l’estomac à se détacher de leurs voisines et à migrer vers des organes distants. En exposant cette voie d’évasion cachée, le travail ouvre des pistes pour que, peut‑être un jour, les médecins puissent ralentir ou bloquer la diffusion du cancer gastrique.
Une protéine au carrefour du cancer et de l’inflammation
Les cliniciens savent depuis longtemps que l’inflammation chronique de l’estomac, par exemple causée par une infection persistante, augmente le risque de cancer gastrique. A20 est une protéine qui aide habituellement à limiter les signaux inflammatoires, mais dans plusieurs cancers elle agit davantage comme un promoteur de la croissance tumorale. Les auteurs ont commencé par se demander si le niveau d’A20 dans les tumeurs gastriques humaines était lié à l’agressivité du cancer. En analysant des échantillons tumoraux de 122 patients, ils ont constaté que les tumeurs présentant des niveaux élevés d’A20 étaient plus invasives, plus susceptibles d’avoir gagné les ganglions lymphatiques et des sites distants, et étaient associées à une survie moindre. Ces données cliniques suggèrent qu’A20 n’est pas un simple spectateur mais peut activement contribuer à l’aggravation du cancer gastrique.
Comment A20 aide les cellules cancéreuses à rompre leurs liens
Pour métastaser, les cellules cancéreuses doivent desserrer les liaisons serrées qui maintiennent normalement les cellules voisines ensemble. Un composant clé de ces liaisons dans de nombreux tissus est une protéine appelée occludine, qui participe à la formation des jonctions serrées agissant comme des dents de fermeture éclair moléculaires entre les cellules. Dans des lignées cellulaires de cancer gastrique cultivées en laboratoire, les chercheurs ont montré qu’augmenter les niveaux d’A20 rendait les cellules plus étalées et plus mobiles, tandis que réduire A20 produisait l’effet inverse. Ils ont observé que lorsque A20 était élevé, l’occludine à la surface cellulaire disparaissait et se redistribuait à l’intérieur de la cellule. Le seul silence de l’occludine suffisait à accroître le mouvement des cellules cancéreuses, indiquant que la perte de cette « fermeture » est une étape cruciale permettant aux cellules de migrer.
Abaisser la « fermeture » cellulaire par destruction interne
L’équipe a ensuite cherché comment A20 provoque la disparition de l’occludine. Les cellules recyclent constamment leurs protéines de surface en les internalisant dans de petites invaginations puis en les orientant soit vers une réutilisation, soit vers la destruction. L’étude a montré qu’A20 accélère le trajet de l’occludine de la surface cellulaire vers ces compartiments internes puis vers des organites digestifs comparables à des centres de recyclage cellulaires. Bloquer la machinerie de destruction protéique dans le protéasome n’a pas permis de sauver l’occludine, mais inhiber l’endocytose ou les sacs acides appelés lysosomes l’a fait. Dans ces conditions de blocage, les cellules cancéreuses migraient moins, même lorsque A20 était abondant. Ensemble, ces expériences montrent qu’A20 favorise la dissémination tumorale en promouvant l’internalisation et la dégradation lysosomale de l’occludine, affaiblissant ainsi la barrière entre les cellules.
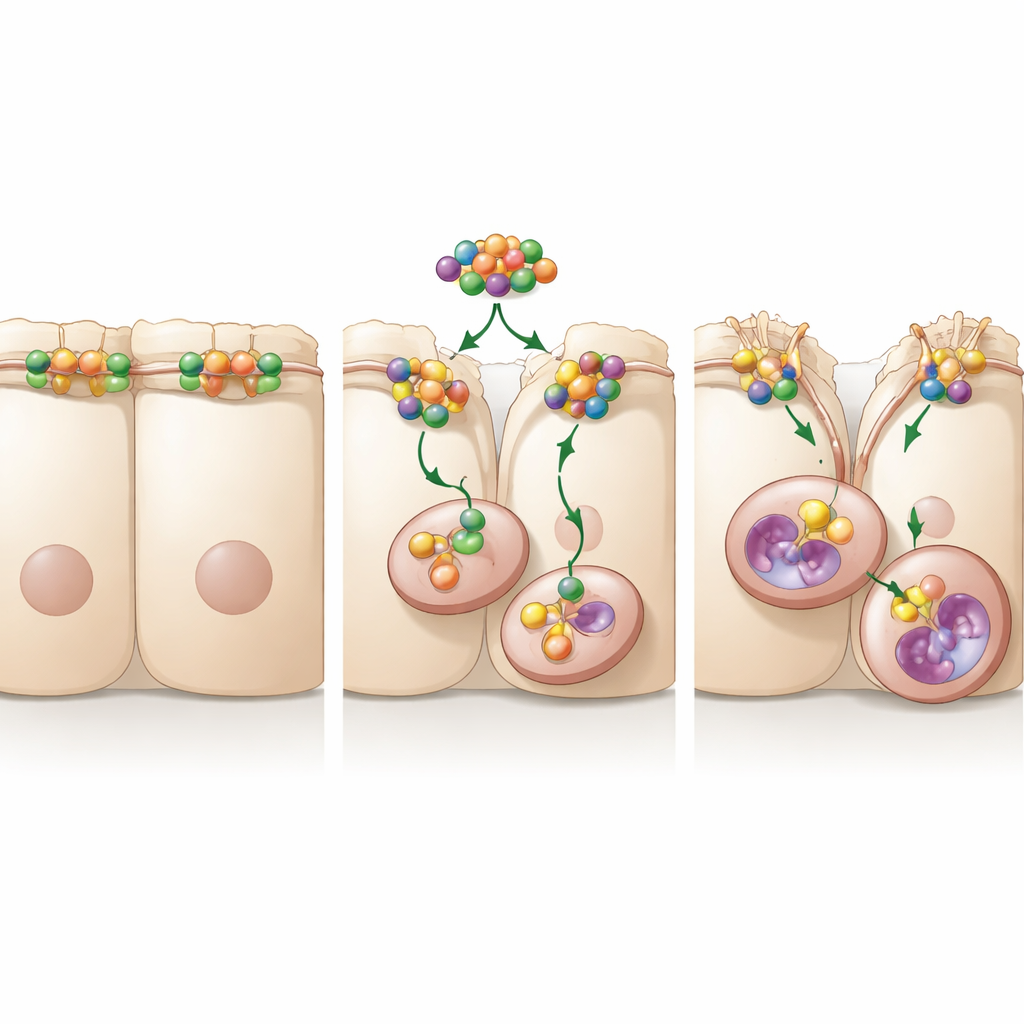
Une cascade de signalisation qui stabilise un commutateur de motilité
En creusant davantage, les chercheurs ont cherché des partenaires qui permettraient à A20 de contrôler le mouvement cellulaire. Ils ont découvert qu’A20 se lie à RhoA, un petit commutateur moléculaire connu pour remodeler l’armature interne de la cellule et relâcher les jonctions entre cellules. Lorsque A20 était présent, les niveaux et l’activité de RhoA étaient plus élevés, et les signaux en aval qui rigidifient les fibres cellulaires étaient prolongés. Lorsque RhoA était diminué ou bloqué chimiquement, les niveaux d’occludine remontaient et la migration cellulaire ralentissait, même si A20 était élevé. L’étude a identifié une région spécifique d’A20, appelée domaine OTU, comme essentielle : lorsque cette région était mutée, A20 ne pouvait plus stabiliser RhoA, ne maintenait pas la signalisation nécessaire pour internaliser l’occludine, et n’augmentait plus la mobilité cellulaire. Cela indique qu’A20 agit comme un gardien de RhoA, le protégeant du marquage destiné à sa destruction et maintenant ainsi activé le mécanisme de motilité.
Ce que cela pourrait signifier pour de futurs traitements
En termes simples, ce travail montre qu’A20 aide les cellules du cancer gastrique à s’échapper en protégeant un commutateur de motilité (RhoA) et en déclenchant la destruction interne d’une fermeture cellulaire clé (occludine). Les tumeurs riches en A20 sont plus susceptibles d’envahir profondément et de se propager, et les patients porteurs de telles tumeurs ont des résultats cliniques plus défavorables au fil du temps. En cartographiant cette voie A20–RhoA–occludine, l’étude met en lumière plusieurs points d’intervention potentiels, comme des médicaments qui perturbent le domaine OTU d’A20, réduisent l’activité de RhoA ou empêchent l’acheminement de l’occludine vers les lysosomes. Bien que de tels traitements ne soient pas encore disponibles et devraient être soigneusement équilibrés avec les rôles normaux d’A20 dans le contrôle de l’inflammation, ces résultats fournissent une cible plus claire pour les efforts visant à ralentir ou prévenir la propagation mortelle du cancer gastrique.
Citation: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Mots-clés: cancer gastrique, métastase, jonctions cellulaires, inflammation, signalisation RhoA