Clear Sky Science · ar
يعزّز A20 هجرة وخَباثة خلايا سرطان المعدة عن طريق تعزيز تَحلّل الأوكلودين
لماذا هذا مهم
سرطان المعدة، أو سرطان المعدة، يعد من أخطر الأورام في العالم إلى حد كبير لأنه غالباً ما ينتشر قبل اكتشافه. يكشف هذا البحث كيف يساعد بروتين مرتبط بالالتهاب، يُسمّى A20، خلايا سرطان المعدة على الانفصال عن جيرانها والسفر إلى أعضاء بعيدة. من خلال كشف هذا المسار الخفي للهروب، يشير العمل إلى طرق جديدة قد تتمكن الأطباء في المستقبل من خلالها إبطاء أو منع انتشار سرطان المعدة.
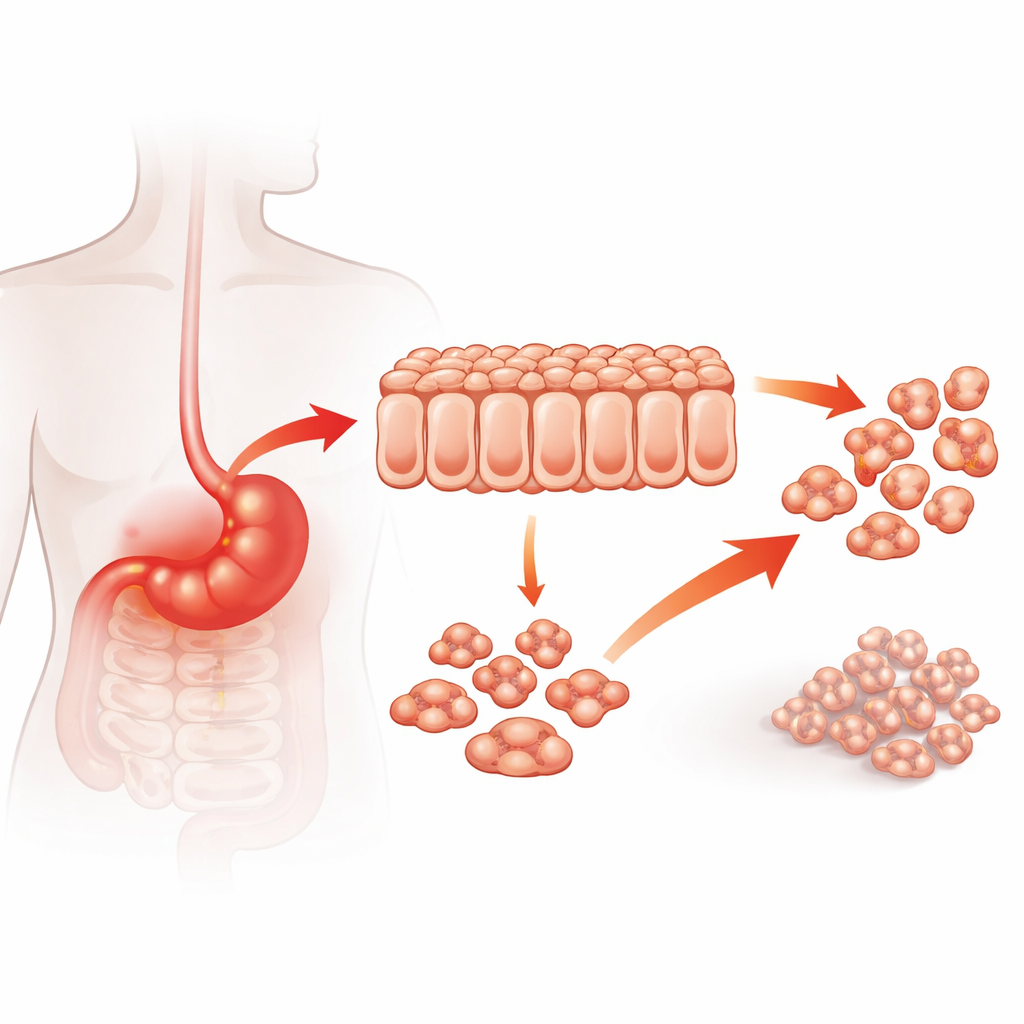
بروتين عند تقاطع السرطان والالتهاب
يعرف الأطباء منذ زمن طويل أن الالتهاب المزمن في المعدة، مثل ذلك الناتج عن عدوى طويلة الأمد، يزيد من خطر الإصابة بسرطان المعدة. يعمل A20 عادةً على ضبط الإشارات الالتهابية، لكن في عدة أنواع من السرطان يتصرف كعامل يروج لنمو الورم. بدأ المؤلفون بسؤال ما إذا كانت مستويات A20 في أورام المعدة البشرية مرتبطة بشدة السرطان. من خلال تحليل عينات أورام من 122 مريضاً، وجدوا أن الأورام ذات المستويات العالية من A20 كانت أكثر غزوًا، وأكثر عرضة للانتشار إلى الغدد الليمفاوية والمواقع البعيدة، وكانت مرتبطة ببقاء أسوأ. تشير هذه البيانات السريرية إلى أن A20 ليس مجرد متفرج بل قد يدفع فعلاً تدهور سرطان المعدة.
كيف يساعد A20 الخلايا السرطانية على الانفلات من روابطها
لكي تنتشر الخلايا السرطانية، يجب أن تُرخّي الروابط المحكمة التي تربط الخلايا المجاورة عادةً. مكوّن رئيسي لهذه الروابط في العديد من الأنسجة هو بروتين يُسمّى الأوكلودين، الذي يساعد في تشكيل الوصلات الضامة التي تعمل كأسنان سحّاب جزيئي بين الخلايا. في خطوط خلايا سرطان المعدة المزروعة في المختبر، أظهر الباحثون أن زيادة مستويات A20 جعلت الخلايا تتوسع وتهاجر أسرع، في حين أن تقليل A20 أعطى تأثيراً معاكساً. لاحظوا أنه عندما كان A20 عالياً، اختفى الأوكلودين من سطح الخلايا وتحول إلى الداخل الخلوي. كَفَيَ إسكات الأوكلودين بمفرده لزيادة حركة الخلايا السرطانية، مما يدل على أن فقدان هذا "السحّاب" خطوة حاسمة تسمح للخلايا بالتجوال.
تخفيض "السحّاب" الخلوي عبر التقطيع الداخلي
سأل الفريق بعد ذلك كيف يتسبب A20 في اختفاء الأوكلودين. تقوم الخلايا دائماً بإعادة تدوير بروتيناتها السطحية بسحبها إلى داخل حُقَن صغيرة ثم إرسالها إما لإعادة الاستخدام أو للتدمير. وُجد أن A20 يسرّع رحلة الأوكلودين من سطح الخلية إلى هذه الحُقَن الداخلية ثم إلى حُجُرات هضمية تشبه مراكز إعادة التدوير الخلوية. لم تؤدِ حاجبة آلية تكسير البروتين في البروتيزوم إلى إنقاذ الأوكلودين، لكن حجب الالتقام الخلوي أو الأكياس الحمضية المعروفة بالليزوزومات فعل ذلك. تحت هذه الظروف المحجوبة، هاجرت الخلايا السرطانية أقل، حتى عندما كان A20 وفيراً. توضح هذه التجارب مجتمعة أن A20 يشجع على انتشار السرطان عن طريق تعزيز الإدخال الداخلي وتحلل الأوكلودين في الليزوزومات، مما يضعف الحاجز بين الخلايا.
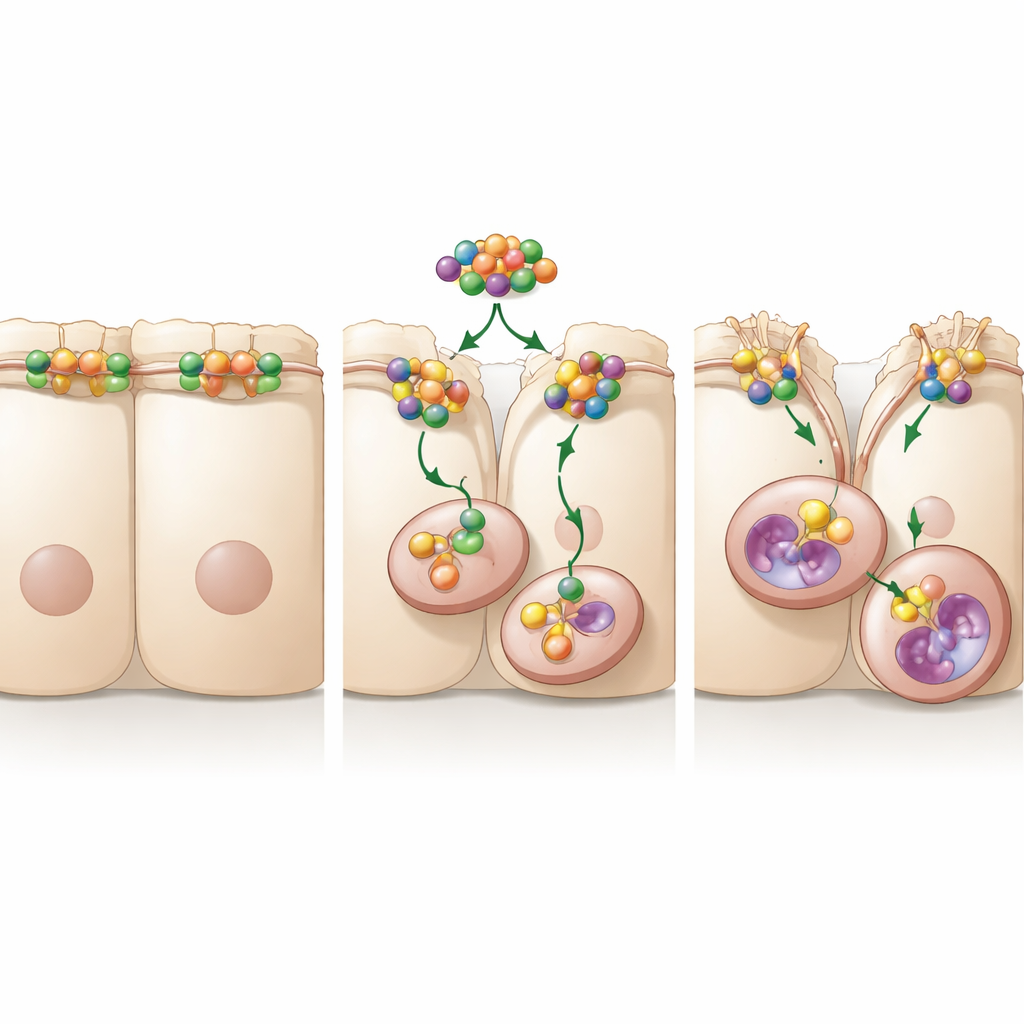
تتابع إشاري يثبت مفتاح الحركة
بحث الباحثون أعمق عن شركاء قد يسمحون لـA20 بالتحكم في حركة الخلية. اكتشفوا أن A20 يرتبط بـRhoA، مفتاح جزيئي صغير معروف بإعادة تشكيل هيكل الخلية الداخلي وإرخاء الوصلات بين الخلايا. عندما كان A20 حاضراً، كانت مستويات RhoA ونشاطه أعلى، وكانت الإشارات اللاحقة التي تُقوّي ألياف الخلية مطوَّلة. عندما انخفض RhoA أو حُجِم كيميائياً، عادت مستويات الأوكلودين للارتفاع وبطأت هجرة الخلايا، حتى لو كان A20 عالياً. حددت الدراسة منطقة محددة في A20 تُسمّى مجال OTU على أنها جوهرية: عندما طُفِّرَت هذه المنطقة، لم يعد بإمكان A20 تثبيت RhoA، ولم يتمكن من الحفاظ على الإشارات اللازمة لسحب الأوكلودين إلى الداخل، وفشل في تعزيز حركة الخلايا. وهذا يشير إلى أن A20 يعمل كحارس لـRhoA، يحميه من وسمه للتخلص وبذلك يبقي آلة الحركة مشغّلة.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
ببساطة، تُظهر هذه الدراسة أن A20 يساعد خلايا سرطان المعدة على الهروب عن طريق حماية مفتاح الحركة (RhoA) وإطلاق التمزق الداخلي لسحّاب خلوي رئيسي (الأوكلودين). الأورام ذات مستويات A20 الأعلى أكثر ميلاً للاختراق والانتشار، والمرضى المصابون بهذه الأورام يتدهور وضعهم مع الزمن. من خلال رسم خريطة لمسار A20–RhoA–الأوكلودين، تسلّط الدراسة الضوء على عدة نقاط تدخل محتملة، مثل أدوية تعطل مجال OTU في A20، أو تقلّل نشاط RhoA، أو تمنع توجيه الأوكلودين إلى الليزوزومات. وعلى الرغم من أن مثل هذه العلاجات غير متاحة بعد وستحتاج إلى موازنة دقيقة مع الأدوار الطبيعية لـA20 في ضبط الالتهاب، توفر النتائج هدفاً أوضح لجهود إبطاء أو منع الانتشار المميت لسرطان المعدة.
الاستشهاد: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
الكلمات المفتاحية: سرطان المعدة, النقائل, وصلات الخلايا, الالتهاب, إشارة RhoA