Clear Sky Science · ru
A20 усиливает миграцию и метастазирование клеток рака желудка, способствуя деградации окклюдина
Почему это важно
Рак желудка — одно из самых смертоносных злокачественных новообразований в мире в основном потому, что он часто распространяется до того, как его обнаружат. В этом исследовании показано, как один белок, связанный с воспалением и называемый A20, помогает клеткам рака желудка отрываться от соседей и мигрировать в отдалённые органы. Выявляя этот скрытый путь побега, работа указывает на новые возможные подходы, с помощью которых врачи в будущем могли бы замедлить или заблокировать распространение рака желудка.
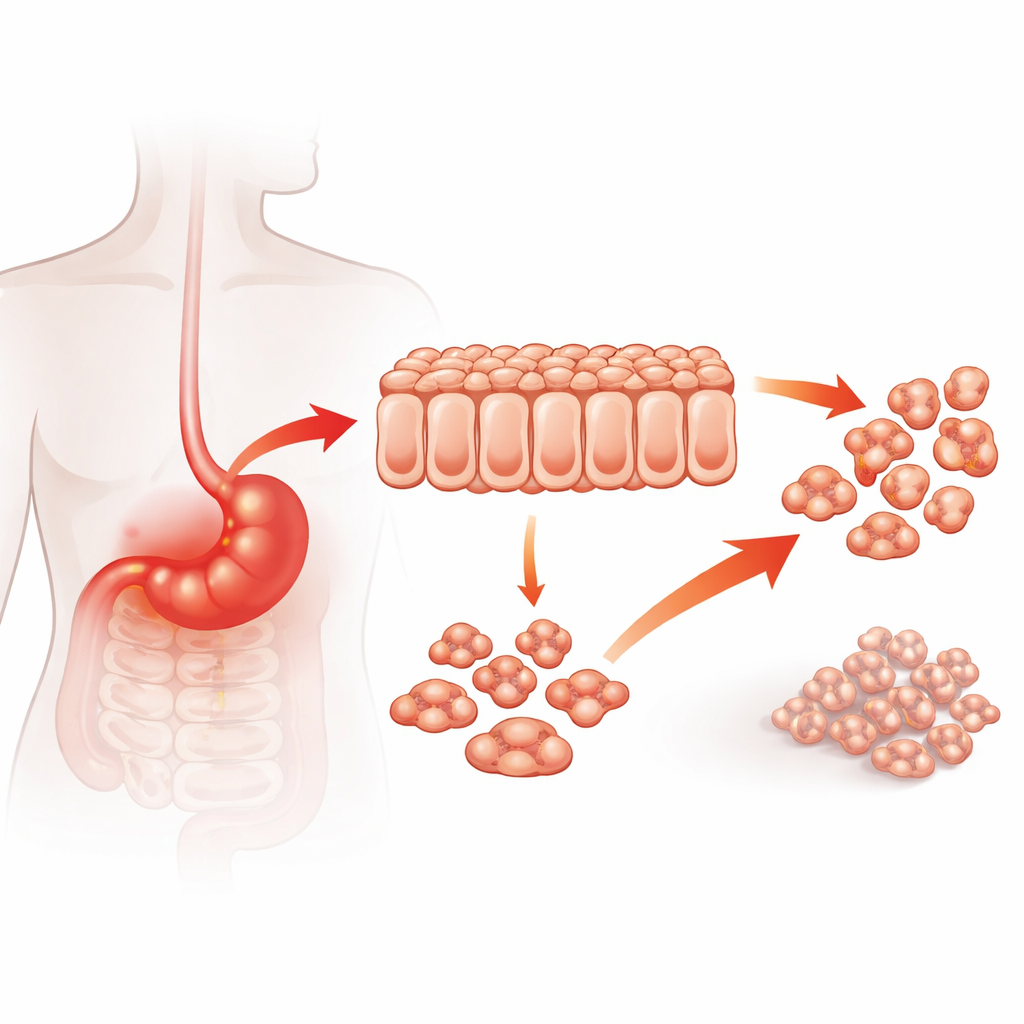
Белок на перекрёстке рака и воспаления
Врачам давно известно, что хроническое воспаление в желудке, например вызванное длительной инфекцией, повышает риск развития рака желудка. A20 — белок, который обычно помогает сдерживать воспалительные сигналы, но в ряде видов рака он ведёт себя скорее как фактор, способствующий росту опухоли. Авторы начали с вопроса, связаны ли уровни A20 в опухолях человека с агрессивностью болезни. Проанализировав образцы опухолей 122 пациентов, они обнаружили, что при высоком уровне A20 опухоли были более инвазивными, чаще распространялись в лимфатические узлы и на отдалённые органы и были связаны с худшей выживаемостью. Эти клинические данные указывают, что A20 — не просто попутчик, а вероятно активный фактор, ускоряющий прогрессирование рака желудка.
Как A20 помогает клеткам рака разрывать связи
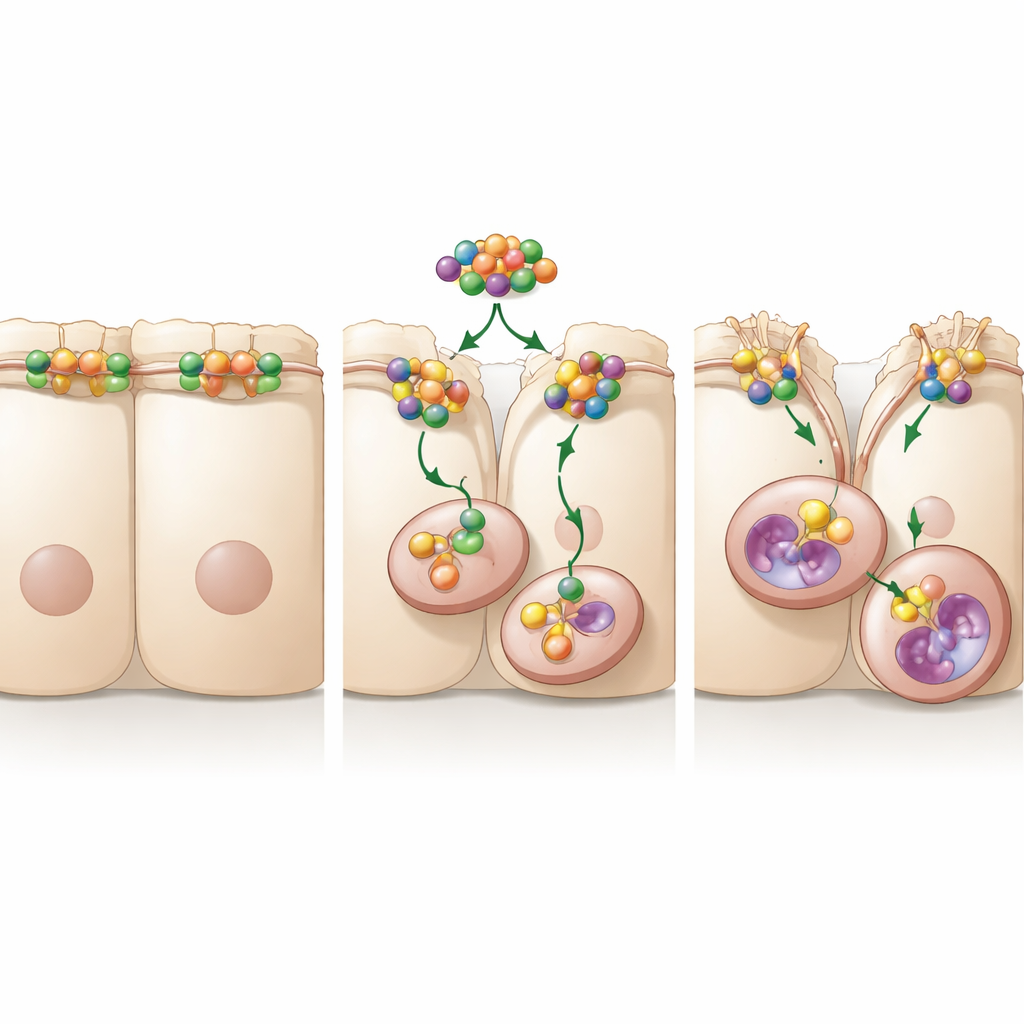
Для метастазирования клеткам рака нужно ослабить плотные связи, которые обычно удерживают соседние клетки вместе. Ключевым компонентом этих связей во многих тканях является белок окклюдин, формирующий плотные контакты, действующие как молекулярные «зубцы» молнии между клетками. В линиях клеток рака желудка, выращенных в лаборатории, исследователи показали, что повышение уровня A20 заставляет клетки расплываться и мигрировать быстрее, тогда как снижение A20 даёт противоположный эффект. Они заметили, что при высоком A20 окклюдин с поверхности клетки исчезает и перемещается внутрь клетки. Подавление окклюдина само по себе было достаточно, чтобы увеличить подвижность раковых клеток, что указывает на то, что потеря этого «замка-молнии» — важный шаг, позволяющий клеткам блуждать.
Понижение «молнии» клетки путём внутреннего разрушения
Команда затем выясняла, как A20 вызывает исчезновение окклюдина. Клетки постоянно перерабатывают свои поверхностные белки, втягивая их в небольшие карманы и отправляя либо на повторное использование, либо на уничтожение. Исследование показало, что A20 ускоряет путь окклюдина с поверхности клетки в эти внутренние карманы, а затем в пищеварительные отделы, напоминающие клеточные центры переработки. Блокирование протеасомного аппарата деградации белков не восстанавливало окклюдин, но блокирование эндоцитоза или кислотных вакуолей — лизосом — оказывало эффект. При таких условиях блокирования клетки мигрировали меньше, даже если A20 был высок. В совокупности эти эксперименты показывают, что A20 способствует распространению рака, стимулируя внутреннюю эндоцитозную маршрутизацию и лизосомную деградацию окклюдина, ослабляя барьер между клетками.
Сигнальная передача, стабилизирующая переключатель подвижности
Углубляясь, исследователи искали партнёров, через которых A20 может контролировать подвижность клетки. Они обнаружили, что A20 связывается с RhoA — небольшим молекулярным переключателем, известным тем, что он перестраивает внутренний скелет клетки и ослабляет клеточные контакты. В присутствии A20 уровни и активность RhoA были выше, а нисходящие сигналы, укрепляющие клеточные фибриллы, сохранялись дольше. Когда RhoA снижали или химически блокировали, уровни окклюдина возвращались к прежним значениям, и миграция клеток замедлялась, даже при высоком A20. Исследование указало на специфический участок A20, называемый OTU-доменом, как на необходимый: при мутации этого участка A20 уже не могла стабилизировать RhoA, не поддерживала сигналы, требуемые для втягивания окклюдина, и не усиливала подвижность клеток. Это свидетельствует о том, что A20 действует как защитник RhoA, оберегая его от пометки на утилизацию и тем самым поддерживая включённый механизм подвижности.
Что это может значить для будущих методов лечения
Проще говоря, эта работа показывает, что A20 помогает клеткам рака желудка убегать, защищая переключатель подвижности (RhoA) и запуская внутреннее уничтожение ключевой «молнии» клетки (окклюдина). Опухоли с повышенным уровнем A20 с большей вероятностью проникают глубже и метастазируют, а пациенты с такими опухолями имеют худший прогноз. Простроив путь A20–RhoA–окклюдин, исследование выделяет несколько потенциальных точек вмешательства: например, препараты, разрушающие OTU-домен A20, снижающие активность RhoA или препятствующие направлению окклюдина в лизосомы. Хотя такие терапии пока недоступны и потребуют аккуратного баланса с нормальными функциями A20 в контроле воспаления, эти результаты дают более чёткую цель для усилий по замедлению или предотвращению смертельно опасного распространения рака желудка.
Цитирование: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Ключевые слова: рак желудка, метастазирование, клеточные соединения, воспаление, сигнализация RhoA