Clear Sky Science · pt
A20 aumenta a migração e a metástase de células do câncer gástrico ao promover a degradação da ocludina
Por que isso importa
O câncer gástrico, ou câncer do estômago, está entre os tumores mais letais do mundo em grande parte porque costuma se espalhar antes de ser detectado. Este estudo revela como uma única proteína ligada à inflamação, chamada A20, ajuda células do câncer de estômago a se desprenderem dos vizinhos e viajarem para órgãos distantes. Ao expor essa via de fuga oculta, o trabalho aponta para novas maneiras pelas quais médicos poderão, algum dia, retardar ou bloquear a disseminação do câncer gástrico.
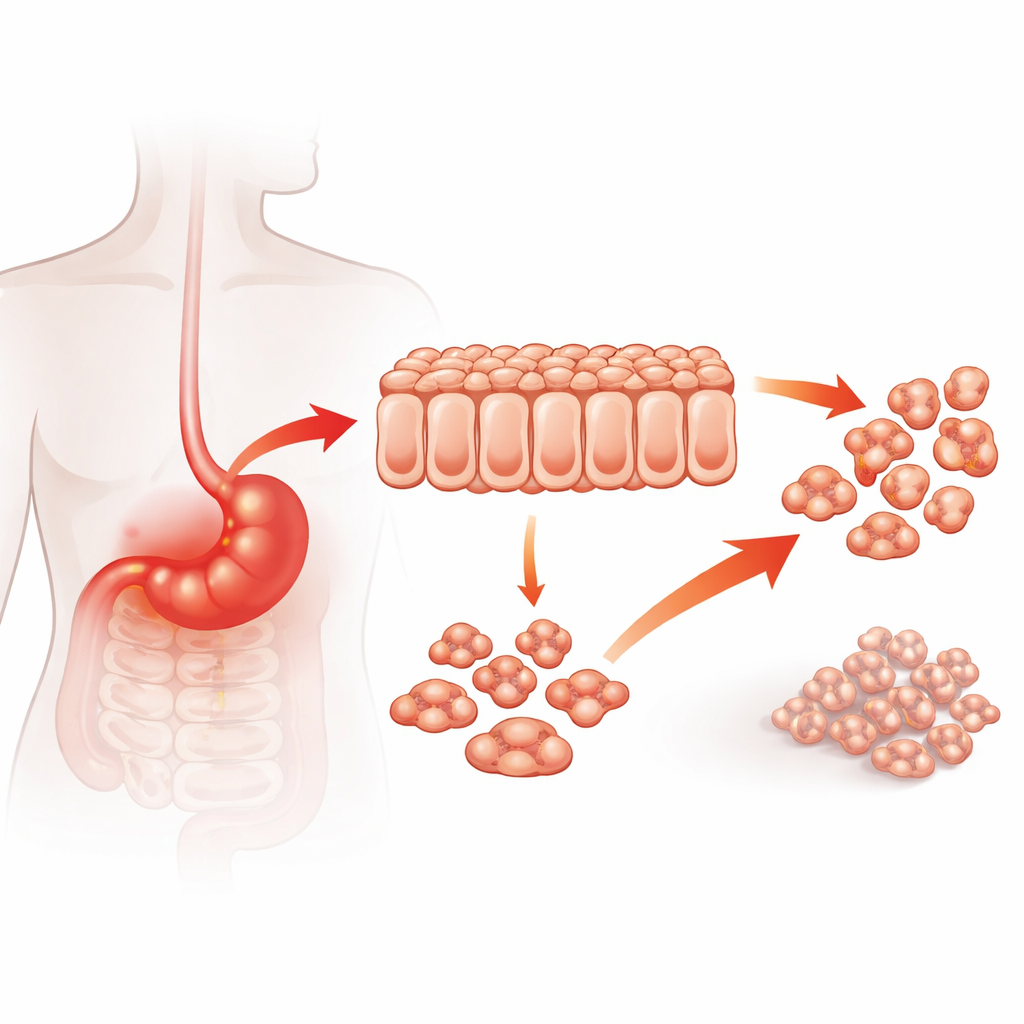
Uma proteína no cruzamento entre câncer e inflamação
Médicos sabem há muito que a inflamação crônica no estômago, como a causada por infecções de longa duração, aumenta o risco de câncer gástrico. A20 é uma proteína que normalmente ajuda a controlar sinais inflamatórios, mas em vários cânceres ela se comporta mais como promotora do crescimento tumoral. Os autores começaram perguntando se os níveis de A20 em tumores gástricos humanos estavam ligados à agressividade do câncer. Ao analisar amostras tumorais de 122 pacientes, encontraram que cânceres com altos níveis de A20 eram mais invasivos, tinham maior probabilidade de ter se espalhado para linfonodos e sítios distantes, e se associavam a pior sobrevida. Esses dados clínicos sugerem que A20 não é apenas um espectador, mas pode impulsionar ativamente o agravamento do câncer gástrico.
Como A20 ajuda as células cancerosas a romper seus vínculos
Para que células cancerosas metastizem, elas precisam afrouxar as ligações firmes que normalmente mantêm as células vizinhas unidas. Um componente chave dessas junções em muitos tecidos é uma proteína chamada ocludina, que ajuda a formar junções apertadas que funcionam como dentes de um zíper molecular entre as células. Em linhagens de células de câncer gástrico cultivadas em laboratório, os pesquisadores mostraram que aumentar os níveis de A20 fez as células se espalharem e migrarem mais rápido, enquanto reduzir A20 teve o efeito oposto. Notaram que, quando A20 estava alto, a ocludina na superfície celular desaparecia e se deslocava para o interior da célula. Silenciar apenas a ocludina foi suficiente para aumentar o movimento das células cancerosas, indicando que a perda desse “zíper” é um passo crucial para permitir que as células se desloquem.
Desligando o “zíper” celular por meio da degradação interna
A equipe então investigou como A20 faz a ocludina desaparecer. As células reciclam constantemente suas proteínas de superfície ao internalizá‑las em pequenas vesículas e enviá‑las para serem reutilizadas ou destruídas. O estudo mostrou que A20 acelera a jornada da ocludina da superfície celular para essas vesículas internas e depois para compartimentos digestivos semelhantes a centros de reciclagem celular. Bloquear a maquinaria de degradação de proteínas no proteossoma não salvou a ocludina, mas bloquear a endocitose ou os sacos ácidos conhecidos como lisossomos sim. Nessas condições de bloqueio, as células cancerosas migraram menos, mesmo quando A20 estava abundante. Juntos, esses experimentos mostram que A20 favorece a disseminação do câncer ao promover a internalização e a degradação lisossomal da ocludina, enfraquecendo a barreira entre as células.
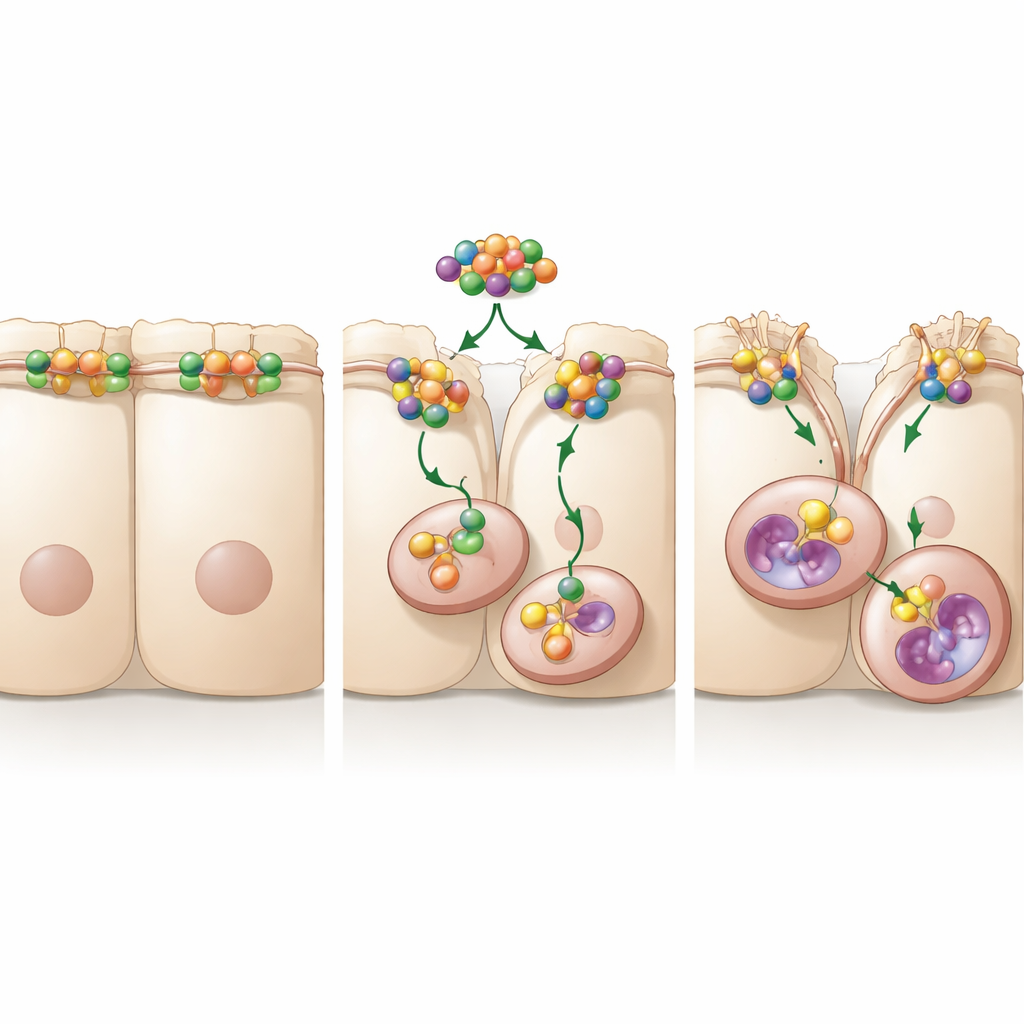
Um circuito de sinalização que estabiliza um interruptor de motilidade
Aprofundando, os pesquisadores buscaram parceiros que pudessem permitir que A20 controlasse o movimento celular. Descobriram que A20 se liga a RhoA, um pequeno interruptor molecular conhecido por remodelar o arcabouço interno da célula e afrouxar junções entre células. Quando A20 estava presente, os níveis e a atividade de RhoA aumentavam, e sinais a jusante que rigidificam fibras celulares eram prolongados. Quando RhoA foi reduzido ou quimicamente bloqueado, os níveis de ocludina voltaram a subir e a migração celular desacelerou, mesmo com A20 elevado. O estudo identificou uma região específica de A20, chamada domínio OTU, como essencial: quando essa região foi mutada, A20 não conseguiu mais estabilizar RhoA, não sustentou a sinalização necessária para internalizar a ocludina e falhou em aumentar o movimento celular. Isso indica que A20 atua como um protetor de RhoA, protegendo‑o de ser marcado para descarte e mantendo assim a maquinaria de motilidade ativada.
O que isso pode significar para tratamentos futuros
Em termos simples, este trabalho mostra que A20 ajuda células do câncer gástrico a escapar ao proteger um interruptor de motilidade (RhoA) e desencadear a degradação interna de um zíper celular chave (occludina). Tumores com mais A20 têm maior probabilidade de invadir profundamente e se espalhar, e pacientes com esses tumores apresentam prognóstico pior ao longo do tempo. Ao mapear essa via A20–RhoA–occludina, o estudo destaca vários pontos potenciais de intervenção, como fármacos que desestabilizem a região OTU de A20, reduzam a atividade de RhoA ou impeçam que a ocludina seja direcionada aos lisossomos. Embora tais tratamentos ainda não estejam disponíveis e precisem ser cuidadosamente equilibrados com os papéis normais de A20 no controle da inflamação, os achados fornecem um alvo mais claro para esforços destinados a retardar ou prevenir a disseminação letal do câncer gástrico.
Citação: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Palavras-chave: câncer gástrico, metástase, junções celulares, inflamação, sinalização RhoA