Clear Sky Science · nl
A20 bevordert migratie en metastase van maagkankercellen door afbraak van occludine te stimuleren
Waarom dit ertoe doet
Maagkanker is een van de dodelijkste tumoren ter wereld, grotendeels omdat hij vaak al is uitgezaaid voordat hij wordt ontdekt. Deze studie onthult hoe één ontstekingsgerelateerd eiwit, A20 genoemd, maagkankercellen helpt los te raken van hun buren en naar verre organen te reizen. Door deze verborgen ontsnappingsroute bloot te leggen, wijst het werk op nieuwe manieren waarop artsen mogelijk de verspreiding van maagkanker in de toekomst kunnen vertragen of blokkeren.
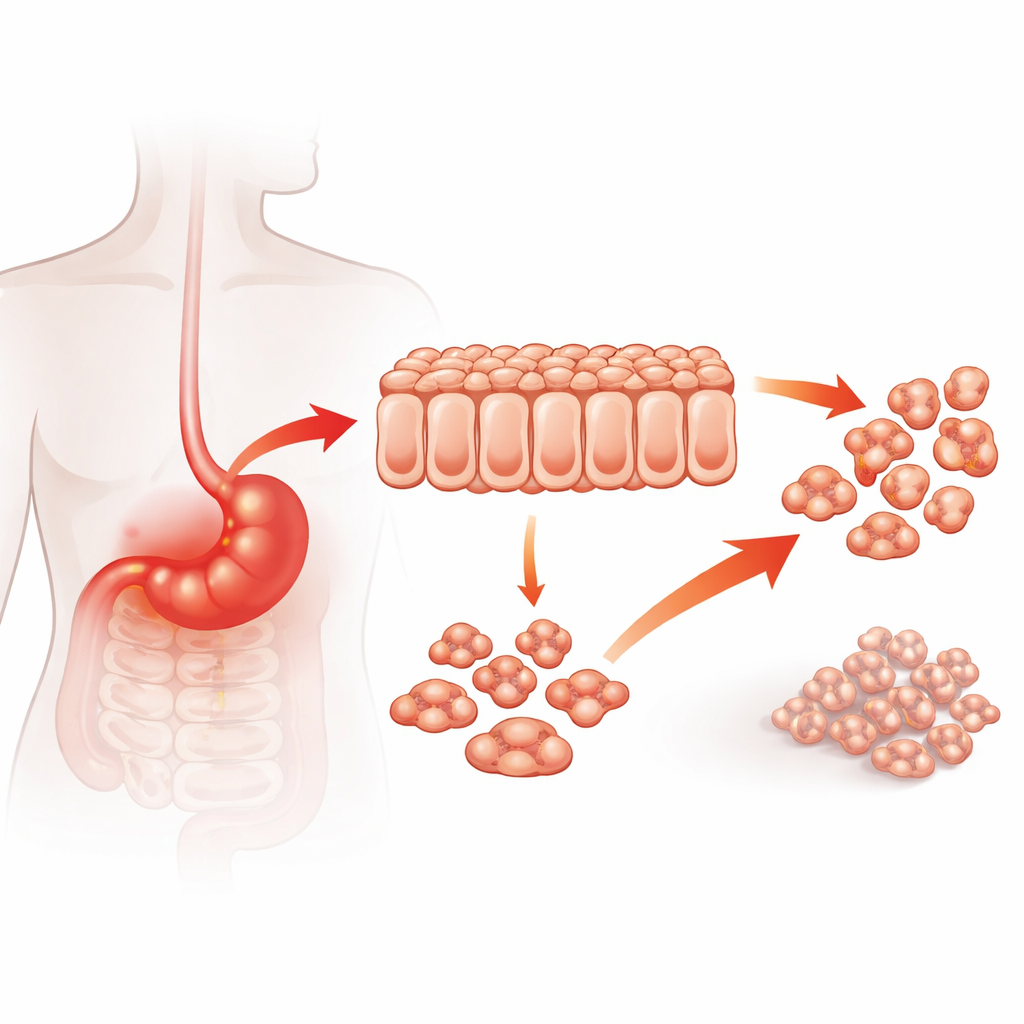
Een eiwit op het kruispunt van kanker en ontsteking
Artsen weten al lang dat chronische maagontsteking, bijvoorbeeld door langdurige infectie, het risico op maagkanker verhoogt. A20 is een eiwit dat normaal gesproken helpt om ontstekingssignalen in toom te houden, maar in verschillende kankers gedraagt het zich eerder als een bevorderaar van tumorgroei. De auteurs vroegen zich eerst af of A20-niveaus in menselijke maagtumoren samenhangen met hoe agressief de kanker is. Bij analyse van tumormonsters van 122 patiënten vonden ze dat kankers met hoge A20-niveaus invasiever waren, vaker naar lymfeklieren en verre locaties waren uitgezaaid en geassocieerd waren met slechtere overleving. Deze klinische gegevens suggereerden dat A20 geen toeschouwer is, maar mogelijk actief bijdraagt aan het verergeren van maagkanker.
Hoe A20 kankercellen helpt hun bindingen te verbreken
Om te metastaseren moeten kankercellen de sterke verbindingen tussen naburige cellen losser maken. Een sleutelcomponent van deze verbindingen in veel weefsels is het eiwit occludine, dat helpt bij het vormen van tight junctions—als het ware moleculaire rits(tanden) tussen cellen. In maagkankercellijnen in het laboratorium toonden de onderzoekers aan dat het verhogen van A20-cijfers cellen deed uitzwermen en sneller laat migreren, terwijl verlaging van A20 het tegengestelde effect had. Ze merkten dat bij hoge A20 occludine aan het celoppervlak verloren ging en naar het celinterieur verschoof. Alleen het stilleggen van occludine was al genoeg om de beweging van kankercellen te verhogen, wat aangeeft dat het verlies van deze “rits” een cruciale stap is om cellen te laten zwerven.
De “rits” naar beneden draaien via interne afbraak
Het team onderzocht vervolgens hoe A20 ervoor zorgt dat occludine verdwijnt. Cellen recyclen constant hun oppervlakte-eiwitten door ze via kleine instulpingen naar binnen te halen en ze óf opnieuw te gebruiken óf te laten afbreken. De studie vond dat A20 de reis van occludine van het celoppervlak naar deze interne compartimenten en vervolgens naar verteringscompartimenten vergelijkbaar met recyclingcentra versnelt. Het blokkeren van het proteasoom, het cellulaire eiwitvermalingssysteem, herstelde occludine niet, maar het blokkeren van endocytose of van de zure zakken die lysosomen heten, wel. Onder deze blokkering migreerden kankercellen minder, zelfs bij overvloedige A20. Samen tonen deze experimenten aan dat A20 de verspreiding van kanker aanmoedigt door de internalisatie en lysosomale afbraak van occludine te bevorderen, waardoor de barrière tussen cellen verzwakt.
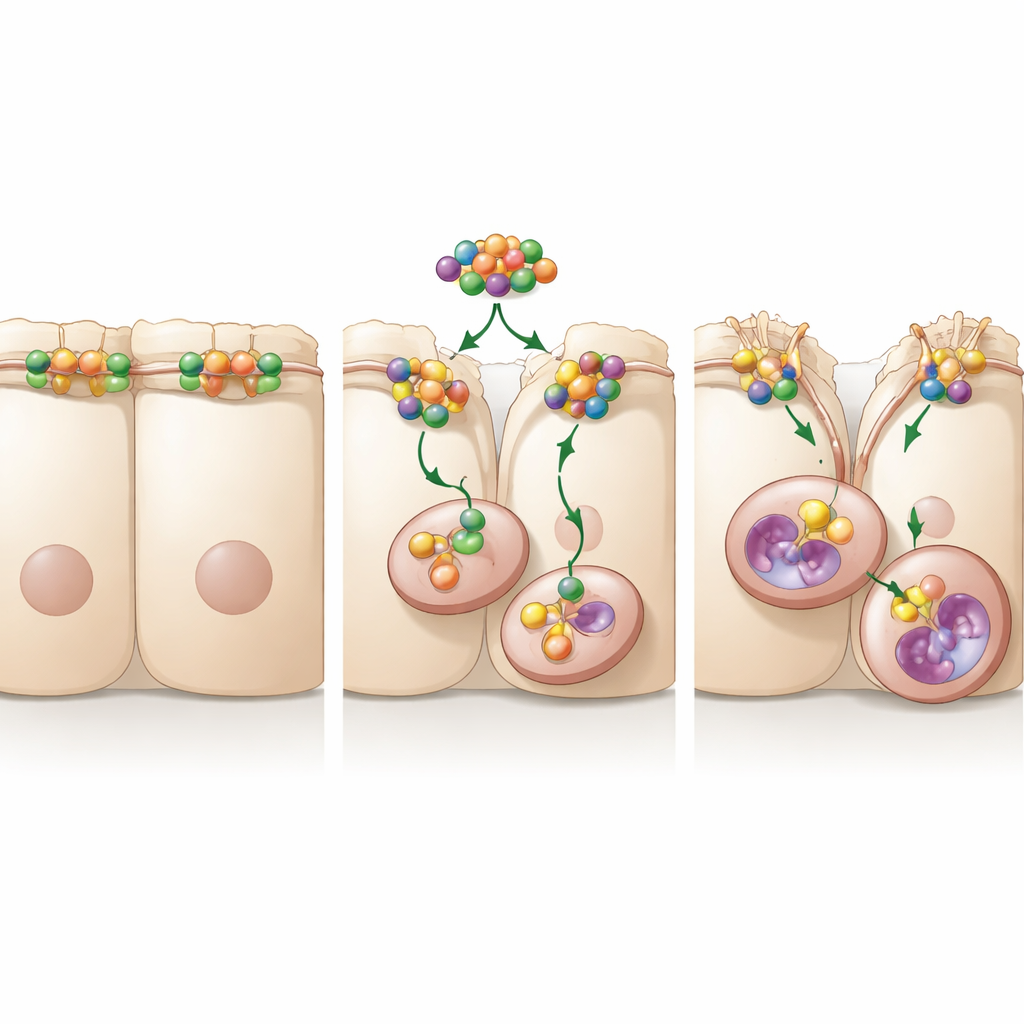
Een signaleringsrelais dat een mobiliteitsschakelaar stabiliseert
Dieper gravend zochten de onderzoekers naar partners die A20 in staat zouden stellen celbeweging te beheersen. Ze ontdekten dat A20 bindt aan RhoA, een kleine moleculaire schakelaar die het inwendige stevigheidskader van de cel kan hervormen en de verbindingen tussen cellen kan versoepelen. Wanneer A20 aanwezig was, waren RhoA-niveaus en -activiteit hoger en werden downstreamsignalen die cellulaire vezels verankeren verlengd. Wanneer RhoA werd verlaagd of chemisch geblokkeerd, stegen occludineniveaus weer en vertraagde celmigratie, zelfs als A20 hoog was. De studie wees een specifiek gebied van A20 aan, het OTU-domein, als essentieel: wanneer dit gebied gemuteerd werd, kon A20 RhoA niet meer stabiliseren, kon het de signalering die nodig is om occludine naar binnen te trekken niet in stand houden en faalde het in het versterken van celbeweging. Dit wijst erop dat A20 als bewaker van RhoA fungeert, het beschermt tegen merkers voor afbraak en zo de mobiliteitsmachine ingeschakeld houdt.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
In eenvoudige termen laat dit werk zien dat A20 maagkankercellen helpt ontsnappen door een mobiliteitsschakelaar (RhoA) te beschermen en de interne afbraak van een sleutelrits (occludine) te veroorzaken. Tumoren met meer A20 hebben meer kans om diep te infiltreren en uit te zaaien, en patiënten met zulke tumoren hebben op termijn een slechtere prognose. Door het A20–RhoA–occludinepad in kaart te brengen, benadrukt de studie verschillende potentiële interventiepunten, zoals middelen die het OTU-domein van A20 verstoren, RhoA-activiteit verminderen of voorkomen dat occludine naar lysosomen wordt geleid. Hoewel dergelijke behandelingen nog niet beschikbaar zijn en zorgvuldig afgewogen moeten worden tegen de normale functies van A20 bij het reguleren van ontsteking, bieden de bevindingen een duidelijker doel voor pogingen om de dodelijke verspreiding van maagkanker te vertragen of te voorkomen.
Bronvermelding: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Trefwoorden: maagkanker, metastase, celverbindingen, ontsteking, RhoA‑signalering