Clear Sky Science · es
A20 potencia la migración y metástasis de las células del cáncer gástrico al promover la degradación de ocludina
Por qué esto importa
El cáncer gástrico, o cáncer de estómago, es uno de los tumores más mortales del mundo, en gran parte porque con frecuencia se disemina antes de detectarse. Este estudio revela cómo una única proteína relacionada con la inflamación, llamada A20, ayuda a las células del cáncer de estómago a separarse de sus vecinas y viajar a órganos distantes. Al desvelar esta vía de escape oculta, el trabajo señala nuevas formas en que los médicos podrían, algún día, frenar o bloquear la propagación del cáncer gástrico.
Una proteína en la encrucijada entre cáncer e inflamación
Los médicos saben desde hace tiempo que la inflamación crónica en el estómago, como la causada por una infección de larga duración, aumenta el riesgo de cáncer gástrico. A20 es una proteína que normalmente ayuda a mantener bajo control las señales inflamatorias, pero en varios cánceres actúa más bien como promotora del crecimiento tumoral. Los autores empezaron preguntándose si los niveles de A20 en tumores gástricos humanos se relacionaban con la agresividad del cáncer. Analizando muestras tumorales de 122 pacientes, encontraron que los cánceres con niveles altos de A20 eran más invasivos, tenían mayor probabilidad de haberse diseminado a ganglios linfáticos y sitios distantes, y se asociaban con una supervivencia peor. Estos datos clínicos sugieren que A20 no es solo un observador, sino que puede impulsar activamente el empeoramiento del cáncer gástrico.
Cómo A20 ayuda a las células cancerosas a soltarse
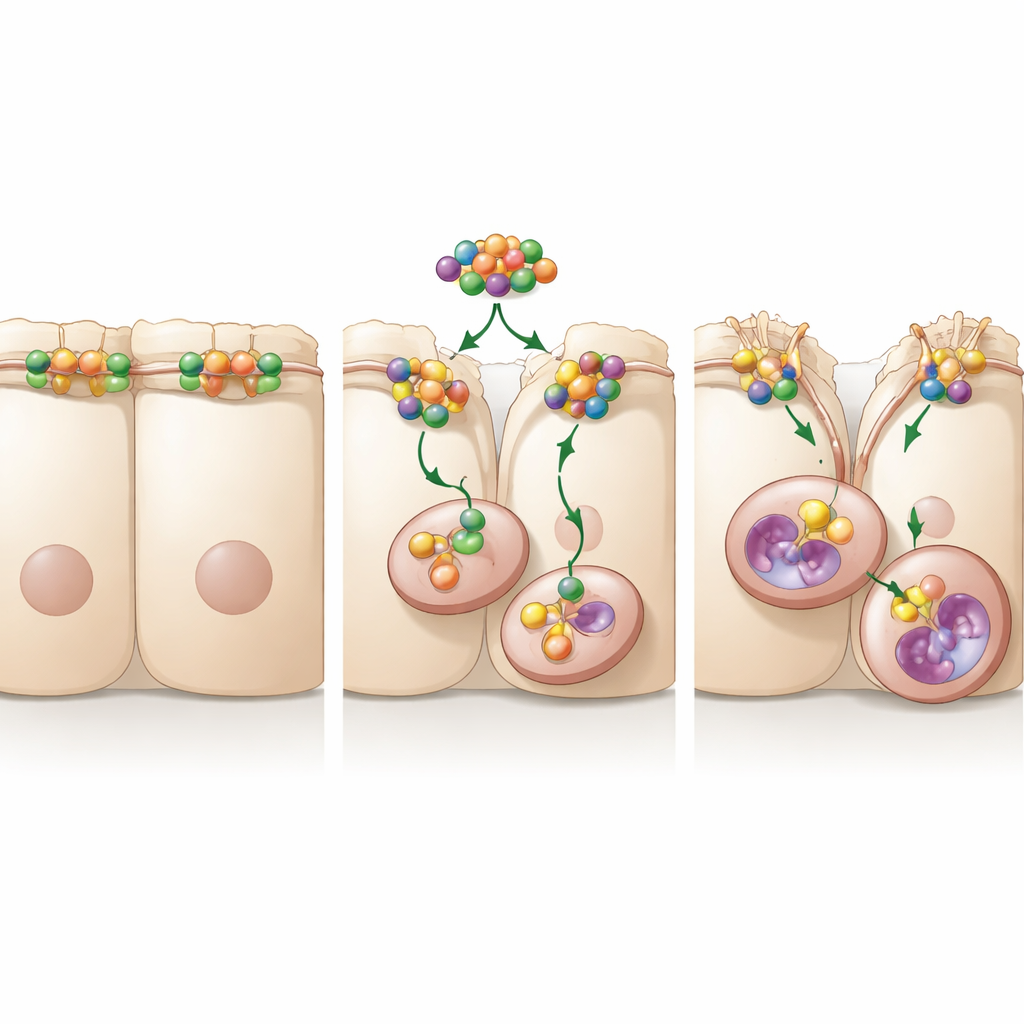
Para metastatizar, las células cancerosas deben aflojar los fuertes lazos que normalmente mantienen unidas a las células vecinas. Un componente clave de estos lazos en muchos tejidos es una proteína llamada ocludina, que ayuda a formar las uniones estrechas que funcionan como dientes de una cremallera molecular entre las células. En líneas celulares de cáncer gástrico cultivadas en el laboratorio, los investigadores mostraron que aumentar los niveles de A20 hizo que las células se dispersaran y migraran más rápido, mientras que reducir A20 tuvo el efecto contrario. Observaron que cuando A20 era alto, la ocludina en la superficie celular desaparecía y se desplazaba hacia el interior de la célula. Silenciar la ocludina por sí solo fue suficiente para aumentar el movimiento de las células cancerosas, lo que indica que la pérdida de esta “cremallera” es un paso crucial para que las células puedan desplazarse.
Bajar la “cremallera” celular mediante su desgarro interno
El equipo preguntó a continuación cómo A20 hace que la ocludina desaparezca. Las células reciclan constantemente sus proteínas de superficie internalizándolas en pequeñas bolsas y enviándolas o bien a ser reutilizadas o bien a ser destruidas. El estudio encontró que A20 acelera el recorrido de la ocludina desde la superficie celular hacia esas bolsas internas y luego hacia compartimentos digestivos similares a centros de reciclaje celular. Bloquear la maquinaria de destrucción de proteínas en el proteasoma no rescató la ocludina, pero bloquear la endocitosis o los sacos ácidos conocidos como lisosomas sí lo hizo. Bajo estas condiciones de bloqueo, las células cancerosas migraron menos, incluso cuando A20 era abundante. En conjunto, estos experimentos muestran que A20 favorece la diseminación del cáncer promoviendo la internalización y la degradación lisosomal de la ocludina, debilitando la barrera entre las células.
Un relevo de señalización que estabiliza un interruptor de motilidad
Ahondando más, los investigadores buscaron socios que pudieran permitir a A20 controlar el movimiento celular. Descubrieron que A20 se une a RhoA, un pequeño interruptor molecular conocido por reorganizar el armazón interior de la célula y aflojar las uniones entre células. Cuando A20 estaba presente, los niveles y la actividad de RhoA eran mayores, y las señales aguas abajo que rigidizan las fibras celulares se prolongaban. Cuando RhoA se redujo o se bloqueó químicamente, los niveles de ocludina volvieron a aumentar y la migración celular se ralentizó, aunque A20 fuera alto. El estudio identificó una región específica de A20, llamada dominio OTU, como esencial: cuando esta región se mutó, A20 ya no pudo estabilizar RhoA, no pudo sostener la señalización necesaria para internalizar la ocludina y no consiguió aumentar el movimiento celular. Esto indica que A20 actúa como guardián de RhoA, protegiéndolo de ser señalado para su eliminación y manteniendo así activada la maquinaria de motilidad.
Qué podría significar esto para tratamientos futuros
En términos sencillos, este trabajo muestra que A20 ayuda a las células del cáncer gástrico a escapar protegiendo un interruptor de motilidad (RhoA) y desencadenando el desgarro interno de una cremallera celular clave (occludina). Los tumores con más A20 son más propensos a invadir profundamente y diseminarse, y los pacientes con este tipo de tumores presentan peores resultados a lo largo del tiempo. Al trazar la vía A20–RhoA–occludina, el estudio destaca varios puntos potenciales de intervención, como fármacos que interrumpan la región OTU de A20, reduzcan la actividad de RhoA o impidan que la ocludina sea dirigida a los lisosomas. Aunque tales tratamientos aún no están disponibles y tendrían que equilibrarse cuidadosamente con los roles normales de A20 en el control de la inflamación, los hallazgos proporcionan un objetivo más claro para los esfuerzos destinados a frenar o prevenir la propagación mortal del cáncer gástrico.
Cita: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Palabras clave: cáncer gástrico, metástasis, uniones celulares, inflamación, señalización RhoA