Clear Sky Science · tr
A20, sıkı bağlantı proteini occludin’in parçalanmasını teşvik ederek mide kanseri hücrelerinin göç ve metastazını artırır
Niçin önemli
Mide kanseri, yani midenin kanseri, çoğunlukla tespit edilmeden önce yayılmaya meyilli olduğu için dünya genelinde en ölümcül tümörlerden biridir. Bu çalışma, A20 adı verilen ve inflamasyonla bağlantılı tek bir proteinin, mide kanseri hücrelerinin komşu hücrelerden ayrılmasına ve uzak organlara göç etmesine nasıl yardımcı olduğunu ortaya koyuyor. Bu gizli kaçış yolunu açığa çıkararak çalışma, gelecekte doktorların mide kanserinin yayılmasını yavaşlatmak veya engellemek için kullanabileceği yeni yaklaşımlara işaret ediyor.
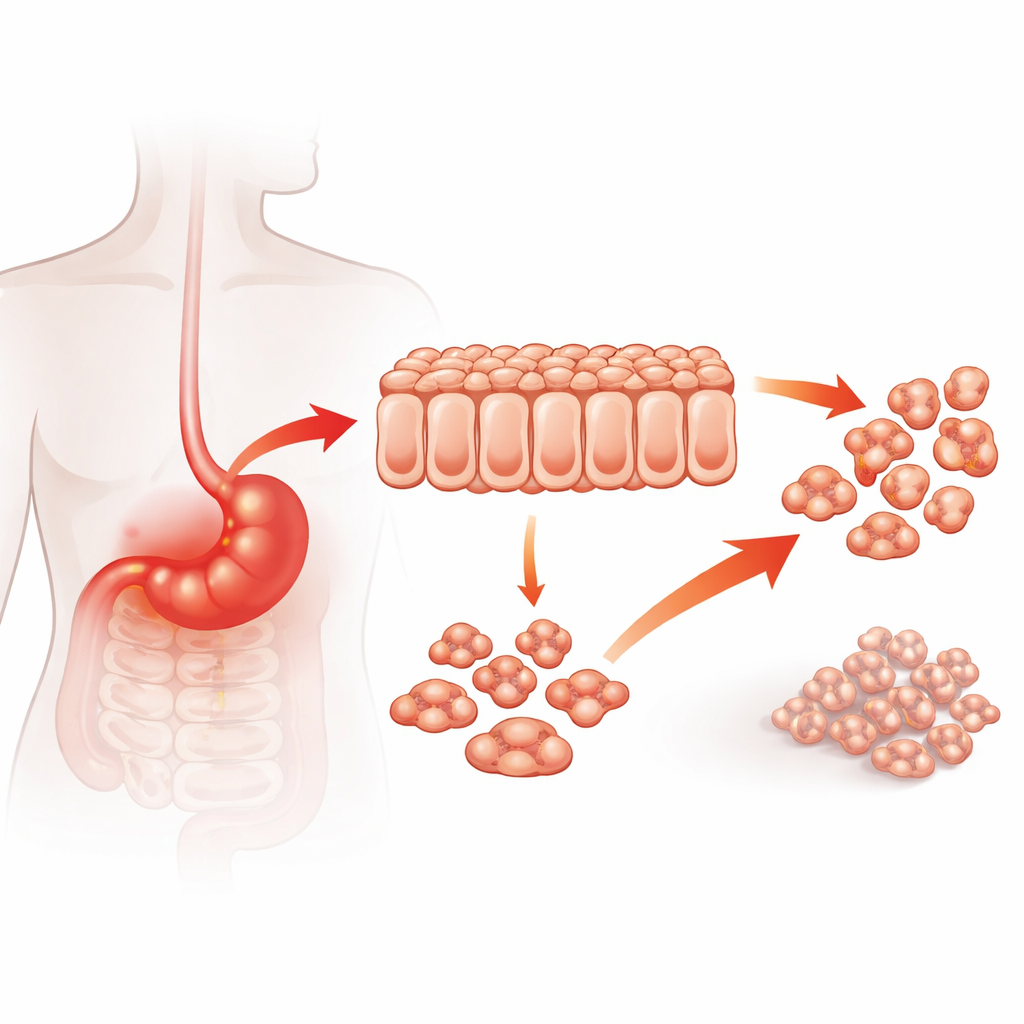
Kanser ile inflamasyonun kavşağındaki bir protein
Doktorlar uzun süredir midedeki kronik inflamasyonun, örneğin uzun süreli enfeksiyonların, mide kanseri riskini artırdığını biliyor. A20 genellikle inflamatuar sinyalleri dizginlemeye yardımcı olan bir proteindir, ancak birkaç kanserde tümör büyümesini destekleyen bir rol oynar. Yazarlar önce insan mide tümörlerindeki A20 düzeylerinin kanserin ne kadar agresif olduğu ile ilişkisinin olup olmadığını sordular. 122 hastadan alınan tümör örneklerini analiz ettiklerinde, A20 düzeyi yüksek olan kanserlerin daha invaziv, lenf düğümlerine ve uzak bölgelere daha çok yayılmış ve daha kötü sağkalım ile ilişkili olduğunu buldular. Bu klinik veriler, A20’in yalnızca bir seyirci olmadığını, mide kanserinin kötüleşmesini aktif olarak hızlandırıyor olabileceğini gösterdi.
A20’in kanser hücrelerinin bağlarını gevşetmesine nasıl yardımcı olduğu
Kanser hücrelerinin metastaz yapabilmesi için normalde komşu hücreleri bir arada tutan sıkı bağları gevşetmeleri gerekir. Birçok dokuda bu bağların kilit bileşenlerinden biri, hücreler arasındaki moleküler fermuar dişleri gibi işlev gören sıkı bağlantılar oluşturmaya yardımcı olan occludin adlı bir proteindir. Laboratuvarda büyütülen mide kanseri hücre hatlarında araştırmacılar, A20 düzeylerini artırmanın hücrelerin yayılmasına ve daha hızlı göç etmesine yol açtığını, A20’i azaltmanın ise ters etki yarattığını gösterdiler. A20 yüksek olduğunda hücre yüzeyindeki occludin’in kaybolduğunu ve hücre iç kısmına kaydığını gözlemlediler. Sadece occludin’in susturulması bile kanser hücresi hareketini artırmaya yeterliydi; bu da bu “fermuar”ın kaybının hücrelerin dolaşmasına izin veren kritik bir adım olduğunu gösteriyor.
Hücresel “fermuar”ı içten parçalatarak kapatmak
Ekip bir sonraki adımda A20’in occludin’i nasıl ortadan kaldırdığını sordu. Hücreler, yüzey proteinlerini küçük cepçiklerle içeri çekerek sürekli olarak geri dönüştürür; bu proteinler ya yeniden kullanılmaya gönderilir ya da yok edilmek üzere sindirim bölmelerine yollanır. Çalışma, A20’in occludin’in hücre yüzeyinden bu iç cepçiklere ve ardından hücresel geri dönüşüm merkezlerine benzer sindirim bölmelerine gidişini hızlandırdığını buldu. Proteazomdaki protein parçalama makinesini bloke etmek occludin’i kurtarmadı, ancak endositoz veya asidik kesecikler olan lizozomları engellemek işe yaradı. Bu engelleme koşullarında, A20 bol olsa bile kanser hücreleri daha az göç etti. Birlikte, bu deneyler A20’in occludin’in içselleştirilmesini ve lizozomal parçalanmasını teşvik ederek hücreler arasındaki bariyeri zayıflattığını ve kanserin yayılmasını desteklediğini gösteriyor.
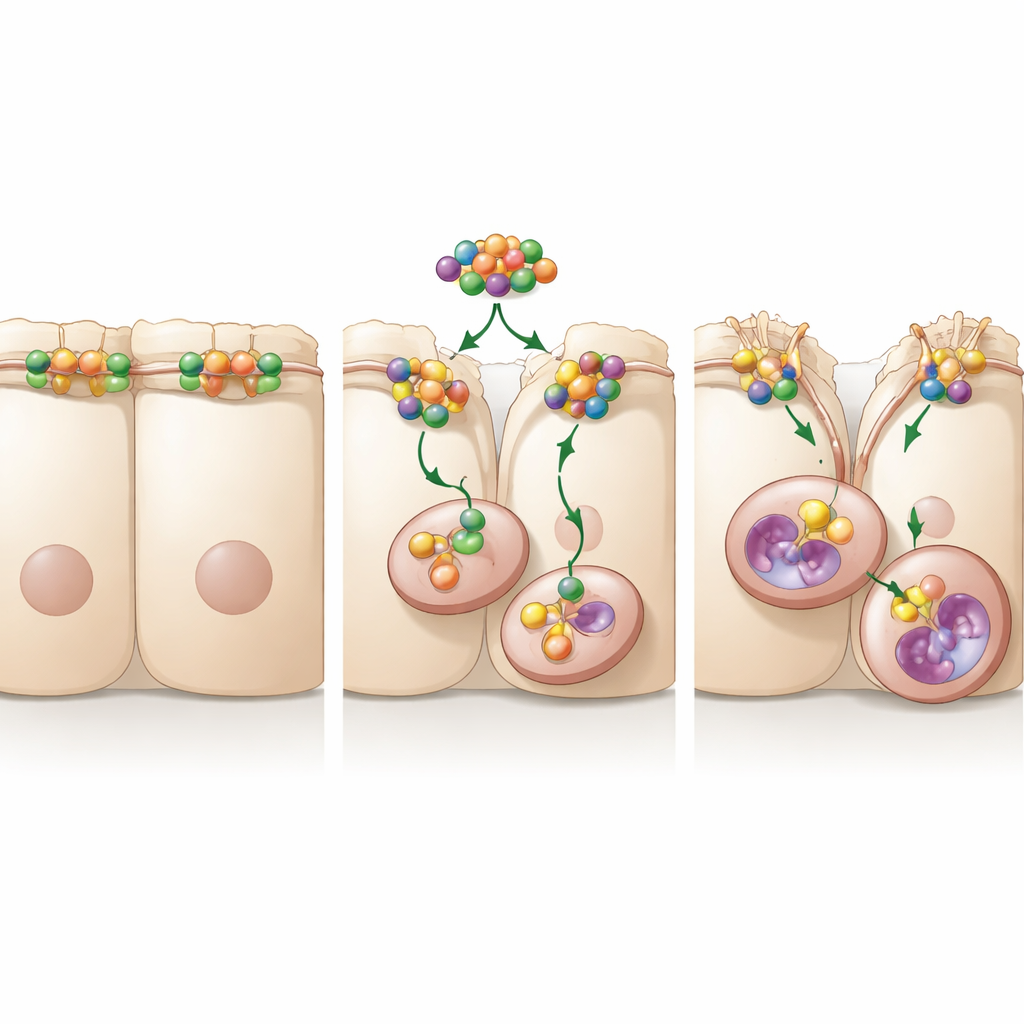
Hareketlilik anahtarını kararlı kılan bir sinyal rölesi
Daha derine indiklerinde, araştırmacılar A20’in hücre hareketini kontrol etmesine izin verebilecek ortaklar aradılar. A20’in, hücrenin iç iskeletini yeniden şekillendiren ve hücreler arasındaki bağlantıları gevşeten küçük bir moleküler anahtar olan RhoA ile bağlandığını keşfettiler. A20 bulunduğunda RhoA düzeyleri ve aktivitesi artıyordu ve hücresel lifleri sertleştiren aşağı akış sinyalleri daha uzun sürdü. RhoA azaltıldığında veya kimyasal olarak bloke edildiğinde occludin düzeyleri geri yükseldi ve hücre göçü yavaşladı, A20 yüksek olsa bile. Çalışma, A20’in OTU adı verilen belli bir bölgesini kritik olarak işaretledi: bu bölge mutasyona uğradığında A20 artık RhoA’yı stabilize edemiyor, occludin’i içeri çekmek için gereken sinyali sürdüremiyor ve hücre hareketini artırmada başarısız oluyordu. Bu, A20’in RhoA’yı atılmaya işaretlenmekten koruyan bir gardiyan gibi davrandığını ve böylece hareketlilik mekanizmasını etkin tuttuğunu gösteriyor.
Gelecekteki tedaviler için olası çıkarımlar
Basitçe söylemek gerekirse, bu çalışma A20’in mide kanseri hücrelerinin kaçmasına yardımcı olduğunu; bunu bir hareketlilik anahtarını (RhoA) koruyarak ve hücresel bir fermuarın (occludin) içsel parçalanmasını tetikleyerek yaptığını gösteriyor. Daha fazla A20 barındıran tümörler daha derin invazyon ve yayılma eğiliminde ve bu tür tümörleri olan hastaların zaman içinde daha kötü sonuçlar aldığı görülüyor. A20–RhoA–occludin yolunu haritalandırarak çalışma, A20’in OTU bölgesini bozacak ilaçlar, RhoA aktivitesini azaltacak yaklaşımlar veya occludin’in lizozomlara yönlendirilmesini engelleyecek stratejiler gibi birkaç olası müdahale noktasını öne çıkarıyor. Bu tür tedaviler henüz mevcut olmasa da ve A20’in inflamasyonu kontrol etmedeki normal rollerine karşı dikkatle dengelenmesi gerekecek olsa da, bulgular mide kanserinin ölümcül yayılmasını yavaşlatma veya önleme çabaları için daha net hedefler sağlıyor.
Atıf: Kuo, YT., Wang, HC. & Shan, YS. A20 enhances the migration and metastasis of gastric cancer cells by promoting occludin degradation. Cell Death Discov. 12, 206 (2026). https://doi.org/10.1038/s41420-026-03082-2
Anahtar kelimeler: mide kanseri, metastaz, hücre bağlantıları, inflamasyon, RhoA sinyalleşmesi